Để đốt cháy hoàn toàn 3,36 lít khí X gồm CO và một hidrocacbon A cần 16,8 gam oxi. Dẫn sản phẩm cháy qua bình (I) đựng P2O5, sau đó dẫn tiếp qua bình (II) đựng dung dịch Ba(OH)2 dư thấy khối lượng bình (I) tăng 7,2 gam, bình (II) có 68,95 gam kết tủa. Xác định công thức phân tử, công thức cấu tạo của A và tính phần trăm thể tích của mỗi khí trong X.
 Giải bởi Vietjack
Giải bởi Vietjack
Số mol các chất là:
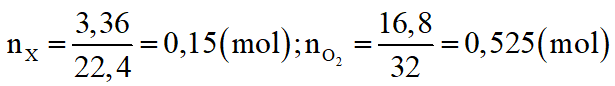
Đặt công thức của A là CxHy.
Sơ đồ phản ứng:
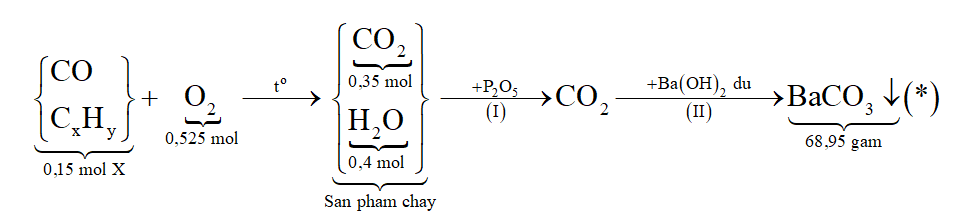
Bình đựng P2O5 hấp thụ H2O, do đó khối lượng bình tăng chính là khối lượng H2O.
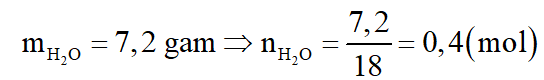
Khí đi ra khỏi bình (I) là CO2, được hấp thụ vào bình đựng dung dịch Ba(OH)2 dư:
Phương trình hóa học:
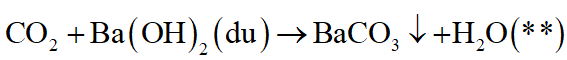
Kết tủa thu được là BaCO3
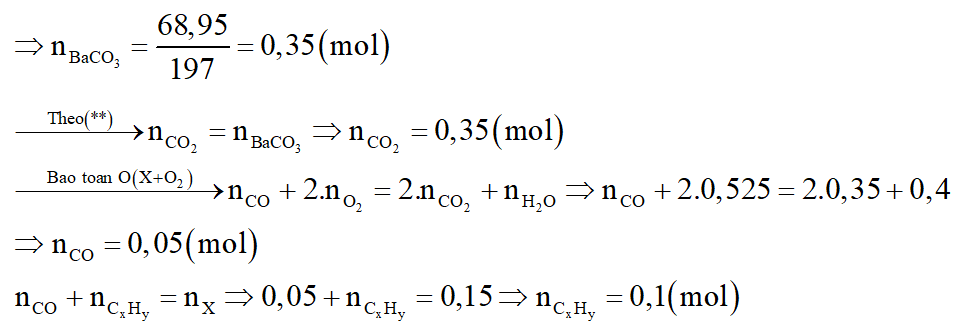
Phần trăm thể tích mỗi khí trong X là:
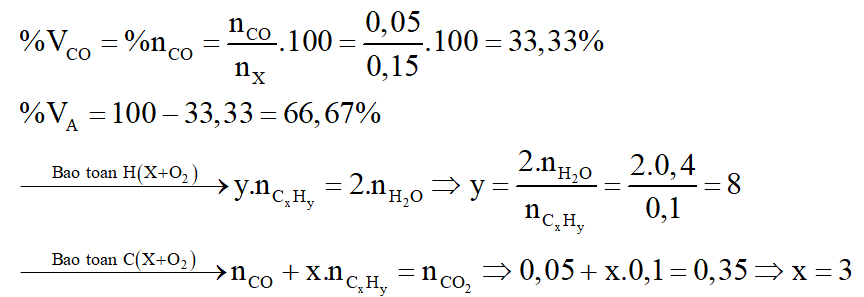
Vậy công thức phân tử của A là: C3H8.
Công thức cấu tạo của A là: CH3 – CH2 – CH3.
Dẫn từ từ 5,60 lít hỗn hợp Y gồm C2H4 và C2H6 đi vào dung dịch brom thấy dung dịch brom nhạt màu và còn 4,48 lít khí thoát ra. Các thể tích khí đo ở điều kiện tiêu chuẩn. Xác định phần trăm khối lượng các chất trong Y.
Có các khí sau đựng riêng biệt trong mỗi bình không dán nhãn: C2H4, HCl, Cl2, CH4. Hãy nêu phương pháp hóa học để phân biệt mỗi khí.