Lithium (Li) là kim loại quan trọng trong các ngành công nghiệp như pin điện, chế tạo hợp kim,... Kim loại Li được điều chế bằng cách điện phân hỗn hợp \({\rm{LiCl}} - {\rm{KCl}}\) với tỉ lệ khối lượng khoảng 6: 4 ở nhiệt độ \(425 - {500^o }{\rm{C}}.\) Hiệu suất điện phân đạt 75%. Khối lượng kim loại Li (theo kg ) thu được từ 1 tấn hỗn hợp \({\rm{LiCl}} - {\rm{KCl}}\) ban đầu là bao nhiêu?
(Làm tròn kết quả đến hàng phần mười)
 Giải bởi Vietjack
Giải bởi Vietjack
Khối lượng \({\rm{LiCl}} = 600\;{\rm{kg}} \Rightarrow \) khối lượng LiCl điện phân \( = 450\;{\rm{kg}}\)
\(2{\rm{LiCl}} \to 2{\rm{Li}} + {\rm{C}}{{\rm{l}}_2}\)
Khối lượng Li thu được \( = \frac{7}{{42,5}} \cdot 450 = 74,1(\;{\rm{kg}})\)
Điện phân các dung dịch chất điện li trong nước với các điện cực trơ. Cho các phát biểu sau:
(a) Khi có dòng điện chạy qua, các ion sẽ di chuyển về các điện cực trái dấu.
(b) Tại anode chỉ xảy ra quá trình oxi hoá các anion hoặc \({{\rm{H}}_2}{\rm{O}}.\)
(c) Tại cathode chỉ xảy ra quá trình khử các cation hoặc \({{\rm{H}}_2}{\rm{O}}.\)
(d) Khối lượng dung dịch điện phân giảm trong quá trìnhh điện phân.
Số phát biểu đúng là
Cho các phát biểu sau:
(a) Các chất tham gia phản ứng điện phân là các hợp chất ion.
(b) Trong đa số trường hợp, tại cực âm, chất có tính oxi hoá lớn hơn sẽ bị điện phân trước.
(c) Trong đa số trường hợp, tại cực dương, chất có tính khử lớn hơn sẽ bị điện phân trước.
(d) Tại các điện cực, các ion luôn bị điện phân trước các phân tử.
Số phát biểu đúng là
Điện phân nóng chảy hỗn hợp gồm aluminium oxide \(\left( {{\rm{A}}{{\rm{l}}_2}{{\rm{O}}_3}} \right)\) và cryolite \(\left( {{\rm{N}}{{\rm{a}}_3}{\rm{Al}}{{\rm{F}}_6}} \right)\) để sản xuất nhôm \(({\rm{Al}})\) trong công nghiệp. Cho các vai trò sau của cryolite:
(1) Tạo với \({\rm{A}}{{\rm{l}}_2}{{\rm{O}}_3}\) thành hỗn hợp có nhiệt độ nóng chảy thấp hơn nhiều nhiệt độ nóng chảy \({\rm{A}}{{\rm{l}}_2}{{\rm{O}}_3}.\)
(2) Tăng khả năng dẫn điện của hỗn hợp điện phân do sự điện li tạo thành các ion.
(3) Hình thành lớp màng ngăn cản sự tiếp xúc giữa \({\rm{Al}}(i)\) mới sinh với không khí.
Hãy cho biết những vai trò nào đúng với cryolite trong quá trình sản xuất nhôm trong công nghiệp.
Điện phân dung dịch \({\rm{CuS}}{{\rm{O}}_4}0,1{\rm{M}}\) với các điện cực trơ. Các quá trình có thể xảy ra tại cathode như sau:
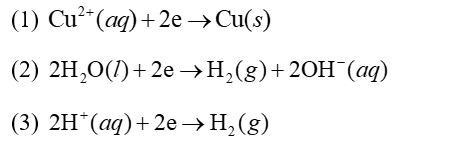
Thứ tự các quá trình điện phân tại cathode là