Trong phòng thí nghiệm, cần điều chế 2,479 L khí hydrogen (ở 25 °C, 1 Bar). Người ta cho kẽm (zinc) tác dụng với dung dịch H2SO4 9,8% (hiệu suất phản ứng 100%).
Tính khối lượng dung dịch H2SO4 cần dùng.
 Giải bởi Vietjack
Giải bởi Vietjack
Số mol H2 cần điều chế:
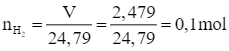
Zn + H2SO4 → ZnSO4 + H2
Theo PTHH: 1 1 mol
Phản ứng: 0,1 ← 0,1 mol
Vậy khối lượng H2SO4 có trong dung dịch: 0,1.98 = 9,8 gam.
Khối lượng dung dịch H2SO4 9,8% cần dùng là:
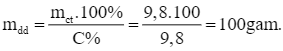
Trong phòng thí nghiệm, cần điều chế 2,479 L khí hydrogen (ở 25 °C, 1 Bar). Người ta cho kẽm (zinc) tác dụng với dung dịch H2SO4 9,8% (hiệu suất phản ứng 100%).
Viết PTHH của phản ứng xảy ra.
Ghép dụng cụ ở cột A với mục đích sử dụng ở cột B sao cho phù hợp:
|
Cột A |
|
Cột B |
|
1) Ống đong |
|
a) Để đặt các ống nghiệm |
|
2) Lọ thuỷ tinh |
|
b) Để khuấy khi hoà tan chất rắn |
|
3) Giá để ống nghiệm |
|
c) Để đong một lượng chất lỏng |
|
4) Thìa thuỷ tinh |
|
d) Để chứa hoá chất |
|
5) Đũa thuỷ tinh |
|
e) Để lấy hoá chất rắn |
Phần I. Trắc nghiệm (4 điểm)
Hãy khoanh tròn chữ cái đứng trước câu trả lời mà em cho là đúng nhất. Mỗi câu trả lời đúng được 0,25 điểm.