A. NH2.
B. N2H4.
 Giải bởi Vietjack
Giải bởi Vietjack
Đáp án D
Amoniac có công thức hóa học là NH3.
Khi thực hiện phản ứng giữa dung dịch HNO3 đặc với kim loại sinh ra khí NO2 độc hại. Để hạn chế khí NO2 thoát ra gây ô nhiễm môi trường, ta phải đậy ống nghiệm bằng bông tẩm
Viết phương trình hóa học?
a) Viết phương trình hóa học dưới dạng phân tử và ion rút gọn của phản ứng xảy ra sau: (0,5đ)
CaCO3 + HCl
b) Viết phương trình nhiệt phân các muối trong các trường hợp sau: (1,5đ)
NH4NO3; NaNO3, MgCO3.
Một loại nước thải công nghiệp có pH = 9. Nước thải đó có môi trường
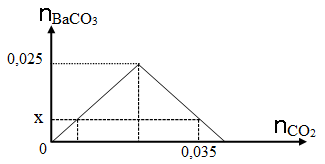
Dẫn từ từ CO2 vào dung dịch chỉ chứa 0,025 mol Ba(OH)2. Đồ thị dưới đây biểu diễn sự phụ thuộc của số mol kết tủa BaCO3 tạo thành theo số mol CO2.
Hợp chất hữu cơ X (C, H, O và N) có công thức trùng với công thức đơn giản nhất, đốt cháy hoàn toàn 7,5 gam X, thu được 4,48 lít CO2; 1,12 lít N2 (các khí đều đo (đktc)) và 4,5 gam H2O. Số nguyên tử hiđro trong một phân tử X là
Dung dịch X gồm 0,05 mol K+, 0,04 mol , 0,03 mol Cl- và . Cô cạn dung dịch X, thu được m gam chất rắn khan. Giá trị của m là:
Hợp chất X có công thức đơn giản nhất là CH2O. Tỉ khối hơi của X so với hiđro bằng 30. Công thức phân tử của X là
Đốt cháy hoàn toàn 4,4 gam hợp chất hữu cơ X (C, H, O). Dẫn sản phẩm cháy lần lượt qua bình (1) đựng dung dịch H2SO4 đặc, bình (2) đựng dung dịch KOH dư. Sau thí nghiệm, khối lượng bình (1) tăng 1,8 gam, khối lượng bình (2) tăng 6,6 gam. Tỉ khối của X đối với hiđro là 44. Xác định công thức của phân tử X.
Phản ứng Ba(OH)2 + 2HCl → BaCl2 + 2H2O có phương trình ion thu gọn là:
Hòa tan hoàn toàn m gam Zn vào dung dịch HNO3 dư, thu được 0,448 ml khí NO (đktc, sản phẩm khử duy nhất). Tính giá trị của m.