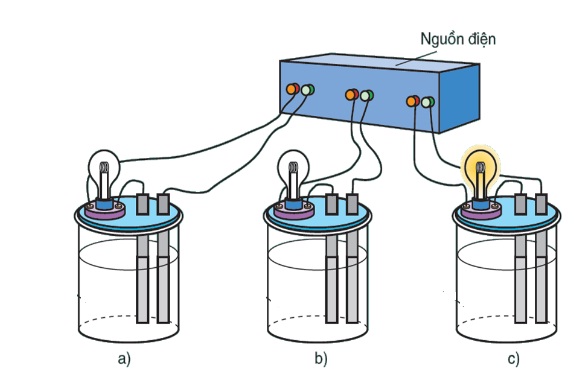
Trộn 500 ml dung dịch chứa hỗn hợp HNO3 0,08M và H2SO4 0,01M với 500 ml dung dịch KOH x M thu được 1 lít dung dịch có pH bằng 12. Giá trị của x là
A. 0,13M.
B. 0,12M.
C. 0,14M.
D. 0.10M.
 Giải bởi Vietjack
Giải bởi Vietjack
Đáp án đúng là: B
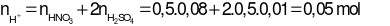
\({n_{O{H^ - }}} = {n_{KOH}} = 0,5x\,\,mol\)
pH = 12 >7 → OH-dư, H+ phản ứng hết
→ pOH = 14 – 12 = 2 → [OH-] = 10-2M
\(\begin{array}{l}{H^ + } + O{H^ - } \to {H_2}O\\0,05\,\,\,\,\,0,5x\end{array}\)
\( \to {n_{O{H^ - }(du)}} = 0,5x - 0,05\,\,mol\)
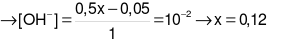
Nguyên tử nguyên tố X có tổng số electron ở các phân lớp p là 10. Nguyên tố X là
Ở trạng thái cơ bản, cấu hình electron của nguyên tử Na (Z = 11) là
Hợp chất nào sau đây ở dạng tinh thể, dễ tan trong nước và có nhiệt độ nóng chảy cao?
Thực hiện thí nghiệm như hình vẽ mô phỏng dưới đây. Em hãy cho biết, chất lỏng trong bình (c) có thể là chất nào sau đây?