B.S + 3F2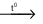 SF6
SF6
A.4S + 6NaOH(đặc)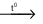 2Na2S + Na2S2O3+ 3H2O
2Na2S + Na2S2O3+ 3H2O
C.S + Hg → HgS
D.S + 6HNO3 (đặc) 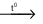 H2SO4+ 6NO2+ 2H2O
H2SO4+ 6NO2+ 2H2O
 Giải bởi Vietjack
Giải bởi Vietjack
Đáp án đúng là: A
- Xác định số oxi hoá của S trong từng phản ứng.
Dễ thấy đáp án B và D, S từ 0 lên +6 ⇒ Thể hiện tính khử.
Đáp án C, S từ 0 xuống – 2 ⇒Thể hiện tính oxi hoá.
Đáp án A, S từ 0 lên +2 và từ 0 xuống – 2 ⇒ S vừa là chất khử, vừa là chất oxi hoá.