Tính lượng nhiệt sinh ra khi đốt cháy hoàn toàn 7,8 gam C6H6 (l)
Cho enthalpy tạo thành chuẩn của các chất tương ứng là
|
Chất |
C6H6 (l) |
CO2 (g) |
H2O (g) |
|
|
+49 |
− 393,5 |
-241,82 |
A. 3135,46 kJ;
B. 684,32 kJ;
C. 313,546 kJ;
D. 68,432 kJ.
 Giải bởi Vietjack
Giải bởi Vietjack
Đáp án đúng là: C
C6H6 (l) +  O2 (g) ⟶ 6CO2 (g) + 3H2O (g)
O2 (g) ⟶ 6CO2 (g) + 3H2O (g)
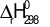 =
= 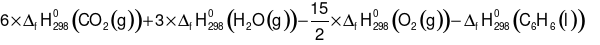
= 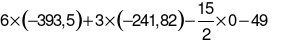
= − 3135,46 (kJ)
Do đó, đốt cháy 1 mol C6H6 thì lượng nhiệt sinh ra là 3135,46 kJ
7,8 gam C6H6 (l) có số mol là:  = 0,1 (mol).
= 0,1 (mol).
Vậy đốt cháy 0,1 mol C6H6 thì lượng nhiệt sinh ra là 3135,46.0,1 = 313,546 (kJ)
Tính biến thiên enthalpy chuẩn của phản ứng nhiệt nhôm và cho biết đây là phản ứng tỏa nhiệt hay thu nhiệt.
2Al (s) + Fe2O3 (s)  2Fe (s) + Al2O3 (s)
2Fe (s) + Al2O3 (s)
Biết  của Fe2O3 (s) và Al2O3 (s) lần lượt là -825,5 kJ/mol; -1676 kJ/mol
của Fe2O3 (s) và Al2O3 (s) lần lượt là -825,5 kJ/mol; -1676 kJ/mol
Cho phản ứng:
4HCl (g) + O2 (g)  2Cl2 (g) + 2 H2O (g)
2Cl2 (g) + 2 H2O (g)
Biến thiên enthalpy chuẩn của phản ứng trên tính theo năng lượng liên kết là bao nhiêu? Phản ứng tỏa nhiệt hay thu nhiệt?
Cho phản ứng có dạng: aA (g) + bB (g) ⟶ mM (g) + nN (g)
Công thức tính biến thiên enthalpy phản ứng theo năng lượng liên kết Eb là
Tính 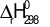 của phản ứng đốt cháy 1 mol C2H2 (g) biết các sản phẩm thu được đều ở thể khí.
của phản ứng đốt cháy 1 mol C2H2 (g) biết các sản phẩm thu được đều ở thể khí.
Cho enthalpy tạo thành chuẩn của các chất tương ứng là
|
Chất |
C2H2 (g) |
CO2 (g) |
H2O (g) |
|
|
+ 227 |
− 393,5 |
− 241,82 |
Cho phương trình nhiệt hóa học sau:
SO2 (g) +  O2 (g)
O2 (g) 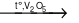 SO3 (g)
SO3 (g) 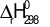 = − 98,5 kJ
= − 98,5 kJ
Lượng nhiệt giải phóng ra khi chuyển 76,8 gam SO2 (g) thành SO3 (g) là
Cho phản ứng:
3O2 (g)⟶2O3 (g) (1)
2O3 (g) ⟶ 3O2 (g) (2)
Biết phân tử O3 gồm 1 liên kết đôi O = O và 1 liên kết đơn O – O.
So sánh 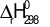 của hai phản ứng là
của hai phản ứng là
Tính 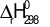 của phản ứng đốt cháy 21 gam CO (g) biết các sản phẩm thu được đều ở thể khí.
của phản ứng đốt cháy 21 gam CO (g) biết các sản phẩm thu được đều ở thể khí.
Cho enthalpy tạo thành chuẩn của các chất tương ứng là
|
Chất |
CO (g) |
CO2 (g) |
O2 (g) |
|
|
- 110,5 |
− 393,5 |
0 |
Cho phản ứng sau ở điều kiện chuẩn:
2H2 (g) + O2 (g)  2H2O (g)
2H2O (g)
Biến thiên enthalpy chuẩn của phản ứng trên tính theo năng lượng liên kết là
Cho phương trình nhiệt hóa học sau:
2H2 (g) + O2 (g) ⟶ 2H2O (g) 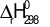 = − 483,64 kJ
= − 483,64 kJ
So sánh đúng là
Để tính biến thiên enthalpy phản ứng theo năng lượng liên kết, phải viết được
Cho phản ứng có dạng: aA + bB ⟶ mM + nN
Công thức tính biến thiên enthalpy phản ứng theo enthalpy tạo thành là
Sự phá vỡ liên kết cần ….. năng lượng, sự hình thành liên kết …... năng lượng.
Cụm từ tích hợp điền vào chỗ chấm trên lần lượt là
Cho phản ứng: NH3 (g) + HCl (g) ⟶ NH4Cl (s)
Biết 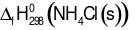 = − 314,4 kJ/mol;
= − 314,4 kJ/mol; 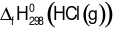 = − 92,31 kJ/mol;
= − 92,31 kJ/mol; 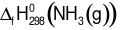 = − 45,9 kJ/mol.
= − 45,9 kJ/mol.
Biến thiên enthalpy chuẩn của phản ứng tính là