Nitrogen dioxide \(\left( {{\rm{N}}{{\rm{O}}_2}} \right)\) và dinitrogen tetroxide \(\left( {{{\rm{N}}_2}{{\rm{O}}_4}} \right)\) cùng tồn tại ở trạng thái cân bằng theo phương trình sau:
Một ống tiêm chứa hỗn hợp cân bằng của hai khí trên có màu nâu. Tiến hành kéo pít tông, giữ nguyên vị trí của pít tông rồi để yên ống tiêm trong một khoảng thời gian (2-3 phút).
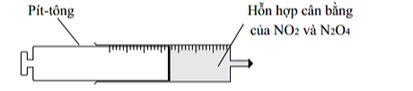
Hiện tượng quan sát được là
A. Hỗn hợp bị nhạt màu, sau đó sẽ có màu nâu đậm hơn so với ban đầu.
B. Hỗn hợp đậm màu hơn, sau đó sẽ có màu nâu nhạt hơn so với ban đầu.
C. Hỗn hợp có màu sắc không thay đổi.
 Giải bởi Vietjack
Giải bởi Vietjack
Ban đầu khi kéo pít tông thì thể tích của hỗn hợp phản ứng tăng, nồng độ các chất giảm, lượng chất có trong hệ sẽ bị loãng ra làm cho hỗn hợp có màu nâu nhạt hơn so với ban đầu. Sau một khoảng thời gian, vì kéo pít tông nên áp suất của hệ giảm, cân bằng sẽ chuyển dịch theo chiều tăng số mol chất khí.
\( \to \) Cân bằng chuyển dịch theo chiều nghịch (chiều tạo khí \({\rm{N}}{{\rm{O}}_2}\) màu nâu đỏ). Từ đó dẫn đến màu của hỗn hợp trở lên đậm hơn.
Chọn A.
Cho lăng trụ tam giác \[ABC.A'B'C'\], trên đường thẳng \[BA\] lấy điểm \[M\] sao cho \[A\] nằm giữa \[B\] và \[M\], \(MA = \frac{1}{2}AB,\,\,E\) là trung điểm \[AC.\] Gọi \(D = BC \cap \left( {MB'E} \right)\). Tỉ số \(\frac{{BD}}{{CD}}\) bằng
Đáp án: ……….Xác định một từ/ cụm từ SAI về mặt ngữ pháp/ hoặc ngữ nghĩa/ logic/ phong cách.
Ngôi chùa mang trong nó bao nhiêu sự tích, bao nhiêu huyền thoại và đã chứng minh bao biến thiên của kinh kì.
Gọi \[x,\,\,y,\,\,z\] là chiều dài, chiều rộng và chiều cao của một thùng giấy có dạng hình hộp chữ nhật không có nắp bên trên (hình vẽ). Biết rằng tổng diện tích xung quanh và đáy còn lại của thùng bằng 100 (đơn vị diện tích). Khi chiếc thùng có thể tích lớn nhất thì tổng \({x^2} + {y^2} + {z^2}\) bằng
Đáp án: ……….
Tìm \[a\] để hàm số \(f\left( x \right) = \left\{ {\begin{array}{*{20}{l}}{\frac{{\sqrt {4x + 1} - 1}}{{a{x^2} + \left( {2a + 1} \right)x}}{\rm{ khi }}x \ne 0}\\{4\quad {\rm{ khi }}x = 0}\end{array}} \right.\) liên tục tại \(x = 0\).
Đáp án: ……….