a. Viết phương trình phản ứng
b. Thành phần % khối lượng của Fe và Cu trong hỗn hợp.
 Giải bởi Vietjack
Giải bởi Vietjack
a. Phương trình hóa học:
2Fe + 6H2SO4Fe2(SO4)3+ 3SO2+ 6H2O
Cu + 2H2SO4CuSO4+ SO2+ 2H2O
b. 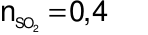 (mol).
(mol).
Gọi số mol của Fe và Cu trong hỗn hợp X lần lượt là x, y (mol).
56x + 64y = 19,2 (1)
Bảo toàn e: 3nFe+ 2nCu= 2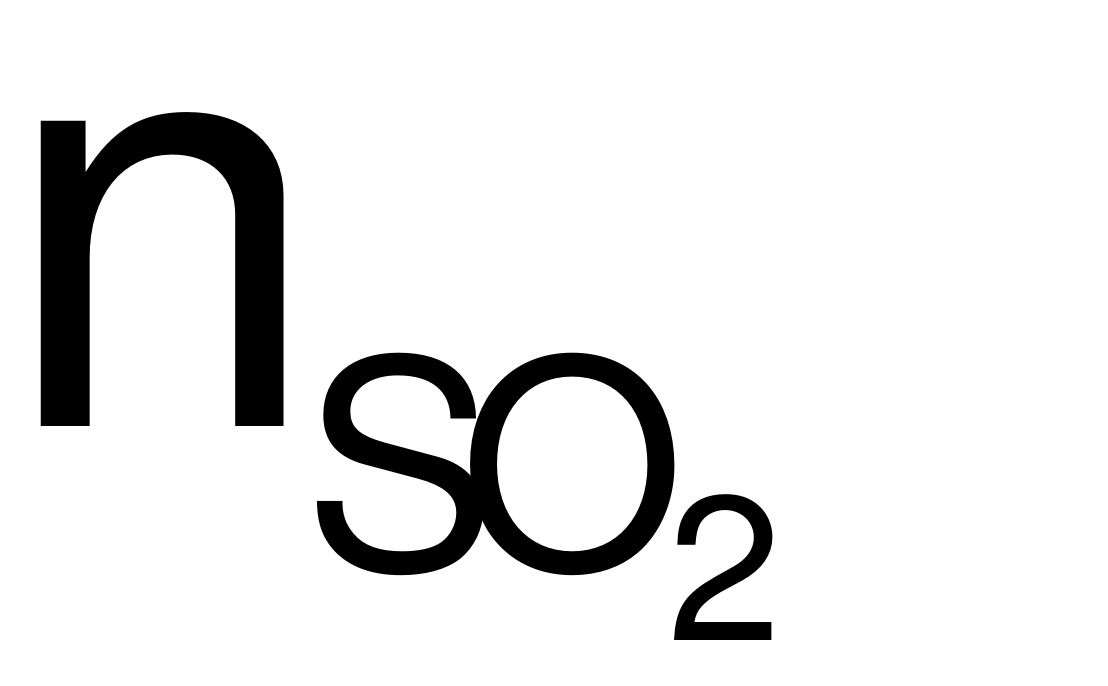
3x + 2y = 0,8 (2)
Từ (1) và (2), suy ra: x = 0,16; y = 0,16.
%mFe= 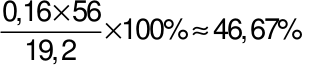 ;
;
%mCu= 100% - 46,67% = 53,33%.
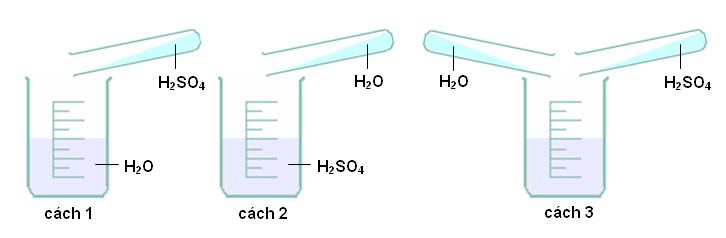
Để đảm bảo an toàn thí nghiệm nên làm theo