Xác định hệ số cân bằng của HCl trong phản ứng dưới đây:
K2Cr2O7 + HCl ⟶ Cl2 + KCl + CrCl3 + H2O
A. 5;
B. 10;
C. 14;
D. 16.
 Giải bởi Vietjack
Giải bởi Vietjack
Đáp án đúng là: C
Sự thay đổi số oxi hóa của các nguyên tố:
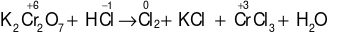
Quá trình oxi hóa và quá trình khử:


Áp dụng nguyên tắc: tổng số electron nhường bằng tổng số electron nhận
|
|
|
|
|
|
⇒ K2Cr2O7 + 14HCl ⟶3Cl2 + 2KCl + 2CrCl3 + 7H2O.
Cho nguyên tố X có số oxi hóa có giá trị là -2. Cách biểu diễn đúng là
Cho phản ứng: 3Cu + 8H+ + 2NO3−⟶3Cu2+ + 2NO + 4H2O
Quá trình khử là
Số oxi hóa của nguyên tử N trong các ion NH4+, NO3−, NO2− lần lượt là
Số oxi hóa của Mn trong các phân tử MnO2, KMnO4, K2MnO4 lần lượt là