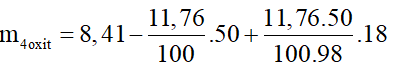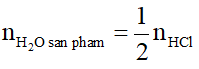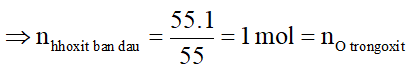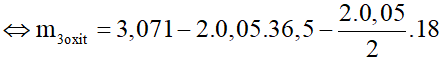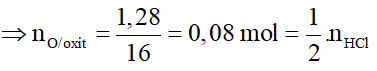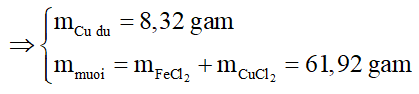Trắc nghiệm Hóa học 9 Bài tập oxit bazơ tác dụng với axit chọn lọc, có đáp án
Trắc nghiệm Hóa học 9 Bài tập oxit bazơ tác dụng với axit chọn lọc, có đáp án
-
1419 lượt thi
-
10 câu hỏi
-
10 phút
Danh sách câu hỏi
Câu 1:
Cho 2,8g hỗn hợp CuO, MgO, tác dụng vừa đủ với 50 ml dd 1M. Cô cạn dung dịch sau phản ứng thu được m gam muối khan. Giá trị của m là:
 Xem đáp án
Xem đáp án
Theo định luật bảo toàn khối lượng ta có:
Mà san pham = = 1.0,05 = 0,05 mol
⇒ = 2,8 + 0,05.98 - 0,05.18 = 6,8g
⇒ Chọn C.
Câu 2:
Cho x gam hỗn hợp gồm MgO, , ZnO, CuO tác dụng vừa đủ với 50g dd 11,76%. Cô cạn dd sau phản ứng thu được 8,41 g muối khan. Giá trị của m là:
 Xem đáp án
Xem đáp án
Tương tự bài 1, ta có:
= 3,61g
⇒ Chọn C.
Câu 3:
Hòa tan hoàn toàn 3,61g hỗn hợp gồm ZnO, CuO, MgO và cần 150 ml dd 0,4M. Cô cạn dd sau phản ứng thu được lượng muối sunfat là:
 Xem đáp án
Xem đáp án
Tương tự bài 1, ta có:
⇔ = 3,61+0,4.0,15.98-0,4.0,15.18
⇔ = 8,41g
⇒ Chọn A.
Câu 4:
Cho 5g hỗn hợp bột oxit kim loại gồm ZnO, FeO, , MgO tác dụng vừa hết với 200ml dd HCl 0,4M thu được dd X. Lượng muối trong dd X là:
 Xem đáp án
Xem đáp án
Ta có:
Tương tự bài 1, ta có:
⇔ = 7,2g
⇒ Chọn C.
Câu 5:
Oxy hóa hoàn toàn a(g) hỗn hợp X (gồm Zn, Pb, Ni) được b(g) hỗn hợp 3 oxit Y (ZnO, PbO, NiO). Hòa tan b(g) Y trên trong dung dịch HCl loãng thu được dung dịch Z. Cô cạn Z được hỗn hợp muối khan có khối lượng (b + 55) gam. Khối lượng a(g) của hỗn hợp X ban đầu là:
 Xem đáp án
Xem đáp án
Áp dụng tăng giảm khối lượng, ta thấy 1 nguyên tử O được thay thế bởi 2 nguyên tử Cl.
ZnO, PbO, NiO →
⇒ Từ 1 mol oxit ban đầu khối lượng muối sau phản ứng tăng là:
m↑= = 2.35,5 - 16 = 55g
Theo bài ra, ta có:
m↑ = = (b +55) - b = 55g
⇒mX = =b-16 = a
⇒ Chọn A.
Câu 6:
Cho m gam hỗn hợp các oxit CuO, , ZnO tác dụng vừa đủ với 50 ml dd HCl 2M. Cô cạn dung dịch sau phản ứng thu được 3,071 g muối clorua. Giá trị của m là:
 Xem đáp án
Xem đáp án
Tương tự bài 1 và bài 4, ta có:
⇔
⇔= 0,321g
⇒ Chọn D.
Câu 7:
Oxi hoá 13,6 gam hỗn hợp 2 kim loại thu được m gam hỗn hợp 2 oxit . Để hoà tan hoàn toàn m gam oxit này cần 500ml dd 1M . Tính m:
 Xem đáp án
Xem đáp án
Ta có:
Theo định luật bảo toàn khối lượng, ta có:
=13,6 + 0,5.16 = 21,6g
⇒ Chọn B.
Câu 8:
Đốt cháy hết 2,86 gam hỗn hợp kim loại gồm Al, Fe, Cu được 4,14 gam hỗn hợp 3 oxit. Để hoà tan hết hỗn hợp oxit này, phải dùng đúng 0,4 lít dung dịch HCl và thu được dung dịch X. Cô cạn dung dich X thì khối lượng muối khan là bao nhêu ?
 Xem đáp án
Xem đáp án
Theo định luật bảo toàn khối lượng, ta có:
⇔
=44-2,86 = 1,28g
⇒ == 0,08.2 = 0,16 mol
Áp dụng định luật bảo toàn khối lượng, ta có khối lượng của muối khan thu được là:
= 2,86 + 0,16.35,5 = 8,54g
⇒ Chọn C.
Câu 9:
Cho 24,12gam hỗn hợp X gồm CuO, , Al2O3 tác dụng vừa đủ với 350ml dd 4M rồi đun đến khan dung dịch sau phản ứng thì thu được m gam hỗn hợp muối khan. Tính m:
 Xem đáp án
Xem đáp án
Đáp án D
Câu 10:
Hòa tan m gam hỗn hợp gồm Cu và trong dung dịch HCl dư sau phản ứng còn lại 8,32gam chất rắn không tan và dung dịch X. Cô cạn dung dịch X thu được 61,92 gam chất rắn khan. Giá trị của m là:
 Xem đáp án
Xem đáp án
Ta thấy sau phản ứng còn Cu dư, chứng tỏ tác dụng với HCl tạo 2 muối và , sau đó tác dụng hết với Cu tạo và .
PTHH:
x…………………....2x………x
2x……..x…………2x………..x
= (2x+x).127 + x.135 = 61,92g
⇒ x= 0,12 mol
⇒
= 0,12.232+ 0,12.64+ 8,32= 43,84g
⇒ Chọn C.