Trắc nghiệm chuyên đề Hóa 9 Chủ đề 8: Ôn tập và kiểm tra chuyên đề Hidrocacbon - Nhiên liệu có đáp án
Trắc nghiệm chuyên đề Hóa 9 Chủ đề 8: Ôn tập và kiểm tra chuyên đề Hidrocacbon - Nhiên liệu có đáp án (Đề 1)
-
1581 lượt thi
-
11 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
 Xem đáp án
Xem đáp án
Chọn đáp án B
dX/H2 = 22 => M = 2 x 22 = 44.
Gọi công thức phân tử chất hữu cơ X là: CxHy => 12x + y = 44
x, y nguyên, dương. Nghiệm thích hợp là C3H8.
Câu 2:
Cho công thức cấu tạo của các chất (I), (II), (III)
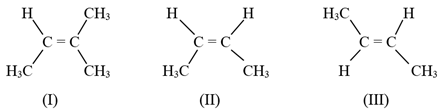
Các chất có cùng công thức phân tử là
 Xem đáp án
Xem đáp án
Chọn đáp án A
(II), (III) đều có công thức phân tử C4H8.
Câu 3:
 Xem đáp án
Xem đáp án
Chọn đáp án B
m = mC + mH = (3,36 x 12)/(22,4)+(4,5 x 2)/18 = 2,3 gam.
Câu 4:
 Xem đáp án
Xem đáp án
Chọn đáp án A
Khi tác dụng với nước (ẩm), khí HCl tạo ra dung dịch axit nên làm quỳ tím hóa đỏ.
Khí clo khi ẩm có tính tẩy màu, nên bằng cách nào đó người ta loại khí clo còn, chỉ kiểm tra sản phẩm phản ứng (khí HCl).
Câu 6:
 Xem đáp án
Xem đáp án
Chọn đáp án B
dX/H2 = 13 => M = 2 x 13 = 26
mC = (8,8 x 12)/44 = 2,4 gam; mH = (1,8 x 2)/( 18) = 0,2 gam
=> mO = 2,6 – (2,4 + 0,2) = 0
nC : nH = 2,4/12:0,2/1 = 1 : 1. Công thức đơn giản nhất: CH
Công thức phân tử (CH)n => M = (12+1)n = 26 => n=2
X là C2H2
Câu 7:
 Xem đáp án
Xem đáp án
Chọn đáp án D
2C2H2 + 5O2→ 4CO2 + 2H2O
nC2H2 = 2,6: 26 = 0,1 mol => nO2 = 0,25 mol
Thể tích không khí: 0,25 x 22,4 x 100/20 = 28 lít (đktc)
Câu 8:
Trong những hidrocacbon sau, những chất nào có phản ứng thế với brom?
CH3-CH3, CH3-CH=CH2, CH3-C≡CH, C6H6
 Xem đáp án
Xem đáp án
Chọn đáp án C
CH3 – CH3 tương tự CH4 có phản ứng thế với brom khi có ánh sáng và brom ở thể khí tương tự với khí clo.
Benzen (C6H6) khi có Fe làm xúc tác brom sẽ thế nguyên tử H của benzen tương tự như clo.
Câu 9:
 Xem đáp án
Xem đáp án
Etilen và axetilen có tính chất hóa học gần giống nhau:

Câu 10:
Tính thể tích khí C2H2 (đktc) tạo ra khi cho 10 gam CaC2 (có 36% tạp chất) tác dụng hết với H2O (cho C=12, Ca=14).
 Xem đáp án
Xem đáp án
CaC2 + 2H2O → Ca(OH)2 + C2H2
mCaC2 = (10 x (100-36))/(100 ) = 6,4 gam.
=> nCaC2 = 6,4 : 64 = 0,1 mol => nC2H2 = 0,1 mol
Thể tích khí C2H2 (đktc) tạo ra = 0,1 x 22,4 = 2,24 lít
Câu 11:
Một hỗn hợp gồm C2H2 và C2H4 có thể tích 5,6 lít khí (đktc) cho qua dung dịch Br2 dư, dung dịch này nặng thêm 6,8 g.
Tính thể tích mỗi khí trong hỗn hợp ban đầu (cho H=1, C=12).
 Xem đáp án
Xem đáp án
C2H2 + 2Br2 → C2H2Br4
C2H4 + Br2 → C2H2Br2
Gọi x, y lần lượt là số mol của C2H2 và C2H4 trong 5,6 lít hỗn hợp.
Ta có: x + y = 5,6/22,4 = 0,25
Dung dịch Br2 nặng thêm = khối lượng C2H2 + khối lượng C2H4 = 26x + 28y = 6,8
Giải ra ta có: x = 0,1 mol, y = 0,15 mol
Vậy: Thể tích C2H2 (đktc) = 0,1 x 22,4 = 2,24 lít
Thể tích C2H4 (đktc) = 0,15 x 22,4 = 3,36 lít
