Trắc nghiệm chuyên đề Hóa 9 Chủ đề 8: Ôn tập và kiểm tra chuyên đề Hidrocacbon - Nhiên liệu có đáp án
Trắc nghiệm chuyên đề Hóa 9 Chủ đề 8: Ôn tập và kiểm tra chuyên đề Hidrocacbon - Nhiên liệu có đáp án (Đề 3)
-
1585 lượt thi
-
11 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
 Xem đáp án
Xem đáp án
Chọn đáp án B
CH4 + 2O2 → CO2 + H2O
CO2 + Ca(OH)2 → CaCO3↓ + H2O
Câu 2:
 Xem đáp án
Xem đáp án
Chọn đáp án C
Công thức cấu tạo của etilen và axetilen: CH2 = CH2, CH≡CH.
Câu 3:
Một chất hữu cơ Z khi đốt phản ứng xảy ra theo phương trình:
aZ + 2O2 → CO2 + 2H2O
Công thức phân tử của Z là (a là số nguyên dương)
 Xem đáp án
Xem đáp án
Chọn đáp án D
Bảo toàn nguyên tố ở 2 vế của phương trình a = 1 => Z là CH4.
Câu 4:
Cho phương trình: C6H6 + Br2 → C6H5Br + HBr
Trong đó
 Xem đáp án
Xem đáp án
Chọn đáp án B
Phương trình:
C6H6(l) + Br2(l) Fe→ C6H5Br (l)+ HBr (khí không màu)
Câu 5:
 Xem đáp án
Xem đáp án
Chọn đáp án A
Phương trình phản ứng đốt cháy C2H4: C2H4 + 3O2 → 2CO2 + 2H2O
- Khi đốt với tỉ lệ thể tích O2 ít hơn 3 lần thể tích C2H4 thì C2H4 còn.
Sau đó khi tác dụng với dung dịch brom làm màu nâu dung dịch Br2 nhạt dần.
C2H4+ Br2 → C2H4Br2
- Khối lượng bình không đổi.
- Nhiệt độ trong bình tăng do phản ứng tỏa nhiệt.
- Khối lượng dung dịch brom không giảm đi.
Câu 6:
 Xem đáp án
Xem đáp án
Chọn đáp án C
Công thức chung của một hidrocacbon mạch hở, có một liên kết ba là CnH2n-2.
CnH2n-2 + 2Br2 → CnH2n-2Br4
nX = 0,4/2 = 0,2 mol => M = 5,2/0,2 = 26
Công thức phân tử của X: C2H2
Công thức cấu tạo thu gọn của X là: HC≡CH
Câu 7:
 Xem đáp án
Xem đáp án
Chọn đáp án B
Câu 8:
Một hỗn hợp gồm etilen và metan khi cho qua dung dịch brom dư thì dung dịch tăng 5,6 g đồng thời có 5,6 lít chất khí bay ra (đktc).
Thành phần % theo thể tích của etilen ban đầu là (cho H=1, C=12)
 Xem đáp án
Xem đáp án
Chọn đáp án D
Hỗn hợp atilen và metan khi cho qua dung dịch brom chỉ có etilen tác dụng theo phương trình: C2H4+ Br2→C2H4Br2
Khí bay ra là metan có thể tích 5,6 lít.
Khối lượng etilen = 5,6 gam hay netilen = 5,6/28 = 0,2 mol
Thể tích etilen = 0,2 x 22,4 = 4,48 lít (đktc)
Vậy thành phần % theo thể tích của etilen: 4,48/(4,48+5,6) x 100% = 44,44%.
Câu 9:
Mạch cacbon là gì? Có bao nhiêu loại mạch cacbon?
Mỗi mạch cacbon lấy 1 ví dụ.
 Xem đáp án
Xem đáp án
Mạch cacbon: Những nguyên tử cacbon trong phân tử chất hữu cơ có thể liên kết trực tiếp với nhau tạo thành mạch cacbon.
Ví dụ: - Mạch thẳng: CH3 – CH2 – CH2 – CH3
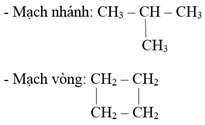
Câu 10:
Butan là một hidrocacbon có tính chất tương tự metan và có công thức phân tử là C4H10.
a) Viết công thức cấu tạo mạch thẳng của butan.
b) Viết phương trình phản ứng đốt cháy butan.
c) Viết phương trình phản ứng thế với clo.
 Xem đáp án
Xem đáp án
a) Công thức cấu tạo của butan: CH3 – CH2 – CH2 – CH3
b)Phương trình phản ứng đốt cháy butan:
C4H10 + 13/2 O2 → 4CO2 + 5H2O
c) Phương trình phản ứng thế với clo
C4H10 + Cl2 a/s→ C4H9Cl + HCl
Câu 11:
Đốt cháy hoàn toàn 3,2 g chất hữu cơ A sản phẩm CO2 và hơi H2O, tạo ra cho qua bình (1) đựng H2SO4 đặc, rồi qu bình (2) đựng dung dịch Ca(OH)2 dư. Độ tăng khối lượng (1) là 7,2 g, bình (2) thu được 20 g kết tủa.
a) Xác định thành phần % theo khối lượng các nguyên tố trong A.
b) Lập công thức phân tử chất A, biết tỉ khối hơi của A so với không khí là 0,5517. (Cho H=1, C=12, O=16, Ca=40, Mkhông khí = 29)
 Xem đáp án
Xem đáp án
a) Thành phần % khối lượng các nguyên tố:
Độ tăng khối lượng bình (1) bằng khối lượng H2O = 7,2 gam
=> mH =7,2/9 = 0,8 gam
Thành phần % khối lượng H = 0,8/32 x 100% = 25%
CO2 + Ca(OH)2 → CaCO3↓ + H2O
nCO2 = nCaCO3 = 20/100 = 0,2 mol
=> mC = 0,2 x 12 = 2,4 gam
Thành phần % khối lượng C = 2,4/3,2 x 100% = 75%
b) Công thức phân tử: Chất A chỉ có 2 nguyên tố C, H.
nC : nH = 0,2 : 0,8 = 1: 4
=> Công thức đơn giản nhất: CH4
Mặt khác khối lượng phân tử = 0,5517 x 29 ≈ 16
M = (12+4)n = 16 => n = 1
Vậy công thức phân tử cúa A: CH4.
