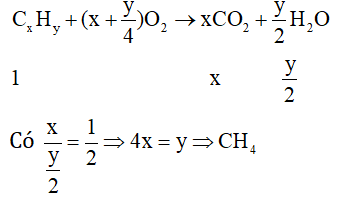Bài tập đốt cháy hiđrocacbon chọn lọc, có đáp án
-
964 lượt thi
-
10 câu hỏi
-
10 phút
Danh sách câu hỏi
Câu 1:
Đốt cháy hoàn toàn 1,68 g một hiđrocacbon X có M = 84 đvCho ta 5,28g . Số nguyên tử C trong phân tử X là:
 Xem đáp án
Xem đáp án
= 1,68/84 = 0,02 mol
= 5,28/44 = 0,12 mol
⇒ = 0,12 mol
Gọi x là số nguyên tử C trong phân tử X, ta có:
x = = 0,12/0,02 = 6 (nguyên tử C)
⇒ Chọn C.
Câu 2:
Đốt cháy hoàn toàn 0,1 mol rồi hấp thu hoàn toàn sản phẩm tạo ra vào 200ml dung dịch 1M thì thu được 19,7 gam kết tủa. Công thức của hiđrôcacbon là:
 Xem đáp án
Xem đáp án
Đốt cháy thu được và . Cho sản phẩm cháy vào : 0,2 mol thu được kết tủa là : 0,1 mol → xảy ra các trường hợp sau:
⇒ Chọn B
Câu 3:
Đốt cháy hoàn toàn hỗn hợp X gồm hidrocacbon Y và khí CO thu được số mol bằng số mol nước. Y là:
 Xem đáp án
Xem đáp án
Gọi số mol của và CO lần lượt là a và b.
Theo định luật bảo toàn nguyên tố ta có:
Đốt cháy và CO thu được số mol bằng số mol
Vậy khi đốt cháy hiđrocacbon có
Vậy hợp chất hidrocacbon là ankan, suy ra CTTQ là .
⇒ Chọn A.
Câu 4:
Đốt một hidrocacbon bằng oxi (lấy dư). Sản phẩm thu được sau khi cho ngưng tụ còn trong đó là oxi. Các thể tích đều đo ở đktc. Xác định công thức phân tử của hidrocacbon.
 Xem đáp án
Xem đáp án
= 65-25 = 40 cm3
= 80.2-40.2-25.2 =
Gọi hidrocacbon là , ta có:
x = /10 = 40/10 = 4
y = /10 = 2.30/10 = 6
Vậy Hidrocacbon có CT là
. ⇒ Chọn B.
Câu 5:
Đốt cháy một hiđrocacbon X mạch hở, khí với 1,92 gam khí oxi trong bình kín rồi cho các sản phẩm sau phản ứng qua bình 1 chứa trong đặc dư, bình 2 chứa 3,5 lít 0,01M thu được 3g kết tủa, khí duy nhất bay ra có thể tích 0,224 lit đo ở và 1,1 atm. Xác định công thức phân tử của X, giả thiết các phản ứng xảy ra hoàn toàn.
 Xem đáp án
Xem đáp án
Khí bay ra sau khi đi qua bình 1 và bình 2 chính là dư.
Theo bài ra: số mol (= 0,035 mol) > số mol kết tủa(= 0,03 mol) nên ở bình 2 xảy ra các trường hợp sau:
⇒ Chọn C.
Câu 6:
Đốt cháy hoàn toàn hiđrocacbon X thu được số mol bằng một nửa số mol . X có CTPT là
 Xem đáp án
Xem đáp án
⇒ Chọn A.
Câu 7:
Trộn 200 hỗn hợp chất hữu cơ X với 900 oxi dư rồi đốt. Thể tích hỗn hợp sau khi đốt là 1,2 lit. Sau khi làm ngưng tụ hơi nước còn lại 0,8 lit, tiếp tục cho đi qua dung dịch NaOH dư thì còn lại 0,4 lit (các thể tích ở cùng điều kiện). Công thức phân tử của X là:
 Xem đáp án
Xem đáp án
Ở cùng điều kiện nhiệt độ và áp suất thì tỉ lệ về thể tích cũng chính là tỉ lệ về số mol
⇒ Chọn B.
Câu 8:
Đốt cháy hoàn toàn a gam hỗn hợp X gồm và và thu được 26,4 gam và 16,2 gam . Hỏi a có giá trị là bao nhiêu
 Xem đáp án
Xem đáp án
Ta biết hỗn hợp X chỉ gồm các hidrocacbon có nguyên tố C và H.
Quy đổi hỗn hợp X gồm C và H.
Khi đó ta có:
= 26,4/44 = 0,6 mol
⇒ = 0,6 mol
⇒ = 0,6.12 = 7,2g
= 16,2/18 = 0,9 mol
⇒ = 0,9.2 = 1,8 mol
⇒ = 1,8g
⇒ = 7,2+1,8 = 9g
⇒ Chọn D.
Câu 9:
Đốt cháy hoàn toàn hỗn hợp 2 hidrocacbon cùng thuộc dãy đồng đẳng thu được 7,84 lít (đktc) và 11,7 gam . Hai hidrocacbon đó thuộc dãy đồng đẳng nào sau đây :
 Xem đáp án
Xem đáp án
= 7,84/22,4 = 0,35 mol
= 11,7/18 = 0,65 mol
⇒ < ⇒ ankan
⇒ Chọn B.
Câu 10:
Đốt cháy hoàn toàn 5,6 lít hỗn hợp hai ankan ( đktc) thu được 8,1 gam . Dẫn hết sản phẩm vào dd dư thì thu được kết tủa là :
 Xem đáp án
Xem đáp án
= 5,6/22,4 = 0,25 mol
= 8,1/18 = 0,45 mol
Vì ankan có CTTQ là nên ta có:
⇒ = 0,45 - 0,25 = 0,2 mol
Vì tác dụng với dư nên tạo kết tủa hoàn toàn.
⇒ n↓ = = 0,2 mol
⇒ m↓ = 0,2.100 = 20g
⇒ Chọn C.