ĐGNL ĐHQG TP.HCM - Vấn đề thuộc lĩnh vực hóa học - Bài tập về sự điện phân
-
597 lượt thi
-
31 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
Điện phân 200 ml dung dịch CuSO4 với I = 1,93 A tới khi catot bắt đầu có bọt khí thoát ra thì dừng lại, cần thời gian là 250 giây. Thể tích khí thu được ở anot (đktc) là
 Xem đáp án
Xem đáp án
Trả lời:
ne trao đổi = I.t / F = 0,005 mol
Ở catot: Cu2+ + 2e → Cu
Ở anot: 2H2O → 4H+ + O2 + 4e
Ở catot bắt đầu có bọt khí thoát ra =>Cu2+ điện phân vừa hết
=>nO2 thu được ở anot = 0,005 / 4 = 0,00125 mol
=>V = 0,028 lít = 28 ml
Đáp án cần chọn là: A
Câu 2:
Điện phân l00 ml dung dịch CuSO4 0,2M với cường độ dòng điện I = 9,65A. Khối lượng Cu bám trên catot khi thời gian điện phân t1 = 200s và t2 = 500s (hiệu suất điện phân là 100%) lần lượt là
 Xem đáp án
Xem đáp án
Trả lời:
nCuSO4 = 0,02 mol =>ne Cu2+ nhận tối đa = 0,02.2 = 0,04 mol
Khi t1 = 200s =>ne trao đổi = I.t / F = 0,02 mol
=>nCu tạo ra = ne trao đổi / 2 = 0,01 mol =>mCu (1) = 0,64 gam
Khi t2 = 500s =>ne trao đổi = I.t / F = 0,05 >0,04
=>nCu = nCuSO4 = 0,02 mol =>mCu (2) = 1,28 gam
Đáp án cần chọn là: C
Câu 3:
Điện phân một lượng dư dung dịch KCl với điện cực trơ, màng ngăn xốp thời gian 16,1 phút dòng điện I = 5A thu được 500 ml dung dịch X. pH của dung dịch X có giá trị là
 Xem đáp án
Xem đáp án
Trả lời:
ne trao đổi = I.t / F = 0,05 mol
Ở cực (-) điện phân H2O: 2H2O + 2e → H2 + 2OH-
=>nOH- = ne = 0,05 mol =>[OH-] = 0,05 / 0,5 = 0,1 M
=>pOH = 1 =>pH = 13
Đáp án cần chọn là: C
Câu 4:
 Xem đáp án
Xem đáp án
Trả lời:
Catot: M2+ + 2e → M
Anot: 2H2O → O2 ↑ + 4H+ + 4e
0,18 → 0,09 → 0,36
=>ne trao đổi = 4.nO2 = 0,36 mol
Mà ne = I.t / F =>I = ne.F / t = 12A
nM = ne trao đổi / 2 = 0,18 mol =>M = 11,52 / 0,18 = 64
=>M là Cu
Đáp án cần chọn là: D
Câu 5:
Điện phân 500 ml dung dịch AgNO3 với điện cực trơ cho đến khi catot bắt đầu có khí thoát ra thì ngừng điện phân. Để trung hòa dung dịch sau điện phân cần 800 ml dung dịch NaOH 1M. Biết I = 20 A, nồng độ mol AgNƠ3 và thời gian điện phân lần lượt là
 Xem đáp án
Xem đáp án
Trả lời:
Đến khi catot bắt đầu có khí thoát ra =>Ag+ bị điện phân vừa hết
nNaOH = 0,8 mol =>nH+ = 0,8 mol
Catot: Ag+ + 1e → Ag
Anot: 2H2O → O2 ↑ + 4H+ + 4e
=>ne trao đổi = nH+ = 0,8 mol
=>nAg+ = 0,8 mol =>CM AgNO3 = 0,8 / 0,5 = 1,6M
n = I.t / F =>t = n.F / I = 3860s
Đáp án cần chọn là: B
Câu 6:
Điện phân dung dịch CuSO4 với điện cực trơ, cường độ dòng điện 10A. Khi ở anot có 4 gam khí oxi bay ra thì ngưng. Phát biểu nào sau đây là đúng ?
 Xem đáp án
Xem đáp án
Trả lời:
nO2 = 0,125 mol
Catot: Cu2+ + 2e → Cu
Anot: 2H2O → O2 ↑ + 4H+ + 4e
=>ne trao đổi = 4.nO2 = 0,5 mol
=>nCu = 0,5 / 2 = 0,25 mol =>m = 16 gam =>A đúng
t = n.F / I = 4825s =>B sai
+) pH của dung dịch ban đầu giảm, khi hết Cu2+ thì nước điện phân ở catot tạo OH-, ở anot tạo ra H+ và nOH- = nH+ nên pH không đổi
+) hết Cu2+, nước điện phân ở catot tạo khí H2
Đáp án cần chọn là: A
Câu 7:
 Xem đáp án
Xem đáp án
Trả lời:
Catot (-) Cu2+, Na+, H2O Anot (+) SO42- , Cl-, H2O
(1) Cu2+ + 2e → Cu (1) 2Cl- → Cl2 + 2e
a → 2a → a b → b/2 → b
Vì catot chưa có khí thoát ra và b>2a
=> Dung dịch sau điện phân chứa: Na+, SO42-, Cu2+, Cl-.
Đáp án cần chọn là: D
Câu 8:
 Xem đáp án
Xem đáp án
Trả lời:
(1) 2NaCl + CuSO4 → Cu +Cl2 + Na2SO4
Ở (1) NaCl phản ứng vừa đủ với CuSO4 =>Dung dịch sau điện phân chỉ có Na2SO4
Đáp án cần chọn là: C
Câu 9:
Điện phân dung dịch hồn hợp chứa 0,04 mol AgNO3 và 0,05 mol Cu(NO3)2, điện cực trơ, dòng điện 5A, trong 32 phút 10 giây. Khối lượng kim loại bám vào catot là
 Xem đáp án
Xem đáp án
Trả lời:
\[{n_{{e_{td}}}} = \frac{{5.1930}}{{96500}} = 0,1mol\]
Catot gồm Ag+ và Cu2+ bị oxi hóa
Ag+ + 1e → Ag
0,04 0,04
Cu2+ + 2e → Cu
0,06 →0,03
\[ \Rightarrow \left\{ {\begin{array}{*{20}{c}}{{n_{Ag}} = 0,04mol}\\{{n_{Cu}} = \frac{{0,1 - 0,04}}{2} = 0,03mol}\end{array}} \right.\]
=>mKL= 0,04.108 + 0,03.64 = 6,24g
Đáp án cần chọn là: A
Câu 10:
Điện phân dung dịch X gồm 0,04 mol AgNO3 và 0,06 mol Fe(NO3)3 với I = 5,36A, điện cực trơ, sau t giây thấy catot tăng 5,44 gam. Giá trị của t là
 Xem đáp án
Xem đáp án
Trả lời:
mAg = 4,32g =>mFe(bị điện phân) = 5,44 – 4,32 = 1,12g =>nFe = 0,02 mol
Ag+ + 1e → Ag
0,04 0,04
Fe3++ 1e → Fe2+
0,06 0,06
Fe2+ + 2e → Fe
0,04 0,02
=>netđ= 0,04 + 0,1 = 0,14 mol
Mà
\[{n_{{e_{td}}}} = \frac{{It}}{F} = 0,1mol\]
\[ \to t = \frac{{F.{n_{{e_{td}}}}}}{I}\]
\[ \Rightarrow t = \frac{{96500.0,14}}{{5,36}} = 2520,522s\]
Đáp án cần chọn là: A
Câu 11:
Điện phân 500 ml dung dịch hỗn họp FeSO4 0,1M, Fe2(SO4)3 0,2M và CuSO4 0,1M với điện cực trơ. Điện phân cho đến khi khối lượng catot tăng 8,8 gam thì ngừng điện phân. Biết cường độ dòng điện đem điện phân là 10A. Thời gian điện phân là:
 Xem đáp án
Xem đáp án
Trả lời:
nFe3+ = 0,2 mol ; nCu2+ = 0,05mol ; nFe2+ =0,05mol
mtăng = mCu + mFe =>mFe = 8,8 – 0,05.64 = 5,6g =>nFe = 0,1mol
Các ion đã điện phân ở catot: Fe3+ , Cu2+, Fe2+ điện phân 1 phần
netđ = nFe3+ + 2nCu2+ + 2nFe2+ = 0,2 + 0,05.2 + 0,1.2 = 0,5 mol
\[ \to t = \frac{{F.{n_{{e_{td}}}}}}{I}\]
\[ \Rightarrow t = \frac{{96500.0,5}}{{10}} = 4825s\]
Đáp án cần chọn là: C
Câu 12:
Điện phân 400ml dd AgNO3 0,2M và Cu(NO3)2 0,1M với cường độ dòng điện
I = 10A, anot bằng Pt. Sau thời gian t, ta ngắt dòng điện, thấy khối lượng catot tăng thêm m gam trong đó có 1,28 gam Cu. Thời gian điện phân t là (hiệu suất điện phân là 100%)
 Xem đáp án
Xem đáp án
Trả lời:
Sinh ra 1,28 g Cu tương đương 0,02 mol Cu mà nCu(NO3)2 = 0,04 >0,02
→ Cu(NO3)2 bị điện phân 1 phần → AgNO3 điện phân hết
nAgNO3 = 0,08mol
Ag+ + 1e → Ag
0,08 → 0,08
Cu2+ + 2e → Cu
0,04 0,02
=>netđ= 0,04 + 0,08 = 0,12 mol
\[ \to t = \frac{{F.{n_{{e_{td}}}}}}{I}\]
\[ \Rightarrow t = \frac{{96500.0,12}}{{10}} = 1158s\]
Đáp án cần chọn là: B
Câu 13:
Dung dịch X chứa HCl, CuSO4, Fe2(SO4)3. Lấy 400 ml dung dịch X đem điện phân với điện cực trơ, I = 7,72A đến khi ở catot thu được 5,12 gam Cu thì dừng lại. Khi đó chỉ thu được 0,1 mol một chất khí duy nhất thoát ra ở anot. Thời gian điện phân và nồng độ [Fe2+] sau điện phân lần lượt là
 Xem đáp án
Xem đáp án
Trả lời:
nCu = 0,08 (mol)
Catot:
Fe3+ + 1e → Fe2+
x x
Cu2+ + 2e → Cu
0,08 0,16 0,08
Anot: chỉ thu được 1 khí nên phải là Cl2
2Cl- - 2e → Cl2
0,2 0,1
Theo định luật bảo toàn e, ta có:
x + 0,16 = 0,2 =>x = 0,04 (mol)
=>[Fe2+] = 0,04/0,4 = 0,1 (M)
\[{n_{{e_{td}}}} = \frac{{It}}{F}\]
\[ \to t = \frac{{F.{n_{{e_{td}}}}}}{I}\]
\[ \Rightarrow t = \frac{{96500.0,2}}{{7,72}} = 2500s\]
Đáp án cần chọn là: B
Câu 14:
Sự điện phân là quá trình oxi hóa - khử xảy ra trên bề mặt các điện cực khi có dòng điện một chiều đi qua chất điện li nóng chảy hoặc dung dịch chất điện li nhằm thúc đẩy một phản ứng hóa học mà nếu không có dòng điện, phản ứng sẽ không tự xảy ra. Trong thiết bị điện phân:
- Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều.
+ Gốc axit có chứa oxi không bị điện phân (ví dụ: NO3-, SO42-, PO43-, CO32-, ClO4-, …).
Khi đó nước bị điện phân theo bán phản ứng: 2H2O → O2 + 4H+ + 4e
+ Thứ tự anion bị điện phân: S2- >I- >Br- >Cl- >RCOO- >OH- >H2O
- Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều.
+ Nếu dung dịch có chứa nhiều cation thì cation nào có tính oxi hóa mạnh hơn sẽ bị điện phân trước.
+ Một số cation không bị điện phân như K+, Na+, Ca2+, Ba2+, Mg2+, Al3+…
Khi đó nước bị điện phân theo bán phản ứng: 2H2O + 2e → H2 + 2OH-
Cho dãy điện hóa sau:
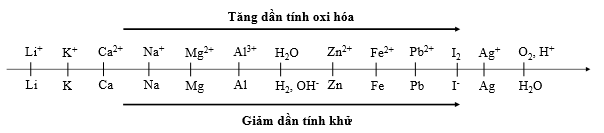
Thí nghiệm 1: Một sinh viên thực hiện quá trình điện phân dung dịch chứa đồng thời CuSO4, Fe2(SO4)3, HNO3, Al(NO3)3 bằng hệ điện phân sử dụng các điện cực than chì cho đến khi bắt đầu thấy xuất hiện khí ở catot thì dừng điện phân.
Thí nghiệm 2: Sinh viên đó tiếp tục điện phân dung dịch hỗn hợp chứa 0,04 mol AgNO3 và 0,05 mol Cu(NO3)2 với điện cực trơ, cường độ dòng điện 5A, trong 32 phút 10 giây. Sau khi dừng điện phân, sinh viên đó nhấc catot và đem rửa sach, sấy khô và đem cân thấy khối lượng catot tăng m gam so với ban đầu. Biết hiệu suất điện phân đạt 100%. (Cho NTK: Cu = 64 đvC; Ag = 108 đvC).
Trong Thí nghiệm 1, bán phản ứng nào xảy ra ở anot?
 Xem đáp án
Xem đáp án
Trả lời:
Tại anot, ion SO42- và NO3- không bị điện phân → xảy ra sự điện phân H2O
Vậy bán phản ứng xảy ra ở anot là: 2H2O → O2 + 4H+ + 4e.
Đáp án cần chọn là: B
Câu 15:
- Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều.
+ Gốc axit có chứa oxi không bị điện phân (ví dụ: NO3-, SO42-, PO43-, CO32-, ClO4-, …).
Khi đó nước bị điện phân theo bán phản ứng: 2H2O → O2 + 4H+ + 4e
+ Thứ tự anion bị điện phân: S2- >I- >Br- >Cl- >RCOO- >OH- >H2O
- Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều.
+ Nếu dung dịch có chứa nhiều cation thì cation nào có tính oxi hóa mạnh hơn sẽ bị điện phân trước.
+ Một số cation không bị điện phân như K+, Na+, Ca2+, Ba2+, Mg2+, Al3+…
Khi đó nước bị điện phân theo bán phản ứng: 2H2O + 2e → H2 + 2OH-
Cho dãy điện hóa sau:

Thí nghiệm 1: Một sinh viên thực hiện quá trình điện phân dung dịch chứa đồng thời CuSO4, Fe2(SO4)3, HNO3, Al(NO3)3 bằng hệ điện phân sử dụng các điện cực than chì cho đến khi bắt đầu thấy xuất hiện khí ở catot thì dừng điện phân.
Thí nghiệm 2: Sinh viên đó tiếp tục điện phân dung dịch hỗn hợp chứa 0,04 mol AgNO3 và 0,05 mol Cu(NO3)2 với điện cực trơ, cường độ dòng điện 5A, trong 32 phút 10 giây. Sau khi dừng điện phân, sinh viên đó nhấc catot và đem rửa sach, sấy khô và đem cân thấy khối lượng catot tăng m gam so với ban đầu. Biết hiệu suất điện phân đạt 100%. (Cho NTK: Cu = 64 đvC; Ag = 108 đvC).
Trong Thí nghiệm 1, kim loại bám vào catot sau khi dừng điện phân là
 Xem đáp án
Xem đáp án
Trả lời:
Khi điện phân dung dịch, tại catot thì cation nào có tính oxi hóa mạnh hơn sẽ bị điện phân trước.
Ta thấy tại catot ion Al3+ không bị điện phân nên không xét đến.
Dựa vào dãy điện hóa ta thấy tính oxi hóa: Fe3+ >Cu2+ >H+ >Fe2+
Vậy thứ tự điện phân tại catot là Fe3+, Cu2+, H+, Fe2+:
(1) Fe3+ + 1e → Fe2+
(2) Cu2+ + 2e → Cu
(3) 2H+ + 2e → H2
(4) Fe2+ + 2e → Fe
Theo đề bài, ta dừng điện phân khi bắt đầu xuất hiện khí thoát ra tại catot ⟹ bán phản ứng (2) vừa kết thúc
Các bán phản ứng đã diễn ra là:
(1) Fe3+ + 1e → Fe2+
(2) Cu2+ + 2e → Cu
Vậy sau khi dừng điện phân chỉ có kim loại Cu bám vào catot.
Đáp án cần chọn là: C
Câu 16:
- Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều.
+ Gốc axit có chứa oxi không bị điện phân (ví dụ: NO3-, SO42-, PO43-, CO32-, ClO4-, …).
Khi đó nước bị điện phân theo bán phản ứng: 2H2O → O2 + 4H+ + 4e
+ Thứ tự anion bị điện phân: S2- >I- >Br- >Cl- >RCOO- >OH- >H2O
- Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều.
+ Nếu dung dịch có chứa nhiều cation thì cation nào có tính oxi hóa mạnh hơn sẽ bị điện phân trước.
+ Một số cation không bị điện phân như K+, Na+, Ca2+, Ba2+, Mg2+, Al3+…
Khi đó nước bị điện phân theo bán phản ứng: 2H2O + 2e → H2 + 2OH-
Cho dãy điện hóa sau:

Thí nghiệm 1: Một sinh viên thực hiện quá trình điện phân dung dịch chứa đồng thời CuSO4, Fe2(SO4)3, HNO3, Al(NO3)3 bằng hệ điện phân sử dụng các điện cực than chì cho đến khi bắt đầu thấy xuất hiện khí ở catot thì dừng điện phân.
Thí nghiệm 2: Sinh viên đó tiếp tục điện phân dung dịch hỗn hợp chứa 0,04 mol AgNO3 và 0,05 mol Cu(NO3)2 với điện cực trơ, cường độ dòng điện 5A, trong 32 phút 10 giây. Sau khi dừng điện phân, sinh viên đó nhấc catot và đem rửa sach, sấy khô và đem cân thấy khối lượng catot tăng m gam so với ban đầu. Biết hiệu suất điện phân đạt 100%. (Cho NTK: Cu = 64 đvC; Ag = 108 đvC).
Trong Thí nghiệm 2, giá trị của m là
 Xem đáp án
Xem đáp án
Trả lời:
32 phút 10 giây = 1930 giây
Số mol electron trao đổi là:
\[{n_e} = \frac{{It}}{F} = \frac{{5.1930}}{{96500}} = 0,1\left( {mol} \right)\]
Thứ tự điện phân tại catot:
(1) Ag+ + 1e → Ag
0,04 → 0,04/0,06 → 0,04 (mol)
(2) Cu2+ + 2e → Cu
0,03/0,02 ← 0,06 → 0,03 (mol)
Vậy có 0,04 mol Ag và 0,03 mol Cu bám vào catot.
Khối lượng catot tăng là: m = 0,04.108 + 0,03.64 = 6,24 gam
Đáp án cần chọn là: D
Câu 17:
- Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều.
+ Gốc axit có chứa oxi không bị điện phân (ví dụ: NO3-, SO42-, PO43-, CO32-, ClO4-, …). Khi đó nước bị điện phân theo bán phản ứng: 2H2O → O2 + 4H+ + 4e
+ Thứ tự anion bị điện phân: S2- >I- >Br- >Cl- >RCOO- >OH- >H2O
- Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều.
+ Nếu dung dịch có chứa nhiều cation thì cation nào có tính oxi hóa mạnh hơn sẽ bị điện phân trước.
+ Một số cation không bị điện phân như K+,Na+, Ca2+, Ba2+, Mg2+, Al3+… Khi đó nước bị điện phân theo bán phản ứng: 2H2O + 2e → H2 + 2OH-
Cho dãy điện hóa sau:

Thí nghiệm 1: Một sinh viên thực hiện quá trình điện phân dung dịch chứa đồng thời AgNO3, Cu(NO3)2, Fe(NO3)3, Mg(NO3)2 bằng hệ điện phân sử dụng các điện cực than chì.
Thí nghiệm 2: Sinh viên đó tiếp tục điện phân dung dịch X gồm 0,04 mol AgNO3 và 0,06 mol Fe(NO3)3 với I = 5,36A, điện cực trơ. Sau thời gian t giây, sinh viên đó lấy catot rửa sạch và sấy khô thấy catot tăng 5,44 gam.
(Cho NTK: Fe = 56 đvC; Ag = 108 đvC).
Trong Thí nghiệm 1, bán phản ứng nào xảy ra ở anot?
 Xem đáp án
Xem đáp án
Trả lời:
Tại anot, ion NO3- không bị điện phân → xảy ra sự điện phân H2O
Vậy bán phản ứng xảy ra ở anot là: 2H2O → O2 + 4H+ + 4e
Đáp án cần chọn là: C
Câu 18:
- Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều.
+ Gốc axit có chứa oxi không bị điện phân (ví dụ: NO3-, SO42-, PO43-, CO32-, ClO4-, …). Khi đó nước bị điện phân theo bán phản ứng: 2H2O → O2 + 4H+ + 4e
+ Thứ tự anion bị điện phân: S2- >I- >Br- >Cl- >RCOO- >OH- >H2O
- Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều.
+ Nếu dung dịch có chứa nhiều cation thì cation nào có tính oxi hóa mạnh hơn sẽ bị điện phân trước.
+ Một số cation không bị điện phân như K+,Na+, Ca2+, Ba2+, Mg2+, Al3+… Khi đó nước bị điện phân theo bán phản ứng: 2H2O + 2e → H2 + 2OH-
Cho dãy điện hóa sau:

Thí nghiệm 1: Một sinh viên thực hiện quá trình điện phân dung dịch chứa đồng thời AgNO3, Cu(NO3)2, Fe(NO3)3, Mg(NO3)2 bằng hệ điện phân sử dụng các điện cực than chì.
Thí nghiệm 2: Sinh viên đó tiếp tục điện phân dung dịch X gồm 0,04 mol AgNO3 và 0,06 mol Fe(NO3)3 với I = 5,36A, điện cực trơ. Sau thời gian t giây, sinh viên đó lấy catot rửa sạch và sấy khô thấy catot tăng 5,44 gam.
(Cho NTK: Fe = 56 đvC; Ag = 108 đvC).
Trong Thí nghiệm 1, thứ tự kim loại sinh ra tại catot là
 Xem đáp án
Xem đáp án
Trả lời:
Khi điện phân dung dịch, tại catot thì cation nào có tính oxi hóa mạnh hơn sẽ bị điện phân trước.
Ta thấy tại catot ion Mg2+ không bị điện phân nên không xét đến.
Dựa vào dãy điện hóa ta thấy tính oxi hóa: Ag+ >Fe3+ >Cu2+ >Fe2+
Vậy thứ tự điện phân tại catot là Ag+, Fe3+, Cu2+, Fe2+.
Ag+ + 1e → Ag
Fe3+ + 1e → Fe2+
Cu2+ + 2e → Cu
Fe2+ + 2e → Fe
⟹ Thứ tự kim loại sinh ra tại catot là Ag, Cu, Fe.
Đáp án cần chọn là: D
Câu 19:
- Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều.
+ Gốc axit có chứa oxi không bị điện phân (ví dụ: NO3-, SO42-, PO43-, CO32-, ClO4-, …). Khi đó nước bị điện phân theo bán phản ứng: 2H2O → O2 + 4H+ + 4e
+ Thứ tự anion bị điện phân: S2- >I- >Br- >Cl- >RCOO- >OH- >H2O
- Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều.
+ Nếu dung dịch có chứa nhiều cation thì cation nào có tính oxi hóa mạnh hơn sẽ bị điện phân trước.
+ Một số cation không bị điện phân như K+,Na+, Ca2+, Ba2+, Mg2+, Al3+… Khi đó nước bị điện phân theo bán phản ứng: 2H2O + 2e → H2 + 2OH-
Cho dãy điện hóa sau:

Thí nghiệm 1: Một sinh viên thực hiện quá trình điện phân dung dịch chứa đồng thời AgNO3, Cu(NO3)2, Fe(NO3)3, Mg(NO3)2 bằng hệ điện phân sử dụng các điện cực than chì.
Thí nghiệm 2: Sinh viên đó tiếp tục điện phân dung dịch X gồm 0,04 mol AgNO3 và 0,06 mol Fe(NO3)3 với I = 5,36A, điện cực trơ. Sau thời gian t giây, sinh viên đó lấy catot rửa sạch và sấy khô thấy catot tăng 5,44 gam.
(Cho NTK: Fe = 56 đvC; Ag = 108 đvC).
Trong Thí nghiệm 2, giá trị của t là
 Xem đáp án
Xem đáp án
Trả lời:
Ta thấy:
\[{n_{Ag\,\max }} = {n_{AgN{O_3}}} = 0,04\left( {mol} \right)\]
\[ \to {m_{Ag\,\max }} = 0,04.108\]
=4,32(g)<5,44(g)
⟹ có Fe bám vào catot
⟹ Ag+ và Fe3+ đã bị điện phân hết, Fe2+ bị điện phân một phần.
Khối lượng Fe bám vào catot là:
\[{m_{Fe}} = 5,44 - 4,32 = 1,12\left( g \right)\]
\[ \to {n_{Fe}}\frac{{1,12}}{{56}} = 0,02\left( {mol} \right)\]
Tại catot (-):
Ag+ + 1e → Ag
0,04 → 0,04 → 0,04 (mol)
Fe3+ + 1e → Fe2+
0,06 → 0,06 → 0,06 (mol)
Fe2+ + 2e → Fe
0,04 ← 0,02 (mol)
→ Số mol e trao đổi là: ne = 0,04 + 0,06 + 0,04 = 0,14 mol
→ Thời gian điện phân là:
\[t = \frac{{n{}_e.F}}{I} = \frac{{0,14.96500}}{{5,36}} = 2520,5\left( s \right)\]
Đáp án cần chọn là: A
Câu 20:
+ Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều.
+ Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều.
Cho dãy điện hóa sau:
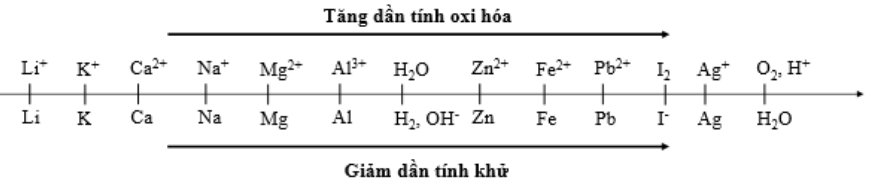
Thí nghiệm 1: Một sinh viên thực hiện quá trình điện phân dung dịch chứa đồng thời Pb(NO3)2 và Al(NO3)3 bằng hệ điện phân sử dụng các điện cực than chì.
Thí nghiệm 2: Sinh viên đó tiếp tục thực hiện điện phân theo sơ đồ như hình bên.
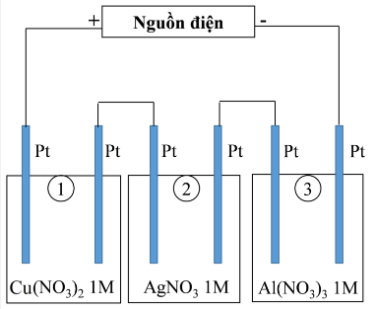
Sau một thời gian, sinh viên quan sát thấy có 3,84 gam kim loại đồng bám lên điệc cực của bình 1. Biết trong hệ điện phân nối tiếp, số điện tử truyền dẫn trong các bình là như nhau. Nguyên tử khối của Ag, Cu và Al lần lượt là 108; 64 và 27 đvC.
Trong thí nghiệm 1, bán phản ứng nào xảy ra ở catot?
 Xem đáp án
Xem đáp án
Trả lời:
Bán phản ứng xảy ra ở catot là Pb2+ + 2e → Pb.
Chú ý: Al3+ không bị điện phân.
Đáp án cần chọn là: A
Câu 21:
+ Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều.
+ Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều.
Cho dãy điện hóa sau:

Thí nghiệm 1: Một sinh viên thực hiện quá trình điện phân dung dịch chứa đồng thời Pb(NO3)2 và Al(NO3)3 bằng hệ điện phân sử dụng các điện cực than chì.
Thí nghiệm 2: Sinh viên đó tiếp tục thực hiện điện phân theo sơ đồ như hình bên.

Sau một thời gian, sinh viên quan sát thấy có 3,84 gam kim loại đồng bám lên điệc cực của bình 1. Biết trong hệ điện phân nối tiếp, số điện tử truyền dẫn trong các bình là như nhau. Nguyên tử khối của Ag, Cu và Al lần lượt là 108; 64 và 27 đvC.
Nếu trong thí nghiệm 1, người sinh viên đổi 2 điện cực than chì bằng 2 điện cực kim loại Pb, phản ứng nào xảy ra ở catot và anot?
 Xem đáp án
Xem đáp án
Trả lời:
Tại catot xảy ra bán phản ứng: Pb2+ + 2e → Pb
Tại anot xảy ra bán phản ứng: Pb → Pb2+ + 2e (cực dương tan dần nên được gọi là hiện tượng dương cực tan).
Đáp án cần chọn là: D
Câu 22:
+ Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều.
+ Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều.
Cho dãy điện hóa sau:

Thí nghiệm 1: Một sinh viên thực hiện quá trình điện phân dung dịch chứa đồng thời Pb(NO3)2 và Al(NO3)3 bằng hệ điện phân sử dụng các điện cực than chì.
Thí nghiệm 2: Sinh viên đó tiếp tục thực hiện điện phân theo sơ đồ như hình bên.

Sau một thời gian, sinh viên quan sát thấy có 3,84 gam kim loại đồng bám lên điệc cực của bình 1. Biết trong hệ điện phân nối tiếp, số điện tử truyền dẫn trong các bình là như nhau. Nguyên tử khối của Ag, Cu và Al lần lượt là 108; 64 và 27 đvC.
Trong thí nghiệm 2, số gam kim loại Ag bám lên điện cực trong bình 2 là
 Xem đáp án
Xem đáp án
Trả lời:
Điện phân dung dịch có thể điều chế các kim loại hoạt động trung bình hoặc yếu (các kim loại đứng sau Al trong dãy điện hóa) bằng cách điện phân dung dịch muối của chúng.
→ Cu2+ và Ag+ bị điện phân; Al3+ không bị điện phân.
Catot của bình 1 (-): Cu2+ + 2e → Cu
→ ne trao đổi (1) = 2.nCu = \[2.\frac{{3,84}}{{64}}\]= 0,12 mol
Catot của bình 2 (-): Ag+ + 1e → Ag
→ ne trao đổi (1) = nAg
Do 3 bình điện phân mắc nối tiếp nên mol electron trao đổi như nhau
→ ne trao đổi (1) = ne trao đổi (2) ⟹ nAg = 0,12 mol
Khối lượng Ag bám lên điện cực trong bình 2 là: mAg = 0,12.108 = 12,96 gam.
Đáp án cần chọn là: C
Câu 23:
*Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều.
+ Nếu điện phân chứa các gốc axit có chứa oxi NO3-, SO42-, PO43-, CO32-, ClO4-, … thì nước sẽ tham gia điện phân theo phương trình: 2H2O → O2 + 4H+ + 4e.
+ Thứ tự anion bị oxi hóa: S2- >I- >Br- >Cl- >RCOO- >OH- >H2O.
*Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều.
+ Nếu điện phân dung dịch có các cation K+, Na+, Ca2+, Ba2+, Mg2+, Al3+ thì nước sẽ tham gia điện phân theo phương trình: 2H2O + 2e → H2 + 2OH-.
+ Nếu trong dung dịch có nhiều cation thì cation nào có tính oxi hóa mạnh hơn sẽ bị điện phân trước.
+ Nếu điện phân không dùng các anot trơ (graphit, platin) mà dùng các kim loại như Ni, Cu, Ag, … thì các kim loại này dễ bị oxi hóa hơn các anion (thế oxi hóa - khử của chúng thấp hơn) và do đó chúng tan vào dung dịch (anot tan).
Thí nghiệm 1: Một sinh viên thực hiện quá trình điện phân dung dịch CuCl2 bằng hệ điện phân sử dụng điện cực Cu.
Thí nghiệm 2: Sinh viên đó tiếp tục thực hiện điện phân dung dịch X bao gồm dung dịch Cu(NO3)2 và NaCl. Sau một thời gian, sinh viên quan sát thấy có 6,4 gam kim loại bám vào catot và anot chỉ thoát ra 1 khí duy nhất. Biết nguyên tử khối của Cu, N, O, Na và Cl lần lượt là 64, 14, 16, 23 và 35,5.
Từ Thí nghiệm 1, cho biết bán phản ứng nào xảy ra ở anot?
 Xem đáp án
Xem đáp án
Trả lời:
Sử dụng điện cực là Cu nên tại anot xảy ra quá trình oxi hóa Cu chứ không phải Cl-.
Bán phản ứng xảy ra tại anot (+): Cu → Cu2+ + 2e.
Đáp án cần chọn là: A
Câu 24:
*Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều.
+ Nếu điện phân chứa các gốc axit có chứa oxi NO3-, SO42-, PO43-, CO32-, ClO4-, … thì nước sẽ tham gia điện phân theo phương trình: 2H2O → O2 + 4H+ + 4e.
+ Thứ tự anion bị oxi hóa: S2- >I- >Br- >Cl- >RCOO- >OH- >H2O.
*Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều.
+ Nếu điện phân dung dịch có các cation K+, Na+, Ca2+, Ba2+, Mg2+, Al3+ thì nước sẽ tham gia điện phân theo phương trình: 2H2O + 2e → H2 + 2OH-.
+ Nếu trong dung dịch có nhiều cation thì cation nào có tính oxi hóa mạnh hơn sẽ bị điện phân trước.
+ Nếu điện phân không dùng các anot trơ (graphit, platin) mà dùng các kim loại như Ni, Cu, Ag, … thì các kim loại này dễ bị oxi hóa hơn các anion (thế oxi hóa - khử của chúng thấp hơn) và do đó chúng tan vào dung dịch (anot tan).
Thí nghiệm 1: Một sinh viên thực hiện quá trình điện phân dung dịch CuCl2 bằng hệ điện phân sử dụng điện cực Cu.
Thí nghiệm 2: Sinh viên đó tiếp tục thực hiện điện phân dung dịch X bao gồm dung dịch Cu(NO3)2 và NaCl. Sau một thời gian, sinh viên quan sát thấy có 6,4 gam kim loại bám vào catot và anot chỉ thoát ra 1 khí duy nhất. Biết nguyên tử khối của Cu, N, O, Na và Cl lần lượt là 64, 14, 16, 23 và 35,5.
Nếu trong Thí nghiệm 1, sinh viên đó thay điện cực Cu bằng điện cực than chì thì bán phản ứng xảy ra ở anot là:
 Xem đáp án
Xem đáp án
Trả lời:
Sử dụng điện cực bằng than chì thì tại anot sẽ xảy ra quá trình oxi hóa Cl-.
Bán phản ứng xảy ra tại anot (+): 2Cl- → Cl2 + 2e.
Đáp án cần chọn là: B
Câu 25:
*Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều.
+ Nếu điện phân chứa các gốc axit có chứa oxi NO3-, SO42-, PO43-, CO32-, ClO4-, … thì nước sẽ tham gia điện phân theo phương trình: 2H2O → O2 + 4H+ + 4e.
+ Thứ tự anion bị oxi hóa: S2- >I- >Br- >Cl- >RCOO- >OH- >H2O.
*Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều.
+ Nếu điện phân dung dịch có các cation K+, Na+, Ca2+, Ba2+, Mg2+, Al3+ thì nước sẽ tham gia điện phân theo phương trình: 2H2O + 2e → H2 + 2OH-.
+ Nếu trong dung dịch có nhiều cation thì cation nào có tính oxi hóa mạnh hơn sẽ bị điện phân trước.
+ Nếu điện phân không dùng các anot trơ (graphit, platin) mà dùng các kim loại như Ni, Cu, Ag, … thì các kim loại này dễ bị oxi hóa hơn các anion (thế oxi hóa - khử của chúng thấp hơn) và do đó chúng tan vào dung dịch (anot tan).
Thí nghiệm 1: Một sinh viên thực hiện quá trình điện phân dung dịch CuCl2 bằng hệ điện phân sử dụng điện cực Cu.
Thí nghiệm 2: Sinh viên đó tiếp tục thực hiện điện phân dung dịch X bao gồm dung dịch Cu(NO3)2 và NaCl. Sau một thời gian, sinh viên quan sát thấy có 6,4 gam kim loại bám vào catot và anot chỉ thoát ra 1 khí duy nhất. Biết nguyên tử khối của Cu, N, O, Na và Cl lần lượt là 64, 14, 16, 23 và 35,5.
Từ Thí nghiệm 2, khối lượng dung dịch giảm là
 Xem đáp án
Xem đáp án
Trả lời:
Tại catot (-) có các cation đi về: Cu2+; Na+ và H2O.
Tại anot (+) có các anion đi về: Cl-; NO3- và H2O.
\[{n_{Cu}} = \frac{{6,4}}{{64}} = 0,1mol\]
Các quá trình trao đổi electron:
+ Tại catot (-) xảy ra quá trình khử
Cu2+ + 2e → Cu
0,2 ← 0,1 (mol)
+ Tại anot (+) xảy ra quá trình oxi hóa
2Cl- → Cl2 + 2e
Áp dụng bảo toàn e:
\[2{n_{Cu}} = 2{n_{C{l_2}}}\]
\[ \to {n_{C{l_2}}} = {n_{Cu}} = 0,1mol\]
Ta có: mdd giảm = mCu↓ + mCl2↑ = 6,4 + 0,1.71 = 13,5 gam.
Đáp án cần chọn là: A
Câu 26:
Sự điện phân là quá trình oxi hóa - khử xảy ra trên bề mặt các điện cực khi có dòng điện một chiều đi qua chất điện li nóng chảy hoặc dung dịch chất điện li nhằm thúc đẩy một phản ứng hóa học mà nếu không có dòng điện, phản ứng sẽ không tự xảy ra. Trong thiết bị điện phân khi điện phân dung dịch:
*Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều.
+ Gốc axit có chứa oxi không bị điện phân (ví dụ: NO3-, SO42-, PO43-, CO32-, ClO4-, …). Khi đó nước bị điện phân theo bán phản ứng: 2H2O → O2 + 4H+ + 4e
+ Thứ tự anion bị điện phân: S2- >I- >Br- >Cl- >RCOO- >OH- >H2O
*Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều.
+ Nếu dung dịch có chứa nhiều cation thì cation nào có tính oxi hóa mạnh hơn sẽ bị điện phân trước.
+ Một số cation không bị điện phân như K+,Na+, Ca2+, Ba2+, Mg2+, Al3+… Khi đó nước bị điện phân theo bán phản ứng: 2H2O + 2e → H2 + 2OH-

Thí nghiệm 1: Một sinh viên thực hiện quá trình điện phân dung dịch X chứa đồng thời AgNO3, Fe(NO3)3, Cu(NO3)2, Fe(NO3)2 bằng hệ điện phân sử dụng các điện cực than chì.
Thí nghiệm 2: Sinh viên đó tiếp tục thực hiện điện phân dung dịch CuCl2. Sau một thời gian sinh viên quan sát thấy có 6,4 gam kim loại bám vào catot. Biết nguyên tử khối của Cu và Cl lần lượt là 64 và 35,5.
ận biết
Trong thí nghiệm 1, thứ tự điện phân các cation tại catot là
 Xem đáp án
Xem đáp án
Trả lời:
Khi điện phân dung dịch, tại catot thì cation nào có tính oxi hóa mạnh hơn sẽ bị điện phân trước.
Dựa vào dãy điện hóa ta thấy tính oxi hóa: Ag+ >Fe3+ >Cu2+ >Fe2+
Vậy thứ tự điện phân là Ag+, Fe3+, Cu2+, Fe2+.
Đáp án cần chọn là: B
Câu 27:
Sự điện phân là quá trình oxi hóa - khử xảy ra trên bề mặt các điện cực khi có dòng điện một chiều đi qua chất điện li nóng chảy hoặc dung dịch chất điện li nhằm thúc đẩy một phản ứng hóa học mà nếu không có dòng điện, phản ứng sẽ không tự xảy ra. Trong thiết bị điện phân khi điện phân dung dịch:
*Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều.
+ Gốc axit có chứa oxi không bị điện phân (ví dụ: NO3-, SO42-, PO43-, CO32-, ClO4-, …). Khi đó nước bị điện phân theo bán phản ứng: 2H2O → O2 + 4H+ + 4e
+ Thứ tự anion bị điện phân: S2- >I- >Br- >Cl- >RCOO- >OH- >H2O
*Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều.
+ Nếu dung dịch có chứa nhiều cation thì cation nào có tính oxi hóa mạnh hơn sẽ bị điện phân trước.
+ Một số cation không bị điện phân như K+,Na+, Ca2+, Ba2+, Mg2+, Al3+… Khi đó nước bị điện phân theo bán phản ứng: 2H2O + 2e → H2 + 2OH-

Thí nghiệm 1: Một sinh viên thực hiện quá trình điện phân dung dịch X chứa đồng thời AgNO3, Fe(NO3)3, Cu(NO3)2, Fe(NO3)2 bằng hệ điện phân sử dụng các điện cực than chì.
Thí nghiệm 2: Sinh viên đó tiếp tục thực hiện điện phân dung dịch CuCl2. Sau một thời gian sinh viên quan sát thấy có 6,4 gam kim loại bám vào catot. Biết nguyên tử khối của Cu và Cl lần lượt là 64 và 35,5.
Trong thí nghiệm 1, giá trị pH của dung dịch thay đổi như thế nào ?
 Xem đáp án
Xem đáp án
Trả lời:
Các quá trình xảy ra trên điện cực:
+ Tại catot:
Ag+ + 1e → Ag
Fe3++ 1e → Fe2+
Cu2+ + 2e → Cu
Fe2+ + 2e → Fe
+ Tại anot: 2H2O → O2 + 4H+ + 4e
Do tại anot sinh ra ion H+ nên pH của dung dịch giảm dần.
Đáp án cần chọn là: B
Câu 28:
Sự điện phân là quá trình oxi hóa - khử xảy ra trên bề mặt các điện cực khi có dòng điện một chiều đi qua chất điện li nóng chảy hoặc dung dịch chất điện li nhằm thúc đẩy một phản ứng hóa học mà nếu không có dòng điện, phản ứng sẽ không tự xảy ra. Trong thiết bị điện phân khi điện phân dung dịch:
*Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều.
+ Gốc axit có chứa oxi không bị điện phân (ví dụ: NO3-, SO42-, PO43-, CO32-, ClO4-, …). Khi đó nước bị điện phân theo bán phản ứng: 2H2O → O2 + 4H+ + 4e
+ Thứ tự anion bị điện phân: S2- >I- >Br- >Cl- >RCOO- >OH- >H2O
*Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều.
+ Nếu dung dịch có chứa nhiều cation thì cation nào có tính oxi hóa mạnh hơn sẽ bị điện phân trước.
+ Một số cation không bị điện phân như K+,Na+, Ca2+, Ba2+, Mg2+, Al3+… Khi đó nước bị điện phân theo bán phản ứng: 2H2O + 2e → H2 + 2OH-

Thí nghiệm 1: Một sinh viên thực hiện quá trình điện phân dung dịch X chứa đồng thời AgNO3, Fe(NO3)3, Cu(NO3)2, Fe(NO3)2 bằng hệ điện phân sử dụng các điện cực than chì.
Thí nghiệm 2: Sinh viên đó tiếp tục thực hiện điện phân dung dịch CuCl2. Sau một thời gian sinh viên quan sát thấy có 6,4 gam kim loại bám vào catot. Biết nguyên tử khối của Cu và Cl lần lượt là 64 và 35,5.
Trong thí nghiệm 2, thể tích khí thoát ra tại điện cực anot là
 Xem đáp án
Xem đáp án
Trả lời:
Các quá trình trao đổi electron:
+ Tại catot: Cu2+ + 2e → Cu
+ Tại anot: 2Cl- → Cl2 + 2e
Ta có:
\[{n_{Cu}} = \frac{{6,4}}{{64}} = 0,1mol\]
Áp dụng định luật bảo toàn electron:
\[2{n_{Cu}} = 2{n_{C{l_2}}}\]
\[ \Rightarrow {n_{Cl_2^{}}} = {n_{Cu}} = 0,2mol\]
\[ \to {V_{C{l_2}}} = 0,1.22,4 = 2,24\left( {lit} \right)\]
Đáp án cần chọn là: B
Câu 29:
 Xem đáp án
Xem đáp án
Trả lời:
n khí = 0,02 (mol)
Do có hỗn hợp khí nên ở Anot Cl- đã điện phân hết và đến H2O điện phân
Hỗn hợp khí là : Cl2 và O2 có số mol lần lượt là x, y.
\[ \Rightarrow \left\{ {\begin{array}{*{20}{c}}{x + y = 0,02}\\{\frac{{71x + 32y}}{{2\left( {x + y} \right)}} = 25,75}\end{array}} \right.\]
\[ \Rightarrow \left\{ {\begin{array}{*{20}{c}}{x + y = 0,02}\\{71x + 32y = 1,03}\end{array}} \right.\]
\[\left\{ {\begin{array}{*{20}{c}}{x = 0,01}\\{y = 0,01}\end{array}} \right.\]
2Cl- - 2e → Cl2
0,02 0,01
2H2O - 4e → O2 + 4H+
0,04 0,01
=>ne = 0,06 (mol)
ở Catot chưa có khí thoát ra tức là Cu2+ dư
=>mCu = 0,03.64 = 1,92 (gam)
Đáp án cần chọn là: C
Câu 30:
Hòa tan hoàn toàn m gam hỗn hợp gồm CuSO4 và FeCl3 vào nước dư thu được dung dịch X. Điện phân dung dịch X với điện cực trơ đến khi ở anot thoát ra 0,2 mol hỗn hợp khí có tỉ khối hơi so với H2 bằng 30,625 thì dừng lại. Dung dịch thu được sau điện phân có chứa 2 muối có nồng độ mol bằng nhau. Giả sử hiệu suất của quá trình điện phân là 100%, khí sinh ra không tan trong dung dịch. Giá trị của m là
 Xem đáp án
Xem đáp án
Trả lời:
Hai khí thoát ra ở anot là Cl2 và O2:
Ta có hệ phương trình:
\[ \Rightarrow \left\{ {\begin{array}{*{20}{c}}{\sum {n_{hh}} = {n_{C{l_2}}} + {n_{{O_2}}} = 0,2}\\{\sum {n_{hh}} = 71{n_{C{l_2}}} + 32{n_{{O_2}}} = 30,625.2.0,2}\end{array}} \right.\]
\[ \Rightarrow \left\{ {\begin{array}{*{20}{c}}{{n_{C{l_2}}} = 0,15}\\{{n_{{O_2}}} = 0,05}\end{array}} \right.\]
Sau phản ứng thu được 2 muối có nồng độ bằng nhau → số mol 2 muối bằng nhau
→ Fe3+ điện phân hết, Cu2+ điện phân dư
BTNT "Cl": 3nFeCl3 = 2nCl2 → nFeCl3 = 2/3. 0,15 = 0,1 (mol)
→ nCu2+ dư = nFe2+ = nFe3+ = 0,1 (mol)
Đặt nCu2+ điện phân = a (mol)
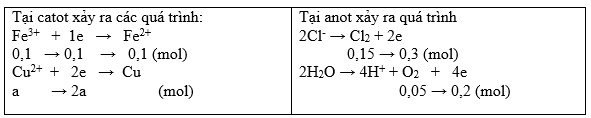
BT e ta có: 0,1 + 2a = 0,3 + 0,2 → a = 0,2 (mol)
BTNT "Cu": nCuSO4 = nCu2+ điện phân + nCu2+ dư = 0,2 + 0,1 = 0,3 (mol)
→ m = mCuSO4 + mFeCl3 = 0,3.160 + 0,1.162,5 = 64,25 (g)
Đáp án cần chọn là: B
Câu 31:
Điện phân dung dịch X chứa hỗn hợp gồm CuSO4 và NaCl (tỉ lệ mol tương ứng 1:3) với điện cực trơ, màng ngăn xốp, cường độ dòng điện không đổi 2A. Sau thời gian điện phân t (giờ) thu được dung dịch Y (chứa 2 chất tan) có khối lượng giảm 12,45 gam so với dung dịch X. Dung dịch Y phản ứng vừa hết với 3,06 gam Al2O3. Bỏ qua sự hòa tan của khí trong nước và sự bay hơi của nước, hiệu suất điện phân 100%. Giá trị của t gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
Trả lời:
nCuSO4 = x(mol); nNaCl = 3x (mol)
Dung dịch X chứa 2 chất tan gồm: Na+: 3x (mol); SO4 2-: x mol =>nOH - = x mol
Mặt khác nAl2O3 = 0,03 (mol) =>nOH - = 2nAl2O3 = 0,06 (mol)
Xét tại cực Catot: nCu = 0,06 mol; nH2 = a mol
Anot: nCl2 = 0,09 mol; nO2 = b mol
=>0,06 * 64 + 2a + 0,09 * 71 +32b = 12,45 (1)
Áp dụng định luật bảo toàn điện tích: 2a - 4b = 0,06 (2)
Từ (1) và (2) =>a = 0,15; b = 0,06
=>ne trao đổi = 0,42 (mol)
=> ne trao đổi= It/F =>t = 5,63 h
Đáp án cần chọn là: D
