Đề kiểm tra giữa học kì 2 môn Hoá 9 có đáp án (Mới nhất) (Đề 10)
-
5702 lượt thi
-
30 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Nước Javen là dung dịch hỗn hợp hai muối NaCl và NaClO.
Câu 2:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Thứ tự hoạt động hóa học của kim loại là Al > Fe > Cu > Ag
Như vậy, trong dãy trên Ag hoạt động hóa học yếu nhất.
Câu 3:
Dẫn chất khí (lượng dư) có công thức hóa học CH2 = CH2 qua dung dịch nước brom màu nâu đỏ. Hiện tượng xảy ra là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Dẫn chất khí (lượng dư) có công thức hóa học CH2 = CH2 qua dung dịch nước brom màu nâu đỏ. Hiện tượng xảy ra là dung dịch brom mất màu hoàn toàn.
Do CH2 = CH2 dư nên brom phản ứng hết tạo ra đibrometan không màu.
Phương trình: CH2 = CH2 + Br2 (dd) → Br – CH2 – CH2 – Br
Câu 4:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Hợp chất chứa cacbon và thuộc loại axit là H2CO3
Câu 5:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Các nguyên tố hóa học trong bảng tuần hoàn được sắp xếp theo chiều tăng dần của điện tích hạt nhân.
Câu 6:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Phân loại một chất là vô cơ hay hữu cơ dựa vào thành phần nguyên tố.
Hợp chất hữu cơ là hợp chất của cacbon (trừ CO, CO2, H2CO3, các muối cacbonat kim loại…)
Câu 7:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Dẫn hỗn hợp khí metan có lẫn SO2 qua dung dịch KOH thì SO2 sẽ phản ứng, còn lại khí metan không phản ứng thoát ra ngoài.
Phương trình: SO2 + 2KOH (dd) → K2SO3 + H2O
Câu 8:
Hiện nay hàm lượng khí CO2 trong khí quyển đang tăng cao gây nên những tác động tiêu cực của “hiệu ứng nhà kính”, làm băng tan và nước biển dâng. Quá trình nào sau đây làm giảm lượng CO2 trong khí quyển?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Quá trình quang hợp của cây xanh hấp thụ khí CO2 và giải phóng khí O2. Làm giảm lượng CO2 trong khí quyển.
Câu 9:
Trong số các hiđrocacbon sau: C3H6, C3H8, C3H4, hiđrocacbon có thể có liên kết ba trong phân tử là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Hiđrocacbon có thể có liên kết ba trong phân tử là C3H4
CH ≡ C – CH3
Câu 10:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Trong cùng một nhóm, theo chiều điện tích hạt nhân tăng, tính kim loại của các nguyên tố tăng dần đồng thời tính phi kim của các nguyên tố giảm dần.
Câu 11:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Ở điều kiện thường, phản ứng etilen tác dụng với dung dịch brom tạo thành đibrometan thuộc loại phản ứng cộng.
CH2 = CH2 + Br2 (dd) → Br – CH2 – CH2 – Br
Câu 12:
Metan và etilen đều tác dụng được với
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Metan và etilen đều tác dụng được với O2 khi đun nóng
CH4 + 2O2 CO2 + 2H2O
C2H4 + 3O2 2CO2 + 2H2O
Câu 13:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu các hợp chất hữu cơ và những chuyển đổi của chúng.
Câu 14:
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Na, Mg, Al theo thứ tự từ trái sang phải cùng thuộc chu kì 3 có tính kim loại giảm dần.
Hay tính kim loại: Na > Mg > Al
Na, K theo thứ tự từ trên xuống dưới cùng thuộc nhóm IA có tính kim loại tăng dần.
Hay tính kim loại K > Na
Do đó tính kim loại giảm dần theo chiều từ: K > Na > Mg > Al.
Câu 15:
Cho phương trình hóa học sau: K2CO3 + 2HCl → 2KCl + X + H2O. X là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
K2CO3 + 2HCl → 2KCl + CO2 + H2O
Vậy X là CO2
Câu 16:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Axit cacbonic (H2CO3) là axit yếu, không bền.
H2CO3 ⇄ CO2 + H2O
Câu 17:
Phản ứng hóa học đặc trưng của metan là phản ứng nào?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Phản ứng hóa học đặc trưng của metan là phản ứng thế.
CH4 + Cl2 CH3Cl + HCl
Câu 18:
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Dẫn xuất của hiđrocacbon là ngoài C và H, trong phân tử còn có các nguyên tố khác như O, N, Cl.
Câu 19:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Chất khí có tác dụng kích thích quả mau chín là etilen (C2H4)
Câu 20:
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
CaCO3 có thể tác dụng với dung dịch HCl
CaCO3 + 2HCl → CaCl2 + H2O + CO2 ↑
Câu 21:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
C2H2 tác dụng được với dung dịch brom tạo ra sản phẩm là chất lỏng ở lại trong dung dịch.
CH ≡ CH + 2Br2 (dư) → CHBr2 – CHBr2
CH4, C2H6 trong phân tử chỉ có liên kết đơn nên không tham gia phản ứng cộng với brom. Do đó hai khí thoát ra ngoài.
Câu 22:
Đốt cháy hoàn toàn 13,44 lít (đktc) hỗn hợp A gồm CH4 và C2H4 rồi cho toàn bộ sản phẩm hấp thụ hết vào dung dịch nước vôi trong dư thấy tạo ra 80g kết tủa. Thành phần phần trăm thể tích khí CH4 trong hỗn hợp A là bao nhiêu?
Cho biết nguyên tử khối của các nguyên tố: C = 12; H = 1; O = 16; Ca = 40.
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
CH4 + 2O2 CO2 + 2H2O (1)
C2H4 + 3O2 2CO2 + 2H2O (2)
CO2 + Ca(OH)2 dư → CaCO3 ↓ + H2O (3)
nhh A = (mol)
Gọi số mol của CH4 và C2H4 lần lượt là x và y (mol)
Ta có: x + y = 0,6 (*)
= = 0,8 (mol)
Theo phương trình (3): = = 0,8 (mol)
Theo phương trình (1): = = x (mol)
Theo phương trình (2): = 2 = 2y (mol)
⇒ x + 2y = 0,8 (**)
Từ (*) và (**) ta có hệ:
⇒ = 0,4 (mol)
= 0,4.22,4 = 8,96 (l)
= ≈ 66,67%
Câu 23:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
SiO2 là oxit axit tác dụng với kiềm tạo muối silicat
SiO2 (r) + 2NaOH(r)Na2SiO3 (r) + H2O
Câu 24:
Dẫn 4,48 lít CO2 (đktc) qua bình đựng nước vôi trong dư. Khối lượng chất kết tủa tạo thành là bao nhiêu?
Cho biết nguyên tử khối của các nguyên tố: C = 12; O = 16; Ca = 40.
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
CO2 + Ca(OH)2 dư → CaCO3 ↓ + H2O
= = 0,2 (mol)
Theo phương trình: = = 0,2 (mol)
Khối lượng kết tủa: = 0,2.(40 +12 + 16.3) = 20 (g)
Câu 25:
Dẫn 0,1 mol hỗn hợp khí metan và axetilen vào dung dịch brom dư, thấy có 0,06 mol khí thoát ra. Các khí đo ở cùng điều kiện nhiệt độ và áp suất. Thành phần phần trăm theo thể tích khí metan có trong hỗn hợp là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
CH ≡ CH + 2Br2 (dư) → CHBr2 – CHBr2
CH4 không phản ứng với dung dịch brom nên khí thoát ra là CH4 (metan)
Thành phần phần trăm theo thể tích cũng bằng phần trăm theo số mol ở cùng điều kiện nhiệt độ và áp suất nên:
= = = 60%
Câu 26:
Dẫn axetilen qua dung dịch brom dư làm bình chứa dung dịch brom tăng lên a gam, a là khối lượng của
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Axetilen phản ứng hết với brom
CH ≡ CH + 2Br2 (dư) → CHBr2 – CHBr2 (l)
Do đó khối lượng bình chứa dung dịch brom tăng là khối lượng của axetilen.
Vậy a là khối lượng của axetilen.
Câu 27:
Đốt cháy hoàn toàn 5,6 gam hiđrocacbon X (gồm hai nguyên tố) thu được 7,2 gam nước. Công thức phân tử của X là
Cho biết nguyên tử khối của các nguyên tố: C = 12; O = 16; H = 1.
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Gọi CTPT của hiđrocacbon X là: CxHy (x; y ∈ ℕ*)
Ta có sơ đồ phản ứng: CxHy CO2 + H2O
= = 0,4 (mol) ⇒ = 2 = 2.0,4 = 0,8 (mol) ⇒ = 0,8.1 = 0,8 (g)
Vì trong X chỉ có hai nguyên tố C và H nên: = = 5,6 – 0,8 = 4,8 (g)
Ta có tỉ lệ:
x : y = = ⇒ Công thức đơn giản nhất của X là: (CH2)n
Trong các công thức phân tử: CH4, C4H10, C3H8, C4H8 chỉ có C4H8 có công thức đơn giản nhất là (CH2)n nên công thức phân tử của hiđrocacbon X là C4H8.
Câu 28:
Đốt cháy 1,2 gam cacbon trong bình chứa 4,48 lít khí oxi. Thể tích khí CO2 thu được sau phản ứng ở đktc là bao nhiêu?
Cho biết nguyên tử khối của các nguyên tố: C = 12; O = 16.
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
C + O2 CO2 ↑
= = 0,1 (mol)
= = 0,2 (mol)
Xét tỉ lệ: ⇒ C hết và O2 dư (tính số mol theo chất hết)
Theo phương trình: = = 0,1 (mol)
= 0,1.22,4 = 2,24 (l)
Câu 29:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Để nhận biết từng khí trong mỗi lọ người ta dùng giấy quỳ tím ẩm
+ Cho quỳ tím ẩm vào khí clo có hiện tượng: quỳ ẩm chuyển đỏ sau đó mất màu.
Cl2 (k) + H2O (l) ⇄ HCl (dd) + HClO (dd)
Dung dịch HCl làm quỳ chuyển đỏ, sau đó HClO có tính tẩy màu làm quỳ mất màu.
+ Cho quỳ tím ẩm vào khí hiđroclorua có hiện tượng: quỳ tím chuyển đỏ.
Do hiđroclorua tan trong nước của quỳ ẩm tạo dung dịch axit HCl làm quỳ chuyển đỏ.
Câu 30:
Cho công thức phân tử C3H6. Số công thức cấu tạo khác nhau có thể có ứng với công thức trên là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Các công thức cấu tạo có thể có của C3H6 là:
CH3 – CH = CH2
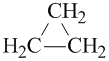
Có 2 công thức cấu tạo.
