Trắc nghiệm Hóa 10 Dạng 4. Giải thích sự tạo thành liên kết cộng hóa trị. Viết công thức Lewis có đáp án
-
2093 lượt thi
-
15 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
Liên kết cộng hóa trị là liên kết được hình thành bởi
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Liên kết cộng hóa trị là liên kết được hình thành bởi một hay nhiều cặp electron chung giữa hai nguyên tử.
Câu 2:
Liên kết cộng hóa trị thường gặp giữa
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Liên kết cộng hóa trị là liên kết được hình thành bởi một hay nhiều cặp electron chung giữa hai nguyên tử, thường gặp giữa phi kim với phi kim.
Ví dụ: Liên kết hóa học trong phân tử O2, N2, CO2, … là liên kết cộng hóa trị.
Câu 3:
Liên kết cho – nhận là một trường hợp đặc biệt của liên kết cộng hóa trị, trong đó
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Liên kết cho – nhận là một trường hợp đặc biệt của liên kết cộng hóa trị, trong đó cặp electron chung chỉ do một nguyên tử đóng góp.
Ví dụ: Khi cặp electron dùng chung chỉ do nguyên tử B đóng góp, nguyên tử B là nguyên tử cho electron, nguyên tử A là nguyên tử nhận electron. Kí hiệu B ® A.
Câu 4:
Trong hợp chất cộng hóa trị, nếu giữa hai nguyên tử có hai cặp electron chung thì
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Trong hợp chất cộng hóa trị, nếu giữa hai nguyên tử có hai cặp electron chung thì hai cặp electron này được biểu diễn bằng một nối đôi (=) và gọi là liên kết đôi.
Ví dụ:

Chú ý:
Nếu giữa hai nguyên tử có một cặp electron chung thì một cặp electron này được biểu diễn bằng một nối đơn (-) và gọi là liên kết đơn.
Nếu giữa hai nguyên tử có ba cặp electron chung thì ba cặp electron này được biểu diễn bằng một nối ba (º) và gọi là liên kết ba.
Câu 5:
Liên kết cộng hóa trị không phân cực là liên kết cộng hóa trị, trong đó
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Liên kết cộng hóa trị trong đó cặp electron dùng chung không bị hút lệch về phía nguyên tử nào được gọi là liên kết cộng hóa trị không phân cực. Ví dụ: Cl2, N2.
Liên kết cộng hóa trị trong đó cặp electron dùng chung lệch về phía nguyên tử có độ âm điện lớn hơn được gọi là liên kết cộng hóa trị phân cực. Ví dụ: HCl (cặp electron dùng chung lệch về phía nguyên tử có độ âm điện lớn hơn là Cl).
Câu 6:
Công thức Lewis của một phân tử được xây dựng từ công thức electron của phân tử, trong đó
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Công thức Lewis của một phân tử được xây dựng từ công thức electron của phân tử, trong đó mỗi cặp electron chung giữa hai nguyên tử tham gia liên kết được thay bằng một gạch nối “ – ”.
Ví dụ:

Câu 7:
Cho các phân tử sau: NaCl, HCl, O2, N2, NH3, CO2, MgO. Có bao nhiêu phân tử có liên kết cộng hóa trị?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Liên kết cộng hóa trị là liên kết được hình thành bởi một hay nhiều cặp electron chung giữa hai nguyên tử, thường gặp giữa phi kim với phi kim.
® Liên kết hóa học trong phân tử HCl, O2, N2, NH3, CO2 là liên kết cộng hóa trị.
Chú ý:
Liên kết hóa học trong phân tử NaCl, MgO là liên kết ion.
Liên kết ion được hình thành bởi lực hút tĩnh điện giữa các ion mang điện tích trái dấu. Liên kết ion được hình thành giữa kim loại điển hình và phi kim điển hình.
Câu 8:
Liên kết hóa học trong phân tử nào sau đây là liên kết cộng hóa trị có cực?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Liên kết cộng hóa trị trong đó cặp electron dùng chung lệch về phía nguyên tử có độ âm điện lớn hơn được gọi là liên kết cộng hóa trị phân cực.
® Liên kết hóa học trong phân tử HCl là liên kết cộng hóa trị có cực (cặp electron dùng chung lệch về phía nguyên tử có độ âm điện lớn hơn là Cl).
Chú ý:
Liên kết cộng hóa trị trong đó cặp electron dùng chung không bị hút lệch về phía nguyên tử nào được gọi là liên kết cộng hóa trị không phân cực.
® Liên kết hóa học trong phân tử Cl2, N2, O2 là liên kết cộng hóa trị không cực.
Câu 9:
Công thức cấu tạo của N2 là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Cấu hình electron của nguyên tử N (Z = 7): 1s22s22p3 (có 5 electron ở lớp ngoài cùng).
Nguyên tử nitrogen có 5 electron hóa trị, hai nguyên tử nitrogen liên kết với nhau bằng cách mỗi nguyên tử nitrogen đóng góp 3 electron, tạo thành 3 cặp electron dùng chung. Khi đó, trong phân tử N2, mỗi nguyên tử đều có 8 electron ở lớp ngoài cùng, thỏa mãn quy tắc octet.

Câu 10:
Liên kết giữa 2 nguyên tử O trong phân tử O2 là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Cấu hình electron của nguyên tử O (Z = 8): 1s22s22p4 (có 6 electron ở lớp ngoài cùng).
Mỗi nguyên tử oxygen có 6 electron hóa trị, hai nguyên tử oxygen liên kết với nhau bằng cách mỗi nguyên tử đóng góp 2 electron, tạo thành 2 cặp electron dùng chung. Trong phân tử O2, mỗi nguyên tử oxygen đều có 8 electron ở lớp ngoài cùng, thỏa mãn quy tắc octet.

® Liên kết giữa 2 nguyên tử O trong phân tử O2 là liên kết đôi.
Câu 11:
Trong phân tử hoặc ion nào sau đây chứa liên kết cho – nhận?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Trong phân tử H2O, nguyên tử oxygen còn 2 cặp electron chưa liên kết, ion H+ có orbital trống, không chứa electron.
Khi cho H2O kết hợp với ion H+, nguyên tử oxygen sử dụng một cặp electron chưa liên kết làm cặp electron chung với ion H+ tạo thành hydronium (H3O+). Trong ion H3O+, nguyên tử oxygen đóng góp cặp electron chung nên là nguyên tử cho, ion H+ không đóng góp electron, đóng vai trò nhận electron.
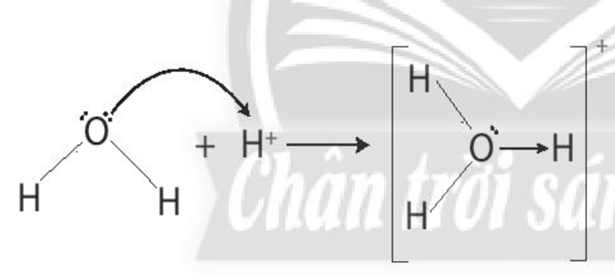
Chú ý: Tất cả các liên kết O-H trong ion H3O+ là tương đương nhau, nhưng để biểu diễn cho liên kết cho – nhận hiện diện trong ion, người ta dùng mũi tên được hướng từ nguyên tử cho sang nguyên tử nhận để phân biệt với các liên kết còn lại.
Câu 12:
Phát biểu nào sau đây không đúng?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Sơ đồ tạo thành phân tử carbon dioxide:

Nhận xét:
Phân tử CO2 có hai liên kết đôi.
Liên kết giữa C và O là liên kết cộng hóa trị phân cực (cặp electron chung lệch về phía nguyên tử có độ âm điện lớn hơn là O). Tuy nhiên, do phân tử CO2 có cấu tạo thẳng nên độ phân cực của hai liên kết (C=O) triệt tiêu nhau, dẫn đến toàn bộ phân tử không bị phân cực.
® Phát biểu không đúng là: Phân tử CO2 là phân tử phân cực vì chứa liên kết cộng hóa trị phân cực.
Câu 13:
Liên kết giữa nguyên tử H và F trong phân tử HF được tạo nên bởi
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Nguyên tử H có cấu hình electron là 1s1; nguyên tử F có cấu hình electron là 1s22s22p5. Để đạt được cấu hình của khí hiếm gần nhất, mỗi nguyên tử này đều cần thêm 1 electron. Vì vậy, mỗi nguyên tử H và F cùng góp 1 electron để tạo nên 1 cặp electron chung.
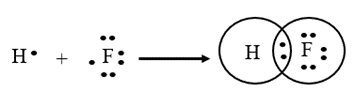
Công thức cấu tạo của HF là: H – F.
Câu 14:
Trong phân tử chlorine (Cl2), hai nguyên tử chlorine liên kết với nhau bằng cách
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Cấu hình electron của nguyên tử Cl (Z = 17): [Ne]3s23p5 (có 7 ở lớp ngoài cùng).
Để đạt cấu hình của khí hiếm gần nhất, nguyên tử Cl cần thêm 1 electron. Vì vậy, hai nguyên tử chlorine liên kết với nhau bằng cách mỗi nguyên tử chlorine góp 1 electron, tạo thành 1 cặp electron dùng chung. Khi đó, trong phân tử Cl2, mỗi nguyên tử đều có 8 electron ở lớp ngoài cùng, thỏa mãn quy tắc octet:
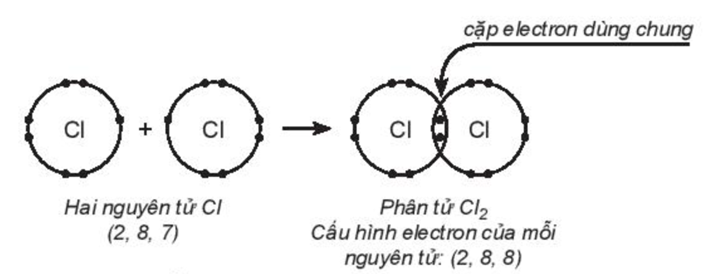
Từ công thức electron, thay một cặp electron dùng chung bằng một gạch nối thì thu được công thức Lewis:

Câu 15:
Chọn phát biểu đúng.
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Phát biểu đúng: Trong phân tử SO2 có liên kết cho – nhận.
Loại B, vì: Liên kết trong phân tử NaCl là liên kết ion.
Loại C, vì: Liên kết trong phân tử O2 là liên kết cộng hóa trị không phân cực.
Loại D, vì: Công thức cấu tạo của phân tử N2 là NºN (liên kết ba).
