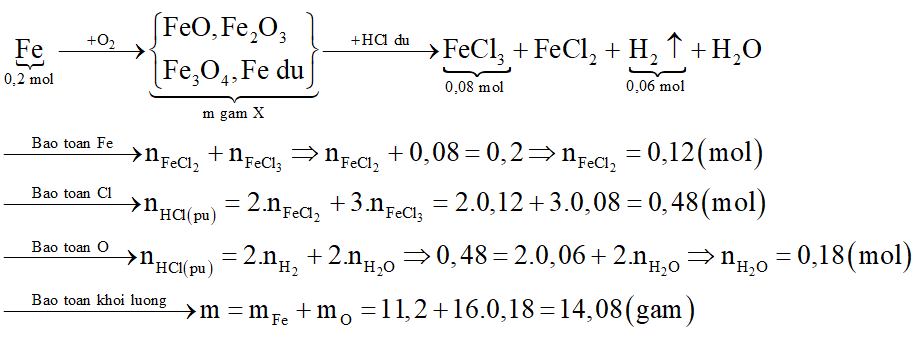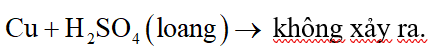- Đề số 1
- Đề số 2
- Đề số 3
- Đề số 4
- Đề số 5
- Đề số 6
- Đề số 7
- Đề số 8
- Đề số 9
- Đề số 10
- Đề số 11
- Đề số 12
- Đề số 13
- Đề số 14
- Đề số 15
- Đề số 16
- Đề số 17
- Đề số 18
- Đề số 19
- Đề số 20
- Đề số 21
- Đề số 22
- Đề số 23
- Đề số 24
- Đề số 25
- Đề số 26
- Đề số 27
- Đề số 28
- Đề số 29
- Đề số 30
- Đề số 31
- Đề số 32
- Đề số 33
- Đề số 34
- Đề số 35
- Đề số 36
- Đề số 37
Trắc nghiệm tổng hợp Hóa 9 Chương 1: Các loại hợp chất vô cơ có đáp án - Đề 10
-
6511 lượt thi
-
20 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
Kim loại nào sau đây tan hết trong nước dư ở nhiệt độ thường?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Kim loại tác dụng với H2O ở điều kiện thường là Na:
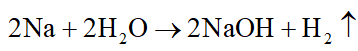
Câu 3:
Các dung dịch nào sau đây đều tác dụng với Al2O3?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Al2O3 tác dụng được với HCl và NaOH:
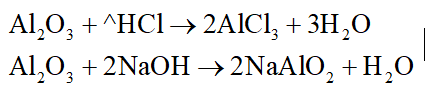
Câu 4:
Cho 25,5 gam hỗn hợp X gồm CuO và Al2O3 tan hoàn toàn trong dung dịch H2SO4 loãng, thu được dung dịch chứa 57,9 gam muối. Phần trăm khối lượng của Al2O3 trong X là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
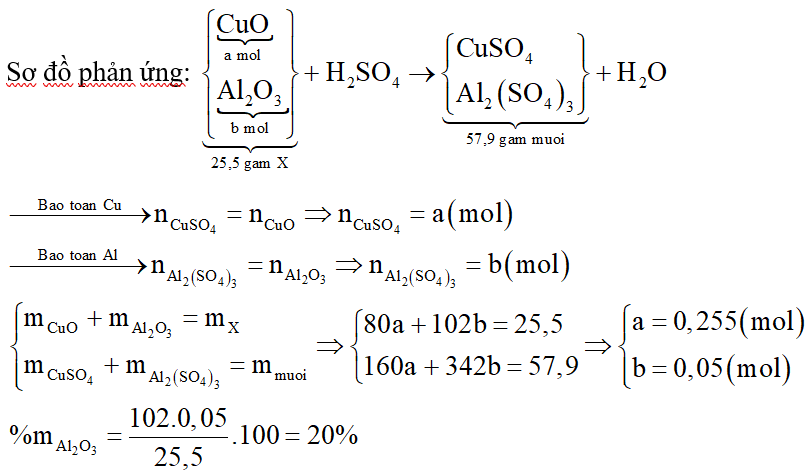
Câu 5:
Sản phẩm thu được khi điện phân dung dịch HCl (điện cực trơ, màng ngăn xốp) là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
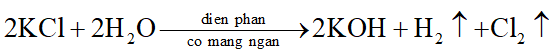
Câu 6:
Cho 12 gam hỗn hợp gồm Fe và Cu tác dụng với dung dịch HCl (dư), thu được 2,24 lít H2 (đktc) và m gam chất rắn không tan. Giá trị của m là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Cu không tác dụng với dung dịch HCl nên chất rắn không tan là Cu.
Số mol H2 thu được là:
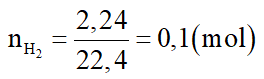
Phương trình hóa học:
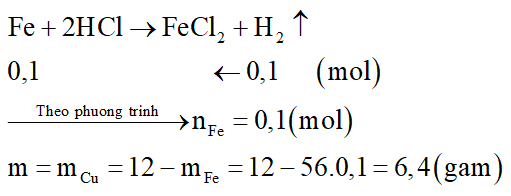
Câu 7:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
H2 không khử được oxit kim loại nhóm IA, nhóm IIA và Al.
Câu 8:
Cho dãy các oxit sau: Na2O, Al2O3, Cr2O3, CaO, CrO3, MgO. Số oxit trong dãy tác dụng với nước ở điều kiện thường là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Các oxit tác dụng được với H2O ở điều kiện thường gồm Na2O, CaO và CrO3:
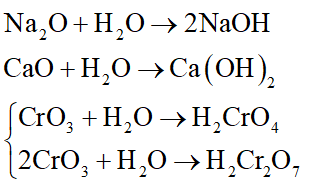
Câu 9:
Để xử lý chất thải có tính axit, người ta thường dùng?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Để xử lý chất thải có tính axit, người ta thường dùng chất có tính bazơ như nước vôi,…
Câu 10:
Hòa tan hết hỗn hợp gồm fe, FeCO3 trong dung dịch H2SO4 loãng dư, thu được dung dịch X và 4,48 lít hỗn hợp khí Y (đktc). Cô cạn dung dịch X, thu được lượng muối khan là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Số mol Y thu được là:
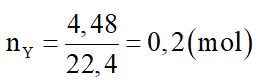
Các phương trình phản ứng:
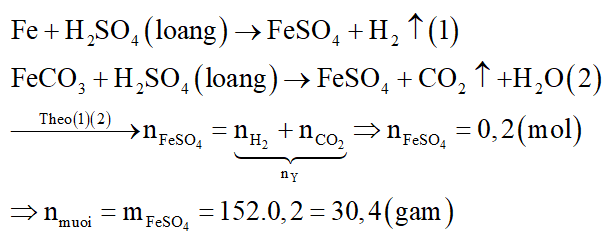
Câu 11:
Cho V1 ml dung dịch NaOH 0,4M vào V2 ml dung dịch H2SO4 0,6M. Sau khi kết tủa phản ứng thu được dung dịch chỉ chứa một chất tan duy nhất. Tỉ lệ V1:V2 là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Số mol các chất là:
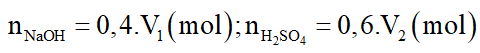
Phương trình hóa học:
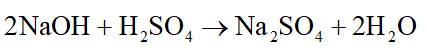
Dung dịch thu được chỉ chứa một chất tan duy nhất nên NaOH phản ứng vừa đủ với H2SO4.
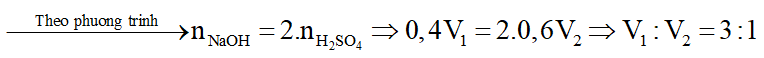
Câu 12:
Oxit nào sau đây tác dụng với nước ở điều kiện thường tạo dung dịch bazơ?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
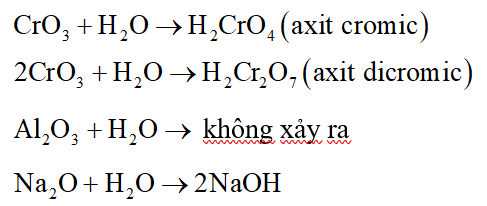
Câu 13:
Có ba mẫu hợp kim cùng khối lượng: Al – Cu, Cu – Ag, Mg – Al. Dùng hóa chất nào sau đây có thể phân biệt 3 mẫu hợp kim trên?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Dùng dung dịch HCl để phân biệt ba mẫu hợp kim trên.
|
|
Al – Cu |
Cu – Ag |
Mg – Al |
|
Dung dịch HCl |
Tan một phần |
Không tan |
Tan hoàn toàn |
Phương trình phản ứng:
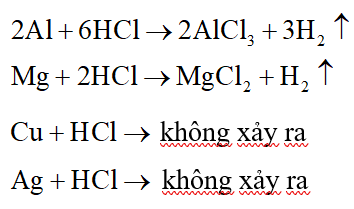
Câu 14:
Cho dãy các kim loại: Na, Ca, Cu, Fe, K. Số kim loại trong dãy không tác dụng với H2O tạo thành dung dịch bazơ là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
- Các kim loại tác dụng với nước tạo thành dung dịch bazơ gồm: Na, Ca, K

- Các kim loại không tác dụng với H2O tạo thành dung dịch bazơ gồm: Fe, Cu.
Câu 15:
Hấp thụ hết V lít khí CO2 (đktc) trong dung dịch chứa 0,3 mol Ba(OH)2, thu được kết tủa và khối lượng dung dịch tăng 2,3 gam. Giá trị của V là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
- Các phương trình hóa học có thể xảy ra:
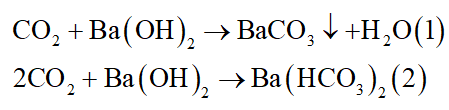
- Khối lượng dung dịch tăng
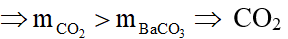
tác dụng với dung dịch thu được hai muối theo sơ đồ sau:
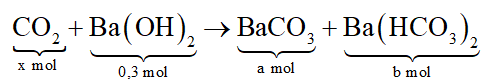
- Gọi số mol các muối thu được là BaCO3: a mol; Ba(HCO3)2: b mol
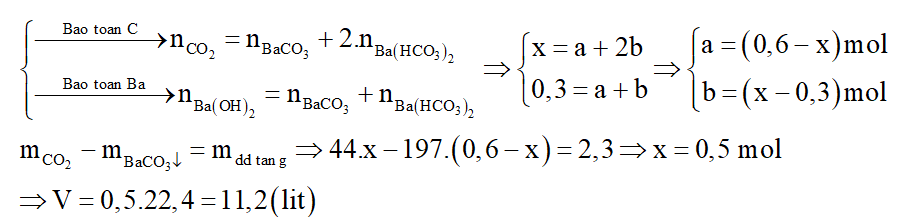
Câu 16:
Cho 6,48 gam kim loại X (hóa trị không đổi) tác dụng với O2 thu được 11,28 gam chất rắn Y. Cho Y tác dụng với dung dịch HCl dư thu được 1,344 lít khí H2 (khí đo ở đktc). Kim loại X là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
+ Chất rắn Y tác dụng với dung dịch HCl thu được khí H2 nên trong Y có X dư.
Số mol H2 thu được là:
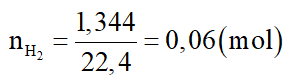
Gọi n là hóa trị của X.
Xét giai đoạn X tác dụng với O2.
Sơ đồ phản ứng:
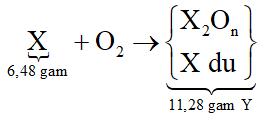
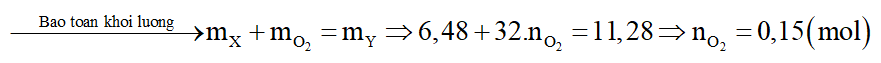
Phương trình hóa học:
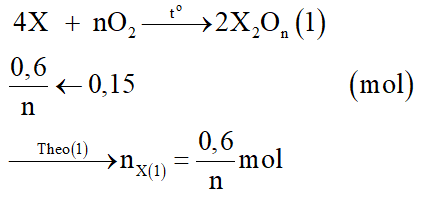
+ Chất rắn Y gồm X2On và X dư. Y tác dụng với dung dịch HCl dư:
Phương trình hóa học:
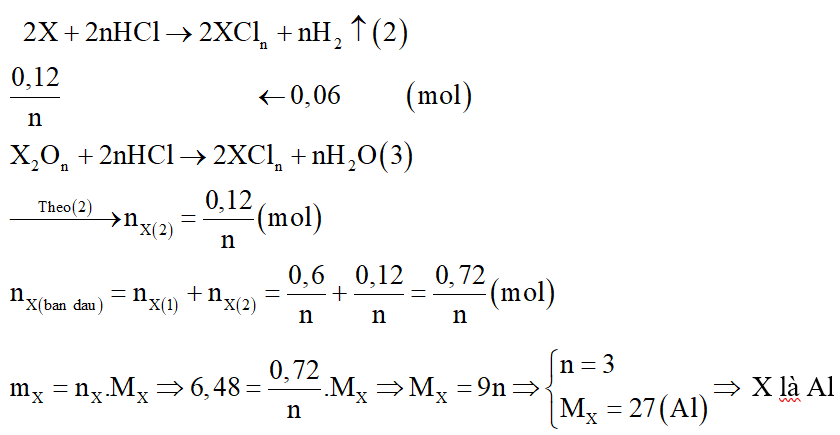
Câu 17:
Hòa tan m gam hỗn hợp gồm KHCO3 và CaCO3 trong lượng dư dung dịch HCl. Sau khi các phản ứng xảy ra hoàn toàn thu được 5,04 lít CO2 (đktc). Giá trị của m là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Số mol CO2 thu được là:
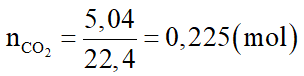
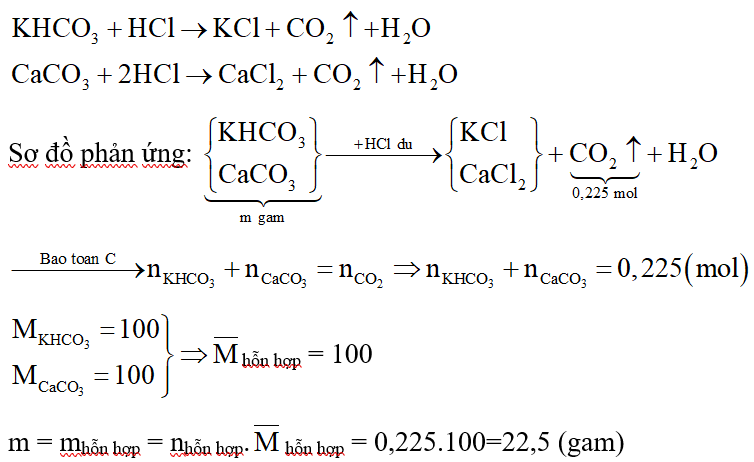
Các phương trình hóa học:
Câu 18:
Để 2,24 gam sắt lâu ngày trong không khí thu được hỗn hợp rắn X gồm 4 chất. Hòa tan X trong dung dịch H2SO4 loãng, dư thu được dung dịch A. Cho A tác dụng hết với dung dịch NaOH, thu được hỗn hợp chất rắn B. Nung B trong không khí đến khối lượng không đổi thu được m gam chất rắn D. Giá trị của m là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Các phương trình phản ứng:
Đốt cháy Fe trong không khí:
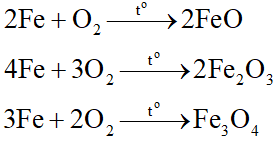
X gồm FeO, Fe2O3, Fe3O4 và Fe dư. X tác dụng với dung dịch H2SO4 loãng, dư:
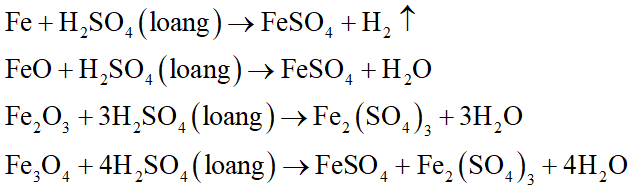
Dung dịch A gồm FeSO4, Fe2(SO4)3 và H2SO4 dư. Dung dịch A tác dụng với dung dịch NaOH:
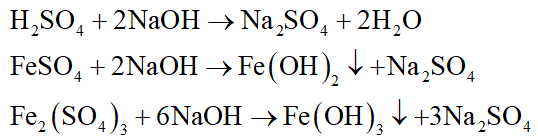
Hỗn hợp rắn B gồm Fe(OH)2 và Fe(OH)3. Nung B trong không khí:
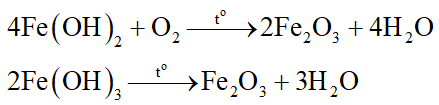
Rắn D là Fe2O3.
Tính toán:
Số mol Fe là:
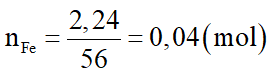
Sơ đồ phản ứng:
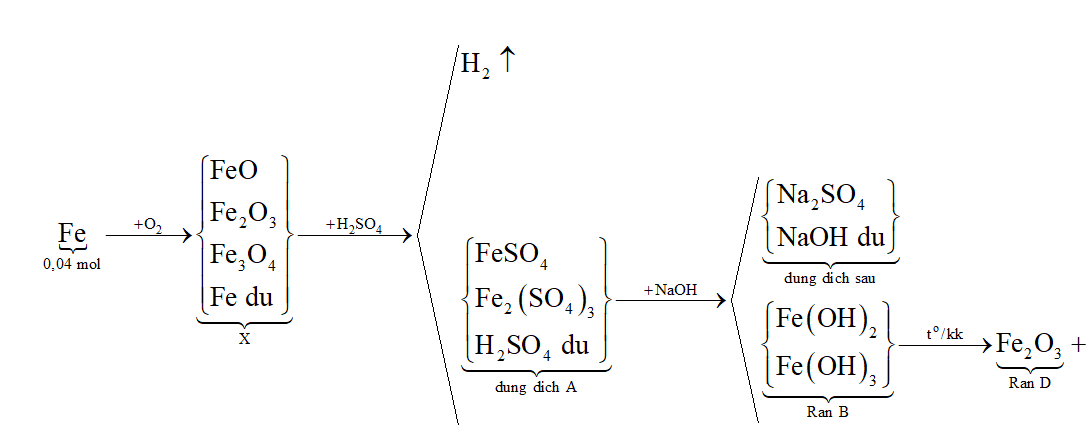
Theo sơ đồ phản ứng thì Fe ban đầu chuyển hết về Fe2O3 trong rắn D. Bảo toàn nguyên tố Fe ta có:
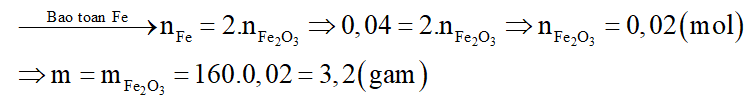
Câu 19:
Hòa tan hoàn toàn 24 gam hỗn hợp X gồm MO, M(OH)2 và MCO3 (M là kim loại có hóa trị không đổi) trong 100 gam dung dịch H2SO4 39,2% thu được 1,12 lít khí (đktc) và dung dịch Y chỉ chứa một chất tan duy nhất có nồng độ 39,41%. Kim loại M là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Sơ đồ phản ứng:
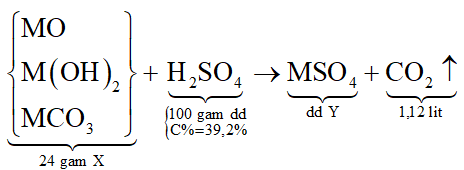
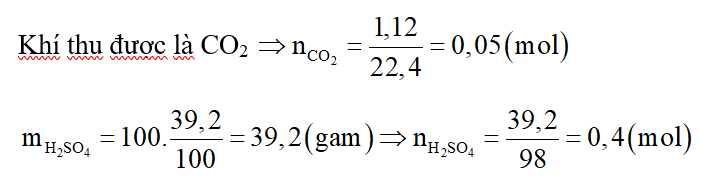
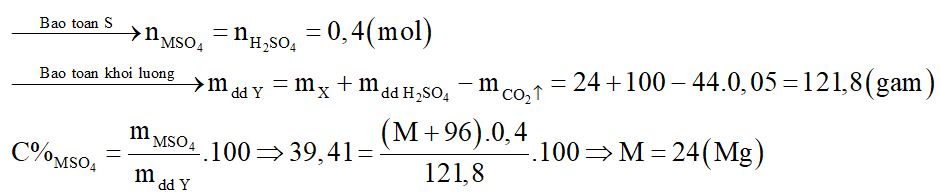
Câu 20:
Đốt cháy 11,2 gam bột Fe trong oxi, sau một thời gian thu được m gam chất rắn X. Hòa tan hết X trong dung dịch HCl loãng dư, thu được 1,344 lít khí H2 (đktc) và dung dịch Y có chứa 13,0 gam FeCl3. Giá trị của m là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Số mol các chất là:
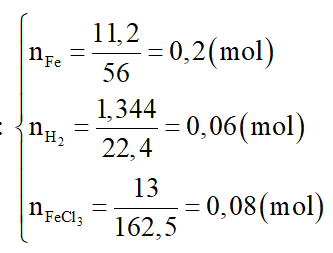
Các phương trình hóa học:
Đốt Fe trong O2:
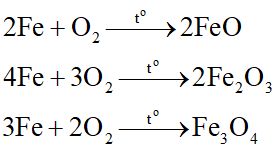
X gồm FeO, Fe2O3, Fe3O4 và Fe dư. X tác dụng với dung dịch HCl dư:
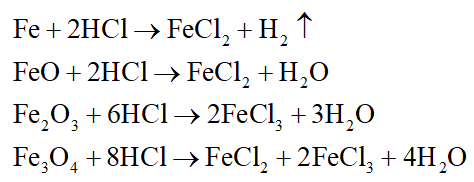
Sơ đồ phản ứng: