- Đề số 1
- Đề số 2
- Đề số 3
- Đề số 4
- Đề số 5
- Đề số 6
- Đề số 7
- Đề số 8
- Đề số 9
- Đề số 10
- Đề số 11
- Đề số 12
- Đề số 13
- Đề số 14
- Đề số 15
- Đề số 16
- Đề số 17
- Đề số 18
- Đề số 19
- Đề số 20
- Đề số 21
- Đề số 22
- Đề số 23
- Đề số 24
- Đề số 25
- Đề số 26
- Đề số 27
- Đề số 28
- Đề số 29
- Đề số 30
- Đề số 31
- Đề số 32
- Đề số 33
- Đề số 34
- Đề số 35
- Đề số 36
Bộ đề kiểm tra định kì học kì 1 Hóa 9 có đáp án (Mới nhất) - Đề 27
-
7766 lượt thi
-
19 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
Một dung dịch có các tính chất sau:
- Tác dụng với nhiều kim loại như Mg, Zn, Fe giải phóng khí hiđro.
- Tác dụng với bazơ hoặc oxit bazơ tạo thành muối và nước
- Tác dụng với đá vôi và giải phóng khí cacbonic
Dung dịch đó là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
- Axit clohiđric tác dụng với các kim loại đứng trước H trong dãy hoạt động hóa học của kim loại, giải phóng khí hiđro.
- Axit clohiđric tác dụng với bazơ/oxit bazơ, tạo muối và nước
- Axit clohiđric tác dụng với CaCO3 giải phóng khí cacbonic.
Câu 3:
Nhỏ một giọt quỳ tím vào dung dịch NaOH, dung dịch có màu xanh; nhỏ từ từ dung dịch HCl cho tới dư, hiện tượng xảy ra là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Dung dịch NaOH là dung dịch kiềm nên làm quỳ tím chuyển sang xanh. Khi cho HCl vào, xảy ra phản ứng trung hòa: làm lượng NaOH giảm xuống nên màu danh nhạt dần và mất hẳn. Đến khi HCl dư, tạo môi trường axit cho dung dịch nên quỳ tím chuyển sang đỏ.
Câu 6:
Cho bột đồng tác dụng với dung dịch axit sunfuric đặc nóng, chất khí thu được là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Đồng không tác dụng với H2SO4 loãng nhưng lại tác dụng với H2SO4 đặc nóng, giải phóng khí SO2
Câu 7:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Canxi oxit được điều chế bằng cách nung đá vôi (thành phần chính là CaCO3) bằng lò nung vôi thủ công hoặc lò nung vôi công nghiệp
Câu 8:
Cặp chất nào sau đây cùng tồn tại trong một dung dịch?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
KNO3 và BaCl2 không phản ứng với nhau nên có thể tồn tại trong cùng một dung dịch.
Câu 9:
Dùng thuốc thử nào có thể phân biệt được các chất rắn sau: MgO, P2O5, BaO, Na2SO4?
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
- MgO không tan trong nước
- Na2SO4 tan trong nước tạo dung dịch muối trung hòa không làm đổi màu quỳ tím
- P2O5 tác dụng với nước tạo dung dịch axit, làm quỳ tím hóa đỏ.
- BaO tác dụng với nước tạo dung dịch bazơ, làm quỳ tím hóa xanh
Câu 10:
Đốt cháy hoàn toàn 6 gam cacbon. Dẫn toàn bộ khí sinh ra đi qua 500ml dung dịch Ca(OH)2 0,5M. Khối lượng kết tủa thu được sau phản ứng là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Số mol C là:
Từ phương trình
500ml = 0,5 lít
Số mol Ca(OH)2 là:
Ta có tỉ lệ:
Muối tạo thành là Ca(HCO3)2 tan
Vậy sau phản ứng không thu được kết tủa.
Câu 12:
Cho 16,2 gam kim loại M (hóa trị n không đổi) tác dụng với 0,15 mol khí oxi. Hòa tan chất rắn sau phản ứng bằng dung dịch HCl dư thấy thoát ra 13,44 lít khí (đktc). Xác định M.
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
4 n 2
Từ phương trình (1)
Vì chất rắn thu được tác dụng với HCl giải phóng khí H2 nên M còn dư
2 2n 2 n
Số mol H2 là:
Từ phương trình (2)
Tổng số mol kim loại M ban đầu là:
Lập bảng giá trị n:
|
n |
1 |
2 |
3 |
|
M |
9 (loại) |
18 (loại) |
27 (chọn) |
Vậy kim loại M là Al
Câu 13:
Chất nào sau đây tác dụng với khí oxi tạo ra oxit bazơ?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Hầu hết kim loại tác dụng với oxi tạo ra oxit bazơ.
Câu 14:
Cho phản ứng giữa lưu huỳnh với hiđro như hình vẽ sau, trong đó ống nghiệm 1 để tạo ra H2, ống nghiệm 2 dùng để nhận biết sản phẩm trong ống.
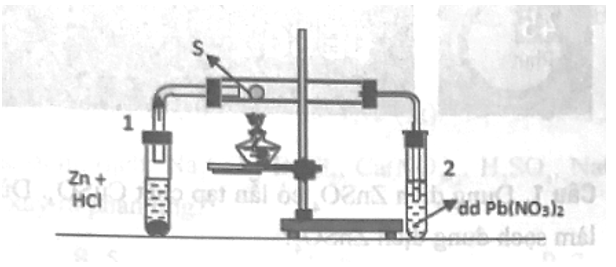
Hiện tượng quan sát được trong ống nghiệm 2 là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Phương trình xảy ra trong ống nghiệm 1:
Khí H2 bay ra tác dụng với lưu huỳnh đun nóng trong ống:
Khí H2S được dẫn vào dung dịch Pb(NO3)2 ở ống nghiệm 2, tạo kết tủa màu đen là PbS.
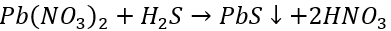
Câu 15:
Sục từ từ khí SO2 vào dung dịch X xuất hiện kết tủa trắng, sau đó kết tủa tan. X là dung dịch nào?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Sục từ từ SO2 vào dung dịch Ca(OH)2 thu được CaSO3 kết tủa màu trắng
Khi SO2 dư thì kết tủa bị hòa tan lại, tạo dung dịch muối Ca(HSO3)2 trong suốt không màu.
Câu 16:
 Xem đáp án
Xem đáp án
- Điện phân dung dịch NaCl có màng ngăn, thu được dung dịch NaOH, khí Cl2 và H2
- Điều chế muối đồng (II) clorua bằng cách đốt kim loại đồng với khí clo vừa thu được.
- Điều chế đồng (II) hiđroxit bằng cách cho NaOH và CuCl2 tác dụng với nhau, lọc lấy kết rủa:
- Nhiệt phân hoàn toàn kết tủa thu được, ta được đồng (II) oxit.
Câu 17:
 Xem đáp án
Xem đáp án
Trong hệ thống nước máy ở thành phố, người ta cho vào một lượng nhỏ khí clo nhằm diệt khuẩn, khí clo tác dụng với nước không hoàn toàn nên có một phần gây mùi.
Axit hipoclorơ HClO có tính oxi hóa rất mạnh nên có tác dụng khử trùng, sát khuẩn nước.
Câu 18:
Hòa tan hoàn toàn 4 gam hỗn hợp gồm 1 kim loại hóa trị II và 1 kim loại hóa trị III cần dùng hết 170 ml dung dịch HCl 2M.
a) Tính thể tích khí hiđro thu được ở đktc.
 Xem đáp án
Xem đáp án
a) 170ml = 0,17 lít
Số mol HCl là:
Áp dụng định luật bảo toàn nguyên tố cho hiđro, ta có:
Thể tích khí hiđro thu được (đktc) là:
Câu 19:
b)* Cho kim loại hóa trị III là nhôm và có số mol bằng 5 lần số mol kim loại hóa trị II. Xác định kim loại hóa trị II.
 Xem đáp án
Xem đáp án
b) Gọi X là kim loại hóa trị II chưa biết, a là số mol của X trong hỗn hợp ban đầu
2 3
1 1
Số mol nhôm bằng 5 lần số mol X nên nAl = 5.nX = 5a
Từ phương trình ta có số mol H2 là:
Khối lượng hỗn hợp kim loại ban đầu:
Vậy kim loại M là Zn
