Đề kiểm tra cuối học kì 2 Hóa 11 Cánh diều có đáp án (Đề 2)
-
78 lượt thi
-
28 câu hỏi
-
0 phút
Danh sách câu hỏi
Câu 1:
Hydrocarbon Y có công thức cấu tạo như sau: (CH3)2CHCH2CH3. Khi cho Y phản ứng với bromine có thể thu được bao nhiêu dẫn xuất monobromo là đồng phân cấu tạo của nhau?
 Xem đáp án
Xem đáp án
Chọn B
Câu 2:
Hợp chất X có phân tử khối là 56; có công thức đơn giản nhất là CH2. Công thức phân tử của X là
 Xem đáp án
Xem đáp án
Chọn C
Câu 3:
Ứng với công thức phân tử C5H8 có bao nhiêu alkyne là đồng phân cấu tạo của nhau?
 Xem đáp án
Xem đáp án
Chọn A
Câu 5:
Trong thể thao, khi các vận động viên bị chấn thương do va chạm, không gây ra vết thương hở, gãy xương, ... thường được nhân viên y tế dùng loại thuốc xịt, xịt vào chỗ bị thương để gây tê cục bộ và vận động viên có thể quay trở lại thi đấu. Hợp chất (X) chính có trong thuốc xịt là
 Xem đáp án
Xem đáp án
Chọn D
Câu 6:
Khi được chiếu sáng, benzene có thể phản ứng với Cl2 tạo thành sản phẩm nào?
 Xem đáp án
Xem đáp án
Chọn C
Câu 8:
Để loại bỏ lớp cặn màu trắng trong ấm đun nước, người ta có thể dùng dung dịch nào sau đây?
 Xem đáp án
Xem đáp án
Chọn A
Câu 10:
Theo Nghị định 100/2019/NĐ-CP, người điều khiển giao thông không được có nồng độ cồn trong máu hoặc hơi thở. Để xác định hàm lượng rượu trong máu người lái xe, người ta sử dụng phương pháp chuẩn độ ethanol có trong mẫu huyết tương bằng K2Cr2O7, môi trường acid. Khi đó CrO3 bị khử thành Cr2O3 (đổi từ màu vàng cam sang xanh), C2H5OH bị oxi hoá thành chất nào sau đây?
 Xem đáp án
Xem đáp án
Chọn C
Câu 12:
Thực hiện phản ứng khử hợp chất carbonyl sau:
CH3COCH2CH3 + 2[H] ?
Sản phẩm thu được là
 Xem đáp án
Xem đáp án
Chọn B
Câu 15:
Một phân tử polyethylene có phân tử khối là 840 000u. Hệ số polymer hóa của phân tử này là
 Xem đáp án
Xem đáp án
Chọn D
Câu 16:
Yếu tố nào sau đây không làm tăng hiệu suất phản ứng ester hoá giữa acetic acid và ethanol?
 Xem đáp án
Xem đáp án
Chọn D
Câu 17:
Oxi hoá alcohol đơn chức X bằng CuO (đun nóng), sinh ra một sản phẩm hữu cơ duy nhất là ketone Y (tỉ khối hơi của Y so với khí hydrogen bằng 29). Công thức cấu tạo của X là
 Xem đáp án
Xem đáp án
Chọn A
Câu 18:
Rutin có nhiều trong hoa hoè. Rutin có tác dụng làm bền vững thành mạch, chống co thắt, chống phóng xạ tia X. Rutin có công thức phân tử C27H30O16 và công thức cấu tạo như sau:
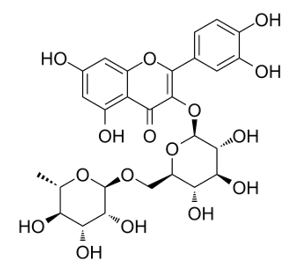
Phân tử rutin có bao nhiêu nhóm -OH alcohol và bao nhiêu nhóm -OH phenol?
 Xem đáp án
Xem đáp án
Chọn A
Câu 19:
Dẫn dòng khí gồm acetylene và ethylene lần lượt đi vào ống nghiệm (1) đựng dung dịch AgNO3/NH3 ở điều kiện thường, sau đó dẫn tiếp qua ống nghiệm (2) đựng nước bromine.
a) Ở ống nghiệm (1) có kết tủa màu vàng nhạt.
b) Ở ống nghiệm (2) màu của nước bromine nhạt dần.
c) Ở ống nghiệm (2) chất lỏng chia thành hai lớp.
d) Ở ống nghiệm (2) thu được chất lỏng đồng nhất.
 Xem đáp án
Xem đáp án
|
a |
Đ |
|
b |
Đ |
|
c |
Đ |
|
d |
S |
Câu 20:
Hợp chất X chứa vòng benzene có công thức phân tử là C8H8O2. Biết X tác dụng được với dung dịch NaOH theo sơ đồ phản ứng sau: X + 2NaOH Y +2H2O.
Cho các phát biểu sau:
a) X có 5 liên kết pi trong phân tử.
b) Y là alcohol đa chức.
c) Trong phân tử Y có 6 nguyên tử hydrogen.
d) X có khả năng làm mất màu dung dịch bromine.
 Xem đáp án
Xem đáp án
|
a |
S |
|
b |
S |
|
c |
Đ |
|
d |
Đ |
Câu 21:
Khi thay thế nguyên tử halogen của phân tử hydrocarbon bằng nguyên tử halogen được dẫn xuất halogen của hydrocarbon (gọi tắt là dẫn xuất halogen).
a) Do phân tử phân cực nên dẫn xuất halogen không tan trong dung môi hữu cơ như hydrocarbon, ether.
b) Nhiều dẫn xuất halogen có hoạt tính sinh học.
c) Trong điều kiện thường, dẫn xuất halogen có thể ở dạng rắn, lỏng hay khí tuỳ thuộc vào khối lượng phân tử, bản chất và số lượng nguyên tử halogen.
d) Nhiều dẫn xuất halogen được sử dụng trong tổng hợp các chất hữu cơ.
 Xem đáp án
Xem đáp án
|
a |
S |
|
b |
Đ |
|
c |
Đ |
|
d |
Đ |
Câu 22:
Aspirin được sử dụng để hạ sốt và giảm đau nhẹ đến trung bình do tình trạng đau nhức cơ, răng, cảm lạnh đau đầu và sưng tấy do viêm khớp.
Aspirin có công thức cấu tạo như sau:
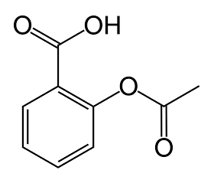
a. Aspirin là hợp chất đa chức.
b. Aspirin có 1 nhóm – OH alcohol.
c. Oxygen chiếm khoảng 35,6% khối lượng aspirin.
d. Công thức phân tử của asprin là C9H8O4.
 Xem đáp án
Xem đáp án
|
a |
S |
|
b |
S |
|
c |
Đ |
|
d |
Đ |
Câu 23:
Cho dung dịch acetic acid có nồng độ x% tác dụng vừa đủ với dung dịch NaOH 20% thu được dung dịch muối sodium acetate có nồng độ 10,25%. Giá trị của x là bao nhiêu?
 Xem đáp án
Xem đáp án
Gọi a là số mol CH3COOH phản ứng.
Phương trình hoá học:
CH3COOH + NaOH → CH3COONa + H2O
(mol) a → a
\( \Rightarrow \)\({m_{{\rm{dd}}\,NaOH}} = \frac{{40a}}{{20\% }} = 200a\,(g)\)
\( \Rightarrow \)\({m_{{\rm{dd}}\,{\rm{C}}{{\rm{H}}_3}{\rm{COONa}}}} = \frac{{82a}}{{10,25\% }} = 800a\,(g)\) \( \Rightarrow \)\({m_{dd\,C{H_3}COOH}} = 600a\,(g).\)
\( \Rightarrow \)\(C{\% _{C{H_3}COOH}} = \frac{{60a}}{{600a}} \times 100\% = 10\% .\)
Câu 24:
Tiến hành chuẩn độ acetic acid bằng dung dịch sodium hydroxide 0,15 M. Sau khi thực hiện thí nghiệm chuẩn độ này 3 lần, thu được bảng dưới đây:
|
Số lần |
Thể tích acetic acid (mL) |
Thể tích dung dịch NaOH cần dùng (mL) |
|
1 |
6,0 |
20,0 |
|
2 |
6,0 |
19,9 |
|
3 |
6,0 |
20,0 |
Nồng độ mol của acetic acid là bao nhiêu?
 Xem đáp án
Xem đáp án
Thể tích trung bình của dung dịch NaOH 3 lần đo:
\({{\rm{V}}_{{\rm{NaOH}}}}{\rm{ = }}\frac{{{\rm{20}}{\rm{,0 + 19}}{\rm{,9 + 20}}{\rm{,0}}}}{{\rm{3}}} \approx {\rm{20}}{\rm{,0 mL}}\);
Thể tích của acetic acid: \({{\rm{V}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}}{\rm{ = 6}}{\rm{,0 mL}}\);
Ta có:\[{{\rm{V}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}} \times {{\rm{C}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}} = {{\rm{V}}_{{\rm{NaOH}}}} \times {{\rm{C}}_{{\rm{NaOH}}}}\]
Nồng độ mol của acetic acid:
\[{{\rm{C}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}} = \frac{{{{\rm{V}}_{{\rm{NaOH}}}}{\rm{ \times }}{{\rm{C}}_{{\rm{NaOH}}}}}}{{{{\rm{V}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}}}} = \frac{{0,15 \times 20,0}}{{6,0}} = 0,5\]M
Câu 25:
Xăng E5 chứa 5% thể tích ethanol hiện đang được sử dụng phổ biến ở nước ta để thay thế một phần xăng thông thường. Một người đi xe máy mua 2 L xăng E5 để đổ vào bình chứa nhiên liệu. Thể tích ethanol có trong lượng xăng trên là bao nhiêu mL?
 Xem đáp án
Xem đáp án
Thể tích ethanol có trong lượng xăng trên là: \(\frac{5}{{100}}.2 = 0,1\,(L) = 100\,mL\)
Câu 26:
Sản phẩm chính theo quy tắc Zaitsev của phản ứng tách HCl ra khỏi phân tử 2-chloro-3-methyl butane là gì?
 Xem đáp án
Xem đáp án
Câu 27:
Cho 50 gam dung dịch acetaldehyde tác dụng với lượng dư dung dịch AgNO3 trong NH3, thu được 21,6 gam Ag. Nồng độ phần trăm của acetaldehyde trong dung dịch đã sử dụng là bao nhiêu?
 Xem đáp án
Xem đáp án
CH3CHO + 2[Ag(NH3)2]OH CH3COONH4 + 2Ag↓ + 3NH3 + H2O
0,1 0,2 (mol)
Theo đề bài, ta có: \({n_{Ag}} = \frac{{21,6}}{{108}} = 0,2\,(mol)\)
Theo phương trình hóa học:
\(\begin{array}{l} \Rightarrow {n_{C{H_3}CHO}} = \frac{1}{2} \times {n_{Ag}} = \frac{1}{2} \times 0,2 = 0,1\,(mol).\\ \Rightarrow C{\% _{C{H_3}CHO}} = \frac{{0,1 \times 44}}{{50}} \times 100\% = 8,8\% .\end{array}\)
Câu 28:
Gas, nhiên liệu phổ biến hiện nay có thành phần chính là propane và butane. Nhiệt lượng giải phóng khi đốt cháy hoàn toàn 1 kg một loại gas là khoảng 50 400 kJ. Biết để làm nóng 1 kg nước lên 1 độ thì cần cung cấp nhiệt lượng là 4 200 J. Để đun sôi 30 kg nước từ nhiệt độ 20oC cần cung cấp bao nhiêu kJ nhiệt?
 Xem đáp án
Xem đáp án
Để đun sôi 30 kg nước từ nhiệt độ 20oC, cần cung cấp nhiệt lượng là:
\(\frac{{4200 \times 30 \times (100 - 20)}}{{1000}} = 10080\)kJ.
