Đề kiểm tra giữa kì 1 Hóa 11 KNTT có đáp án (Đề 4)
-
77 lượt thi
-
32 câu hỏi
-
60 phút
Danh sách câu hỏi
Câu 2:
Mối quan hệ giữa tốc độ phản ứng thuận (vt) và tốc độ phản ứng nghịch (vn) ở trạng thái cân bằng được biểu diễn như thế nào?
 Xem đáp án
Xem đáp án
Chọn B
Câu 6:
Biểu thức nào sau đây là biểu thức hằng số cân bằng (KC) của phản ứng:
C(s) + 2H2(g) CH4(g)
 Xem đáp án
Xem đáp án
Chọn D
Câu 7:
Cho cân bằng hóa học sau: N2(g) + 3H2(g) 2NH3(g) có ∆H < 0. Cân bằng trên chuyển dịch theo chiều thuận khi
 Xem đáp án
Xem đáp án
Chọn C
Câu 8:
Cho cân bằng hóa học sau: CaCO3(s) CaO(s) + CO2(g)
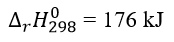
Yếu tố nào sau đây làm cho cân bằng dịch chuyển theo chiều thuận?
 Xem đáp án
Xem đáp án
Chọn C
Câu 9:
Đối với phản ứng sau, cân bằng sẽ bị ảnh hưởng như thế nào khi tăng nhiệt độ (các điều kiện khác giữ không đổi)?
H2(g) + O2(g) H2O(l) = -286 kJ
 Xem đáp án
Xem đáp án
Chọn B
Câu 10:
Các dung dịch acid, base, muối dẫn điện được là do trong dung dịch của chúng có các
 Xem đáp án
Xem đáp án
Chọn A
Câu 17:
Cho các chất: NH3, HCl, H3PO4, Ba(OH)2. Theo thuyết Bronsted – Lowry có bao nhiêu chất trong dãy trên là acid?
 Xem đáp án
Xem đáp án
Chọn D
Câu 21:
Quan sát hình bên dưới và từ dữ kiện năng lượng liên kết trong phân tử N2, dự đoán về độ bền phân tử và khả năng phản ứng của nitrogen ở nhiệt độ thường.
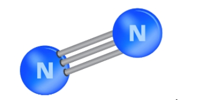
.
Eb (NºN) = 945 kJ/mol
 Xem đáp án
Xem đáp án
Chọn B
Câu 26:
Bóng cười được bơm một loại khí có tên gọi là Dinitrogen. Công thức phân tử của Dinitrogen là
 Xem đáp án
Xem đáp án
Chọn D
Câu 27:
Cho các nhận định sau về cấu tạo phân tử nitric acid:
(a) Liên kết O-H phân cực về oxygen.
(b) Nguyên tử ![]() có số oxi hoá là +5.
có số oxi hoá là +5.
(c) Liên kết cho - nhận kém bền.
Số nhận định đứng là
 Xem đáp án
Xem đáp án
Chọn C
Câu 28:
X là một trong các nguyên nhân gây ra mưa acid, sương mù quang hoá, hiệu ứng nhà kính, hiện tượng phù nhưỡng, ô nhiễm môi trường .… X là
 Xem đáp án
Xem đáp án
Chọn C
Câu 29:
Hãy mô tả đặc điểm của ao, hồ có hiện tượng phú dưỡng và đề xuất cách cải tạo?
 Xem đáp án
Xem đáp án
Đặc điểm của ao, hồ có hiện tượng phú dưỡng
- Xuất hiện dày đặc tảo xanh trong nước.
- Nguồn thuỷ sản trong ao hồ bị suy kiệt.
- Xuất hiện mùi hôi thối khó chịu.
Cách cải tạo
- Sử dụng chế phẩm vi sinh để tăng vi sinh có lợi. Tảo phát triển mạnh trong nước thiếu oxygen. Do đó tăng cường oxygen ngay lập tức bằng việc lắp đặt thiết bị sục khí để khuấy trộn bề mặt ao và giúp giải phóng các loại khí như CO2. Điều này cũng cho phép nước hấp thụ nhiều oxygen hơn, trong thời gian ngắn sẽ giúp giảm sự hiện diện của tảo.
- Xử lí nước thải trước khi đổ vào ao hồ. Nước ao, hồ nên được thay, càng nhiều càng tốt (nên dùng nước đã được xử lý trước khi cấp vào ao).
- Trồng một số thực vật thuỷ sinh phù hợp với môi trường phú dưỡng: bèo tây, ngổ trâu, cải xoong … Trồng thực vật thủy sinh cũng sẽ làm giảm mức độ dinh dưỡng trong nước ao, hồ và do đó không khuyến khích sự nhân lên của thực vật phù du.
(Nếu HS nêu được một vài ý trong các gạch đầu dòng trên vẫn cho điểm tối đa của mỗi ý)Câu 31:
a/ Cho 100 ml dung dịch hỗn hợp gồm Ba(OH)2 0,1M và NaOH 0,1M với V ml dung dịch HCl 0,0875M thu được dd có pH = 2. Tính giá trị V?
b/ Cẩm tú cầu là loài hoa được trồng nhiều nhất tại Sa Pa hay Đà Lạt. Màu của loại hoa này có thể thay đổi tùy thuộc vào pH của thổ nhưỡng nên có thể điều chỉnh màu hoa thông qua việc điều chỉnh độ pH của đất trồng:
|
pH đất trồng |
<7 |
=7 |
>7 |
|
Hoa sẽ có màu |
Lam |
Trắng sữa |
Hồng |
 Xem đáp án
Xem đáp án
· ![]() mol OH- = 0,03 mol; Mol H+ = 0,0875 V
mol OH- = 0,03 mol; Mol H+ = 0,0875 V
Dung dịch sau khi trộn pH = 2 → Môi trường axit.
PTHH: H+ + OH- H2O
0,03 0,03
· H+ dư = 0,0875V- 0,03
Hay (0,0875V-0,03)/(0,1+V) = 10-2 → V = 0,4 litCâu 32:
 Xem đáp án
Xem đáp án
Bón thêm vôi CaO và tưới nước thì trong đất sẽ có phản ứng xảy ra:
CaO + H2O → Ca(OH)2
Dung dịch Ca(OH)2 có môi trường kiềm → pH đất trồng > 7
→ Hoa cẩm tú cầu trồng trên đất này sẽ có màu hồng.