Trắc nghiệm Hóa học 11 KNTT Sulfur và sulfur dioxide có đáp án
-
161 lượt thi
-
15 câu hỏi
-
40 phút
Danh sách câu hỏi
Câu 1:
Tính chất nào sau đây không phải tính chất vật lí của sulfur?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Tính chất vật lí của sulfur: Ở điều kiện thường, sulfur có màu vàng, ở thể rắn, không tan trong nước, ít tan trong alcohol,…Câu 2:
Cho các phản ứng sau:
(a) S + O2 SO2
(b) Hg + S HgS
(c) S + 6HNO3 H2SO4 + 6NO2 + 2H2O
(d) Fe + S FeS
Có bao nhiêu phản ứng trong đó sulfur đóng vai trò là chất khử?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Sulfur đóng vai trò là chất khử trong phản ứng (a), (c).
Câu 3:
Sulfur dioxide có tính chất hóa học gì?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Sulfur dioxide vừa có tính khử và vừa có tính oxi hoá.
Câu 4:
Sulfur trong chất nào sau đây vừa có tính oxi hóa, vừa có tính khử?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Sulfur dioxide vừa có tính khử và vừa có tính oxi hoá.
Câu 5:
SO2 luôn thể hiện tính khử trong các phản ứng với
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
SO2 luôn thể hiện tính khử trong các phản ứng với O2, nước Br2, dung dịch KMnO4.
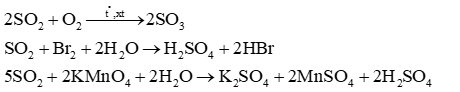
Câu 6:
Dãy chất nào sau đây đều thể hiện tính oxi hóa khi phản ứng với SO2?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Dãy chất thể hiện tính oxi hóa khi phản ứng với SO2 là O2, nước bromine, dung dịch KMnO4.
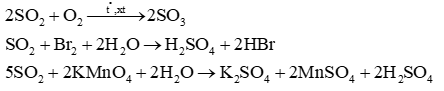
Câu 7:
Khí nào sau đây có khả năng làm mất màu nước bromine?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Khí SO2 có khả năng làm mất màu nước bromine.
\[S{O_2} + B{r_2} + 2{H_2}O \to 2HBr + {H_2}S{O_4}\]
Câu 8:
Sulfur dioxide có thể tham gia những phản ứng sau:
(1) SO2 + Br2 + 2H2O H2SO4 + 2HBr
(2) SO2 + 2H2S 3S + 2H2O
Câu nào sau đây diễn tả không đúng tính chất của các chất trong phản ứng trên?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Vì phản ứng (2): SO2 là chất oxi hóa.
Câu 9:
Cho các phản ứng:
(1) SO2 + Br2 + 2H2O →
(2) 2SO2 + O2
(3) 5SO2 + 2KMnO4 + 2H2O →
(4) SO2 + 2NaOH →
(5) SO2 + 2H2S →
(6) SO2 + 2Mg →
Tính oxi hóa của SO2 được thể hiện ở phản ứng nào?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
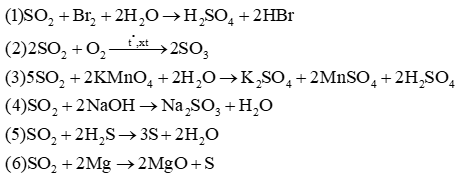
Câu 10:
Cho các phản ứng:
(1) SO2 + Cl2 + 2H2O → H2SO4 + 2HCl
(2) SO2 + 2Mg → S + 2MgO
(3) SO2 + 2H2S → 3S + 2H2O
(4) 2SO2 + O2 → 2SO3
(5) SO2 + NaOH → NaHSO3
(6) SO2 + 2NaOH → Na2SO3 + H2O
(7) 5SO2 + 2KMnO4 + 2H2O → 2H2SO4 + K2SO4 + 2MnSO4
Những phản ứng mà SO2 thể hiện tính khử là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Những phản ứng mà SO2 thể hiện tính khử là (1); (4); (7).
Câu 11:
Chất được dùng để tẩy trắng giấy và bột giấy trong công nghiệp là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
SO2 dùng để tẩy trắng giấy và bột giấy trong công nghiệp.
Câu 12:
SO2 là một khí độc được thải ra từ các vùng công nghiệp, là một trong những nguyên nhân chính gây ra hiện tượng nào dưới đây?
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
SO2 là một khí độc được thải ra từ các vùng công nghiệp, là một trong những nguyên nhân chính gây ra hiện tượng mưa acid.
Câu 13:
Cho các phát biểu sau:
(a) Sulfur là chất rắn, màu trắng, không tan trong nước.
(b) Sulfur và sulfur dioxide vừa có tính oxi hóa, vừa có tính khử.
(c) Khi phản ứng với hydrogen, sulfur thể hiện tính oxi hóa
(d) Nước thải sinh hoạt là một trong các nguồn phát thải khí SO2.
(e) Sulfur dioxide được sử dụng để tẩy trắng vải sợi, bột giấy, sản xuất sulfuric acid và diệt nấm mốc.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Phát biểu đúng là (b), (c), (e)
(a) sai vì sulfur là chất rắn màu vàng.
(d) sai vì khí thải trong sinh hoạt (đốt cháy các nhiên liệu hoá thạch như than) mới thải khí SO2.
Câu 14:
Để phân biệt CO2 và SO2 chỉ cần dùng thuốc thử là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Để phân biệt CO2 và SO2 chỉ cần dùng thuốc thử là nước bromine. Vì chỉ có SO2 mới phản ứng với nước bromine, còn CO2 thì không.
\[S{O_2} + B{r_2} + 2{H_2}O \to 2HBr + {H_2}S{O_4}\]
Câu 15:
Cho các phản ứng sinh ra khí SO2:
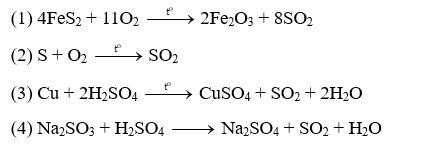
Các phản ứng được dùng để điều chế khí SO2 trong công nghiệp là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Các phản ứng được dùng để điều chế khí SO2 trong công nghiệp là: (1) và (2).
