Trắc nghiệm Hóa 11 CD Bài 5. Một số hợp chất quan trọng của nitrogen có đáp án
Trắc nghiệm Hóa 11 CD Bài 5. Một số hợp chất quan trọng của nitrogen có đáp án
-
145 lượt thi
-
30 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
Khi cho giấy quỳ tím tẩm ướt vào bình đựng khí NH3 thì giấy quỳ tím chuyển sang màu
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Khi cho giấy quỳ tím tẩm ướt vào bình đựng khí NH3 thì giấy quỳ tím chuyển sang màu xanh.
Câu 2:
Ở trạng thái lỏng nguyên chất, phân tử chất nào sau đây tạo được liên kết hydrogen với nhau?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
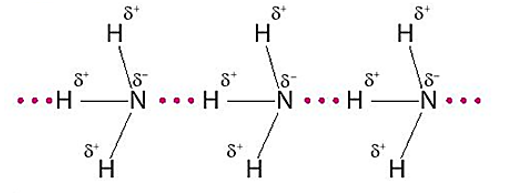
Các phân tử ammonia có thể tạo được liên kết hydrogen với nhau
Câu 3:
Trong nước, phân tử/ion nào sau đây thể hiện vai trò là acid theo thuyết Bronsted - Lowry?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
có khả năng nhường proton, thể hiện vai trò là acid theo thuyết Bronsted – Lowry.
Câu 4:
Cho dung dịch vào dung dịch chất nào sau đây thu được kết tủa trắng?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
3NH3 + AlCl3 + 3H2O → Al(OH)3↓ + 3NH4Cl
Câu 5:
Nhiệt phân hoàn toàn muối nào sau đây thu được sản phẩm chỉ gồm khí và hơi?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Câu 6:
Phân biệt được đung dịch và NaCl bằng thuốc thử là dung dịch
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Phân biệt được đung dịch và NaCl bằng thuốc thử là dung dịch KOH.
+ Nếu có khí mùi khai thoát ra → NH4Cl.
+ Nếu không có hiện tượng xuất hiện → NaCl.
Câu 7:
Chất có thể dùng để làm khô khí NH3 là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
KOH rắn có tác dụng hút ẩm và KOH rắn không phản ứng với NH3 nên được dùng để làm khô khí NH3.
Câu 8:
Tính base của NH3 do:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Tính base của NH3 do: trên N còn cặp e tự do.
Câu 9:
Trong các phản ứng dưới đây, phản ứng nào NH3 thể hiện tính base?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Câu 10:
Cho phản ứng: 2NH3 + 3Cl2 6HCl +N2. Kết luận nào sau đây đúng?
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Số oxi hoá của N tăng từ -3 lên 0, do đó NH3 đóng vai trò là chất khử trong phản ứng.
Câu 11:
Xét cân bằng hoá học:
.
Cân bằng sẽ chuyển dịch theo chiều thuận khi cho thêm vài giọt dung dịch nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Thêm HCl sẽ làm giảm OH−, do đó cân bằng sẽ chuyển dịch theo chiều thuận, tức chiều sinh ra nhiều OH−.
Câu 12:
Cho phương trình: N2(g) + 3H2(g) 2NH3 (g)
Khi tăng nồng độ của hydrogen lên 2 lần, tốc độ phản ứng thuận:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Áp dụng định luật tác dụng khối lượng:
Khi tăng nồng độ của hydrogen lên 2 lần, tốc độ phản ứng thuận tăng 23 = 8 lần.
Câu 13:
X là muối khi tác dụng với dung dịch NaOH dư sinh khí mùi khai, tác dụng với dung dịch BaCl2 sinh kết tủa trắng không tan trong HNO3. X là muối nào trong số các muối sau?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
(NH4)2SO4 + 2NaOH → Na2SO4 + 2NH3↑ + 2H2O
(NH4)2SO4 + BaCl2 → 2NH4Cl + BaSO4↓
Câu 14:
Cho các phát biểu sau:
(1) Các muối ammonium tan trong nước tạo dung dịch chất điện li mạnh;
(2) Ion NH4+ tác dụng với dung dịch acid tạo kết tủa màu trắng;
(3) Muối ammonium tác dụng với dung dịch base thu được khí có mùi khai;
(4) Hầu hết muối ammonium đều bền nhiệt.
Phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Các phát biểu (1) và (3) đúng.
Câu 15:
Xét cân bằng hoá học: .
Hiệu suất phản ứng khi hệ đạt cân bằng ở áp suất 200 bar và 300 bar lần lượt bằng x % và y %. Mối quan hệ giữa x và y là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Khi tăng áp suất, cân bằng chuyển dịch theo chiều làm giảm số mol khí tức chiều thuận.
Như vậy, mối quan hệ giữa hiệu suất phản ứng khi hệ đạt cân bằng ở 200 bar và 300 bar là x < y.
Câu 16:
Trong phân tử HNO3, nguyên tử N có:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
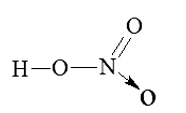
Từ công thức cấu tạo của HNO3 xác định được trong phân tử HNO3, nguyên tử N có hoá trị là IV.
Gọi số oxi hoá của N trong HNO3 là x, ta có: (+1) + x + (-2).3 = 0 Þ x = +5.
Câu 17:
Phú dưỡng là hiện tượng xảy ra do sự gia tăng hàm lượng của nguyên tố
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Phú dưỡng là hiện tượng xảy ra do sự gia tăng hàm lượng của nguyên tố nitrogen (N) và phosphorus (P).
Câu 19:
Kim loại nào sau đây không tác dụng với nitric acid?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Au (gold, vàng) không tác dụng với HNO3.
Câu 20:
Kim loại không tan trong dung dịch HNO3 đặc, nguội là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Al bị thụ động hoá trong HNO3 đặc, nguội.
Câu 21:
Hợp chất nào của nitrogen không được tạo ra khi cho HNO3 tác dụng với kim loại?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
N2O5 không được tạo ra khi cho HNO3 tác dụng với kim loại.
Câu 22:
Cho phản ứng:
Hệ số tỉ lượng của HNO3 trong phương trình hoá học trên là (biết hệ số tỉ lượng của các chất trong phản ứng là các số nguyên, tối giản)
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Câu 23:
Cho phản ứng:
Hệ số tỉ lượng a, b, c, d, e là những số nguyên dương có tỉ lệ tối giản. Tổng (a + b) bằng
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Vậy a + b = 5.
Câu 24:
Cho dung dịch tác dụng với các chất sau: . Số phản ứng trong đó đóng vai trò acid theo thuyết Brønsted – Lowry là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
HNO3 đóng vai trò acid theo thuyết Brønsted – Lowry khi phản ứng với NH3, CaCO3, NaOH.
Câu 25:
Một oxide của nitrogen có công thức NOx trong đó N chiếm 30,43% về khối lượng. Công thức của oxide đó là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Vậy oxide là NO2.
Câu 26:
Cho Iron(III) oxide tác dụng với nitric acid thì sản phẩm thu được là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Fe2O3 + 6HNO3 → 2Fe(NO3)3 + 3H2O
Câu 27:
Dãy gồm tất cả các chất khi tác dụng với HNO3 thì HNO3 chỉ thể hiện tính oxi hoá là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
HNO3 chỉ thể hiện tính oxi hoá khi tác dụng với dãy:
Câu 28:
Xét phản ứng trong quá trình tạo ra NOx nhiệt:
Nhiệt tạo thành chuẩn của NO(g) là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Nhiệt tạo thành chuẩn của NO:
Câu 29:
Cho m gam Al phản ứng hoàn toàn với dung dịch HNO3 loãng (dư), thu được 4,958 lít khí NO (đkc, sản phẩm khử duy nhất). Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
PTHH:
Theo phương trình: nAl = nNO = 0,2 (mol)
→ mAl = 0,2.27 = 5,4 (g).
Câu 30:
Cho 19,2 gam kim loại M tan hết trong dung dịch HNO3 dư thu được 4,958 lít khí NO duy nhất (đkc). Kim loại M là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Áp dụng định luật bảo toàn electron: ne nhường = ne nhận
Þ (với n là hoá trị của kim loại).
Vậy n = 2; M = 64 thoả mãn. Kim loại là Cu.