Đề kiểm tra cuối học kì 2 Hóa 11 CTST có đáp án (Đề 2)
-
80 lượt thi
-
28 câu hỏi
-
60 phút
Danh sách câu hỏi
Câu 4:
Công thức phân tử nào sau đây có thể là công thức của hợp chất thuộc dãy đồng đẳng của benzene?
 Xem đáp án
Xem đáp án
Chọn D
Câu 5:
Dẫn V lít (đkc) acetylene qua dung dịch AgNO3/NH3 dư thấy thu được 60 gam kết tủa. Giá trị V là
 Xem đáp án
Xem đáp án
Chọn A
Câu 10:
Đun hai alcohol đơn chức với H2SO4 đặc, 140oC, được hỗn hợp 3 ether. Lấy 0,72 gam một trong ba ether đem đốt cháy hoàn toàn thu được 1,76 gam CO2 và 0,72 gam H2O. Hai alcohol đó là
 Xem đáp án
Xem đáp án
Chọn D
Câu 13:
Hợp chất thơm X có công thức phân tử C7H8O3. Cứ 0,1 mol X tác dụng vừa đủ với 100 mL NaOH 2 M. Mặt khác, nếu cho 0,02 mol X phản ứng với lượng dư Na thì thu được 743,7 mL H2 (ở đkc). Công thức cấu tạo của X là
 Xem đáp án
Xem đáp án
Chọn A
Câu 14:
Thực hiện phản ứng khử hợp chất carbonyl sau:
CH3COCH2CH3 + 2[H] ?
Sản phẩm thu được là
 Xem đáp án
Xem đáp án
Chọn D
Câu 16:
Trong các hợp chất dưới đây, hợp chất nào phản ứng được với HCN cho sản phẩm là cyanohydrin?
 Xem đáp án
Xem đáp án
Chọn D
Câu 17:
Cho các chất: propionic acid (X), acetic acid (Y), ethyl alcohol (Z) và dimethyl ether (T). Dãy gồm các chất được sắp xếp theo chiều tăng dần nhiệt độ sôi là
 Xem đáp án
Xem đáp án
Chọn A
Câu 18:
Acetic acid được điều chế bằng phương pháp lên men giấm từ dung dịch chất nào sau đây?
 Xem đáp án
Xem đáp án
Chọn A
Câu 19:
Alkene là những hydrocarbon mạch hở, chỉ chứa các liên kết đơn và một liên kết đôi C = C trong phân tử, có công thức chung CnH2n (n ≥ 2). Cho công thức cấu tạo một alkene sau:
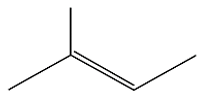
a) Công thức phân tử của alkene là: C5H10.
b) Alkene này có đồng phân hình học do có liên kết đôi.
c) Danh pháp thay thế của alkene là: 2 – methylbut – 2 – ene.
d) Ở điều kiện thường, hợp chất này ở thể khí.
 Xem đáp án
Xem đáp án
|
a |
Đ |
|
b |
S |
|
c |
Đ |
|
d |
S |
Câu 20:
Thị trường tiêu thụ phenol trên thế giới khoảng 11,37 triệu tấn trong năm 2021, dự kiến sẽ tăng lên 14,07 triệu tấn vào năm 2029. Phenol được sử dụng để sản xuất nhiều loại hóa chất như bisphenol A, nhựa phenolfomaldehyde, picric acid và các chất khác. Khoảng 90% lượng phenol được sản xuất từ cumene (bằng phương pháp cumene, chu trình cumene,…).
a) Phenol là alcohol thơm.
b) Công thức cấu tạo của phenol là: C6H5OH.
c) Cumene còn có tên gọi khác là isopropyl benzene.
d) Ngoài điều chế từ cumene, phenol còn được tách ra từ nhựa than đá.
 Xem đáp án
Xem đáp án
|
a |
S |
|
b |
Đ |
|
c |
Đ |
|
d |
Đ |
Câu 21:
Thực hiện thí nghiệm theo các bước như sau:
Bước 1: Thêm 4 mL isoamyl alcohol và 4 mL acetic acid và khoảng 2 ml H2SO4 đặc vào ống nghiệm khô. Lắc đều.
Bước 2: Đưa ống nghiệm vào nồi nước sôi từ 10 -15 phút. Sau đó lấy ra và làm lạnh.
Bước 3: Cho tiếp dung dịch NaCl bão hòa vào ống nghiệm.
a) Tại bước 2 xảy ra phản ứng ester hóa.
b) Sau bước 3, hỗn hợp chất lỏng tách thành hai lớp.
c) Sau bước 3, hỗn hợp chất lỏng thu được có mùi hoa nhài.
d) H2SO4 đặc đóng vai trò chất xúc tác và hút nước để chuyển dịch cân bằng.
 Xem đáp án
Xem đáp án
|
a |
Đ |
|
b |
Đ |
|
c |
S |
|
d |
Đ |
Câu 22:
Aspirin được sử dụng để hạ sốt và giảm đau nhẹ đến trung bình do tình trạng đau nhức cơ, răng, cảm lạnh đau đầu và sưng tấy do viêm khớp.
Aspirin có công thức cấu tạo như sau:
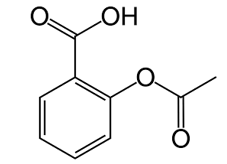
a. Aspirin là hợp chất đa chức.
b. Aspirin có 1 nhóm – OH alcohol.
c. Oxygen chiếm khoảng 35,6% khối lượng aspirin.
d. Công thức phân tử của asprin là C9H8O4.
 Xem đáp án
Xem đáp án
|
a |
S |
|
b |
S |
|
c |
Đ |
|
d |
Đ |
Câu 23:
Cho 4,32 gam acid hữu cơ X đơn chứa tác dụng hết với Na2CO3, thu được 5,64 gam muối của acid hữu cơ. Xác định công thức cấu tạo của X.
 Xem đáp án
Xem đáp án
Gọi công thức tổng quát của X là RCOOH.
2RCOOH + Na2CO3 ® 2RCOONa + CO2 + H2O
Mol: x x
Áp dụng phương pháp tăng giảm khối lượng, ta có:
(R + 44 + 23).x – (R + 45).x = 5,64 – 4,32 Þ x = 0,06
Þ R + 45 = \(\frac{{4,32}}{{0,06}}\) = 72 Þ R = 27 (C2H3-)
Vậy công thức cấu tạo của X là C2H3COOH hay CH2=CH-COOH.
Câu 24:
Tiến hành chuẩn độ acetic acid bằng dung dịch sodium hydroxide 0,15 M. Sau khi thực hiện thí nghiệm chuẩn độ này 3 lần, thu được bảng dưới đây:
|
Số lần |
Thể tích acetic acid (mL) |
Thể tích dung dịch NaOH cần dùng (mL) |
|
1 |
6,0 |
20,0 |
|
2 |
6,0 |
19,9 |
|
3 |
6,0 |
20,0 |
Nồng độ mol của acetic acid là bao nhiêu?
 Xem đáp án
Xem đáp án
Thể tích trung bình của dung dịch NaOH 3 lần đo:
\({{\rm{V}}_{{\rm{NaOH}}}}{\rm{ = }}\frac{{{\rm{20}}{\rm{,0 + 19}}{\rm{,9 + 20}}{\rm{,0}}}}{{\rm{3}}} \approx {\rm{20}}{\rm{,0 mL}}\);
Thể tích của acetic acid: \({{\rm{V}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}}{\rm{ = 6}}{\rm{,0 mL}}\);
Ta có:\[{{\rm{V}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}} \times {{\rm{C}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}} = {{\rm{V}}_{{\rm{NaOH}}}} \times {{\rm{C}}_{{\rm{NaOH}}}}\]
Nồng độ mol của acetic acid:
\[{{\rm{C}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}} = \frac{{{{\rm{V}}_{{\rm{NaOH}}}}{\rm{ \times }}{{\rm{C}}_{{\rm{NaOH}}}}}}{{{{\rm{V}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}}}} = \frac{{0,15 \times 20,0}}{{6,0}} = 0,5\]M
Câu 25:
Đun nóng một alcohol no, đơn chức X với H2SO4 đặc ở nhiệt độ thích hợp thu được chất hữu cơ Y. Tỉ khối hơi của Y so với X là 0,7. Công thức phân tử của X là gì?
 Xem đáp án
Xem đáp án
Vì \[{d_{{\raise0.7ex\hbox{$Y$} \!\mathord{\left/
{\vphantom {Y X}}\right.\kern-\nulldelimiterspace}
\!\lower0.7ex\hbox{$X$}}}}\; = {\rm{ }}0,7 < 1\; \to Y{\rm{ }}l\`a {\rm{ }}alkene.\]
\[{d_{{\raise0.7ex\hbox{$Y$} \!\mathord{\left/
{\vphantom {Y X}}\right.\kern-\nulldelimiterspace}
\!\lower0.7ex\hbox{$X$}}}}\; = \;\frac{{14n}}{{14n + 18}} = 0,7 \Rightarrow n = 3\]
Công thức phân tử của X là C3H8O.
Câu 26:
Sản phẩm chính theo quy tắc Zaitsev của phản ứng tách HCl ra khỏi phân tử 2-chloro-3-methyl butane là gì?
 Xem đáp án
Xem đáp án
Câu 27:
Tiến hành thí nghiệm phản ứng tráng bạc bằng cách lấy 50 mL dung dịch CH3CHO 1M phản ứng với thuốc thử Tollens dư. Sau khi kết thúc phản ứng, bình phản ứng có một lớp bạc sáng bóng bám vào thành bình. Loại bỏ hóa chất trong bình rồi tráng bằng nước cất, sấy khô, khối lượng bình tăng m gam so với ban đầu. Giá trị của m là bao nhiêu? Biết hiệu suất tráng bạc là 75% vào chỉ 60% lượng bạc tạo thành bám vào thành bình, phần còn lại ở dạng kết tủa bột màu đen.
 Xem đáp án
Xem đáp án
CH3CHO + 2[Ag(NH3)2]OH CH3COONH4 +2Ag + 3NH3 + H2O
\({n_{C{H_3}CHO}}\) = 50 . 10-3 = 0,05 mol.
\({n_{Ag}}\) = 0,05 . 2 = 0,1 \( \Rightarrow \)mAg sinh ra theo lí thuyết = 108 . 0,1 = 10,8 (g).
\[ \Rightarrow \]Khối lượng Ag bám vào thành bình là: m = 10,8 . 75% . 60% = 4,86 (g).
Câu 28:
Gas, nhiên liệu phổ biến hiện nay có thành phần chính là propane và butane. Nhiệt lượng giải phóng khi đốt cháy hoàn toàn 1 kg một loại gas là khoảng 50 400 kJ. Biết để làm nóng 1 kg nước lên 1 độ thì cần cung cấp nhiệt lượng là 4 200 J. Để đun sôi 30 kg nước từ nhiệt độ 20oC cần cung cấp bao nhiêu kJ nhiệt?
 Xem đáp án
Xem đáp án
Để đun sôi 30 kg nước từ nhiệt độ 20oC, cần cung cấp nhiệt lượng là:
\(\frac{{4200 \times 30 \times (100 - 20)}}{{1000}} = 10080\)kJ.