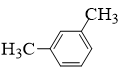
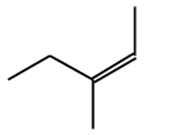
Đề kiểm tra giữa học kì 2 Hóa 11 CTST có đáp án (Đề 1)
-
64 lượt thi
-
31 câu hỏi
-
60 phút
Danh sách câu hỏi
Câu 1:
Bề mặt những vũng đầm lầy thường xuất hiện các bong bóng khí, đó là alkane đơn giản nhất, có tên gọi là
 Xem đáp án
Xem đáp án
Chọn D
Câu 4:
Quá trình “bẻ gãy” các phân tử alkane mạch dài thành những hydrocarbon mạch ngắn hơn được gọi là
 Xem đáp án
Xem đáp án
Chọn A
Câu 7:
Nếu muốn phản ứng: CH≡CH + H2 dừng lại ở giai đoạn tạo thành ethylene thì cần sử dụng xúc tác nào dưới đây?
 Xem đáp án
Xem đáp án
Chọn B
Câu 9:
Khi cho acetylene phản ứng với lượng dư AgNO3/NH3 tới khi phản ứng xảy ra hoàn toàn, thu được sản phẩm hữu cơ là
 Xem đáp án
Xem đáp án
Chọn C
Câu 13:
Benzene có thể phản ứng với bromine khan khi có mặt xúc tác FeBr3. Phản ứng này thuộc loại phản ứng nào?
 Xem đáp án
Xem đáp án
Chọn A
Câu 14:
Mỗi nguyên tử halogen trong phân tử dẫn xuất halogen của hydrocarbon tạo được bao nhiêu liên kết?
 Xem đáp án
Xem đáp án
Chọn A
Câu 15:
Tên gọi theo danh pháp thay thế của dẫn xuất halogen có công thức cấu tạo CH3 – CHCl – CH3 là
 Xem đáp án
Xem đáp án
Chọn B
Câu 16:
Cho các dẫn xuất halogen sau: (1) C2H5F; (2) C2H5Cl; (3) C2H5Br; (4) C2H5I. Thứ tự giảm dần của nhiệt độ sôi là
 Xem đáp án
Xem đáp án
Chọn C
Câu 17:
Phần trăm khối lượng hydrogen trong alkane X là 25,00 %. Công thức phân tử của X là
 Xem đáp án
Xem đáp án
Chọn A
Câu 18:
Khi cho 2,2-dimethylbutane tác dụng với chlorine thu được tối đa bao nhiêu dẫn xuất monochloro?
 Xem đáp án
Xem đáp án
Chọn A
Câu 19:
Đồng phân cấu tạo nào của alkane có công thức phân tử C6H14 tạo ra nhiều sản phẩm thế nhất khi phản ứng với chlorine (tỉ lệ mol 1:1), chiếu sáng?
 Xem đáp án
Xem đáp án
Chọn A
Câu 20:
Ứng với công thức phân tử C5H8 có bao nhiêu alkyne là đồng phân cấu tạo của nhau
 Xem đáp án
Xem đáp án
Chọn A
Câu 23:
Thực hiện thí nghiệm như hình vẽ bên. Kết thúc thí nghiệm, trong bình đựng dung dịch AgNO3 trong NH3 xuất hiện kết tủa màu vàng nhạt.
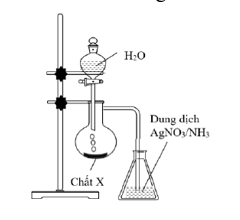
Chất X là
 Xem đáp án
Xem đáp án
Chọn C
Câu 24:
Đun nóng hydrocarbon thơm X có công thức phân tử C8H10 với dung dịch KMnO4 nóng thu được dung dịch X có chứa C6H5COOK và K2CO3. Chất X là
 Xem đáp án
Xem đáp án
Chọn C
Câu 26:
Ở điều kiện thích hợp (nhiệt độ, áp suất, chất xúc tác), benzene tác dụng được với tất cả các chất trong dãy nào dưới đây?
 Xem đáp án
Xem đáp án
Chọn D
Câu 27:
Nhiệt độ sôi của các dẫn xuất halogen được sắp xếp theo thứ tự: CH3F < CH3CI < CH3Br < CH3I. Nguyên nhân dẫn đến sự tăng dần nhiệt độ sôi từ CH3F đến CH3I là do
 Xem đáp án
Xem đáp án
Chọn C
Câu 28:
Cho vài giọt brombenzene vào ống nghiệm có chứa sẵn nước, lắc nhẹ rồi để yên trong vài phút. Phát biểu nào sau đây là đúng?
 Xem đáp án
Xem đáp án
Chọn A
Câu 29:
Hợp chất A là dẫn xuất monochloro của alkylbenzene (B). Phân tử khối của A bằng 126,5.
(a) Tìm công thức phân tử và viết công thức cấu tạo có thể có của A.
(b) Chất A có phản ứng thủy phân khi đun nóng với dung dịch NaOH, tạo ra chất E có mùi thơm, có khả năng hòa tan nhiều chất hữu cơ, ức chế sự sinh sản của vi khuẩn nên được dùng nhiều trong công nghiệp sản xuất mĩ phẩm. Tìm công thức cấu tạo đúng của A. Viết phương trình hóa học.
 Xem đáp án
Xem đáp án
(a) A là dẫn xuất monochloro của alkylbenzene nên công thức phân tử của A có dạng CnH2n-7Cl.
Theo bài ra: 12n + 2n – 7 + 35,5 = 126,5 Þ n = 7.
Công thức phân tử của A là C7H7Cl.
Các công thức cấu tạo có thể có của A là:
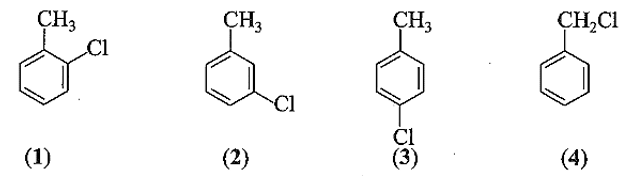
(b) Chất A có phản ứng thủy phân khi đun nóng với dung dịch NaOH nên công thức cấu tạo phù hợp với A là (4). Phương trình hoá học:
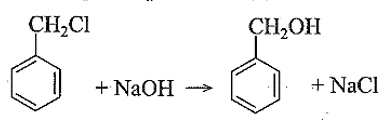
Câu 30:
a. Viết các phương trình phản ứng minh hoạ các quá trình điều chế polystyrene từ hexane.
b. Vì sao khu vực trạm xăng dầu, khu vực có nhiều xe cơ giới qua lại, nơi có khói thuốc lá …lại được xem là nơi có nguồn hydrocarbon thơm gây tổn hại đến sức khoẻ con người?
 Xem đáp án
Xem đáp án
a. Điều chế polystyrene từ hexane:
C6H14 C6H6 + 4H2
C6H6 + CH2=CH2 C6H5CH2CH3
C6H5CH2CH3 C6H5CH=CH2 + H2
nC6H5CH=CH2
b. Khu vực có trạm xăng dầu, khu vực có nhiều xe cơ giới qua lại, nơi có khói thuốc lá,... là nơi có nguồn hydrocarbon thơm, đây là các chất độc gây tổn hại đến sức khoẻ con người. Trong xăng tồn tại benzene (C6H6); trong thuốc lá tồn tại nicotine (là hợp chất chứa vòng benzene) rất độc.
Câu 31:
Một bình gas (khí hóa lỏng) sử dụng trong hộ gia đình X chứa 12 kg hỗn hợp propane và butane với tỉ lệ mol 1 : 2. Khi đốt cháy hoàn toàn, 1 mol propane tỏa ra lượng nhiệt là 2 220 kJ và 1 mol butane tỏa ra lượng nhiệt là 2 850 kJ. Trung bình, lượng nhiệt tiêu thụ từ đốt khí gas của hộ gia đình X là 11 000 kJ/ngày và hiệu suất sử dụng nhiệt là 80%.
(a) Tính tổng lượng nhiệt tỏa ra khi đốt cháy hoàn toàn 12 kg gas trên.
(b) Tính số ngày hộ gia đình X sử dụng hết bình gas trên.
 Xem đáp án
Xem đáp án
(a) Gọi số mol C3H8 là a (mol) và số mol C4H10 là 2a (mol), ta có:
44a + 58.2a = 12.1000 Þ a = 75 mol
Nhiệt tỏa ta khi đốt cháy 12 kg gas trên là Q = 75.2220 + 150.2850 = 594 000 (kJ).
(b) Vì H = 80% \[ \Rightarrow \] nhiệt sử dụng thực tế là 594000.80% = 475 200 kJ.
Số ngày sử dụng hết bình gas = \(\frac{{475200}}{{11000}} \approx 43\) (ngày).