Đề thi cuối kì 1 Hóa 11 CTST cấu trúc mới có đáp án (Đề 1)
-
145 lượt thi
-
28 câu hỏi
-
60 phút
Danh sách câu hỏi
Câu 2:
Điền vào chỗ trống “....” trong câu sau bằng cụm từ thích hợp: “Cân bằng hóa học là trạng thái của phản ứng thuận nghịch khi tốc độ phản ứng thuận ........ tốc độ phản ứng nghịch”.
 Xem đáp án
Xem đáp án
Chọn B
Câu 4:
Cho hình vẽ về cách thu khí dời nước như sau:
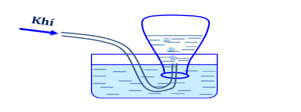
Hình vẽ trên có thể áp dụng để thu được khí nào trong các khí sau đây?
 Xem đáp án
Xem đáp án
Chọn A
Câu 8:
Chất nào sau đây được dùng làm chất phụ gia để làm đông các sản phẩm như đậu hũ, đậu non…?
 Xem đáp án
Xem đáp án
Chọn B
Câu 12:
Hydrocarbon là loại hợp chất hữu cơ mà thành phần phân tử có các nguyên tố nào sau đây?
 Xem đáp án
Xem đáp án
Chọn A
Câu 13:
Xét cân bằng : Fe2O3 (s) + 3CO (g) 2Fe (s) + 3CO2 (g)
Biểu thức hằng số cân bằng của hệ là
 Xem đáp án
Xem đáp án
Chọn D
Câu 15:
Mưa acid là hiện tượng nước mưa có pH thấp hơn 5,6 (giá trị pH của khí carbon dioxide bão hoà trong nước). Chất khí nào sau đây không phải là nguyên nhân chính gây nên hiện tượng mưa acid?
 Xem đáp án
Xem đáp án
Chọn D
Câu 17:
Cho hỗn hợp các alkane có mạch carbon thẳng sau: pentane (sôi ở 36 °C), heptane (sôi ở 98 °C), octane (sôi ở 126 °C) và nonane (sôi ở 151 °C). Có thể tách riêng các chất đó bằng cách nào sau đây?
 Xem đáp án
Xem đáp án
Chọn D
Câu 19:
Cho các hiện tượng quan sát được trong các thí nghiệm sau:
a). Cho dung dịch H2SO4 loãng tiếp xúc với lá kẽm (zinc) bị phủ bởi lớp zinc oxide thấy lớp oxide tan dần sau đó kim loại tan và có bọt khí xuất hiện.
b). Cho dung dịch H2SO4 loãng tiếp xúc với mẩu đá vôi thấy có khí không màu thoát ra, dung dịch thu được có màu xanh lam.
c). Cho dung dịch H2SO4 loãng tiếp xúc bột baking soda thấy bột baking soda tan ra, dung dịch sủi bọt khí, dung dịch thu được không màu.
d). Cho dung dịch H2SO4 loãng vào nước vôi trong Ca(OH)2 thấy nước vôi trong bị vẩn đục.
 Xem đáp án
Xem đáp án
|
a |
S |
|
b |
S |
|
c |
Đ |
|
d |
Đ |
Câu 20:
Cho phương trình hóa học tổng hợp ammonia từ nitrogen và hydrogen bằng quá trình Haber như sau:
a). Do ammonia dễ hoá lỏng hơn nên khi làm lạnh hỗn hợp sẽ tách được ammonia lỏng ra khỏi hỗn hợp khí.
b). Phản ứng trên là phản ứng thuận nghịch nên tại thời điểm cân bằng, hỗn hợp trong buồng phản ứng gồm ammonia, nitrogen và hydrogen.
c). Nếu không sử dụng chất xúc tác thì không thể tạo thành ammonia.
d). Nếu giảm áp suất của hệ thì phản ứng sẽ chuyển dịch theo chiều thuận.
 Xem đáp án
Xem đáp án
|
a |
Đ |
|
b |
Đ |
|
c |
S |
|
d |
S |
Câu 21:
Cho các phát biểu sau:
a). HCHO và C6H12O6 có cùng công thức đơn giản nhất.
b). CH3OH và CH3CH2OH là đồng đẳng của nhau.
c). CH3OCH3 và CH3CH2OH đều là dẫn xuất của hydrocarbon.
d). C6H5OH và C2H5OH là đồng phân của nhau.
 Xem đáp án
Xem đáp án
|
a |
Đ |
|
b |
Đ |
|
c |
S |
|
d |
S |
Câu 22:
Cho dãy chất: CH4; C6H6; C6H5-OH; C2H5ZnI; C2H5PH2.
a). Các chất trong dãy đều là hydrocarbon
b). Có 2 chất là hydrocarbon.
c). Các chất trong dãy đều là hợp chất hữu cơ.
d). Có 3 hợp chất vô cơ và 2 hợp chất hữu cơ.
 Xem đáp án
Xem đáp án
|
a |
S |
|
b |
Đ |
|
c |
Đ |
|
d |
S |
Câu 23:
pH của dung dịch KOH 0,004M có giá trị là? (làm tròn kết quả đến hàng phần mười)
 Xem đáp án
Xem đáp án
pH = 14 + log [OH-] = 11,6.
Câu 25:
Dẫn khí SO2 vào 200 mL dung dịch KMnO4 0,02 M đến khi mất màu tím theo sơ đồ phản ứng:
Thể tích khí SO2 (đkc) mL đã phản ứng là? (kết quả làm tròn đến hàng đơn vị).
 Xem đáp án
Xem đáp án
Vkhí = 0,01.24,79 = 0,2479 lít = 248 mL.
Câu 26:
Kết quả phân tích nguyên tố cho thấy thành phần phần trăm khối lượng các nguyên tố có trong hợp chất X như sau: carbon là 52,17%; hydrogen là 13,04%; còn lại là oxygen. Nghiên cứu cũng xác định được phân tử khối của chất X này là 46. Tổng số nguyên tử có trong 1 phân tử X là?
 Xem đáp án
Xem đáp án
%O = 100% - %C - %H = 100% - 52,17% - 13,04% = 34,79%.
Đặt công thức đơn giản nhất của hợp chất X là: CxHyOz. Ta có:
x : y : z =
= 4,3475 : 13,04 : 2,17 = 2 : 6 : 1.
Vậy công thức đơn giản nhất của X là: C2H6O.
Þ Công thức phân tử của X có dạng: (C2H6O)n.
Phân tử khối của X là 46 nên (12.2 + 6 + 16).n = 46 Þ n = 1.
Vậy công thức phân tử của X là: C2H6O.
Tổng số nguyên tử có trong X là: 2 + 6 + 1 = 9.
Câu 27:
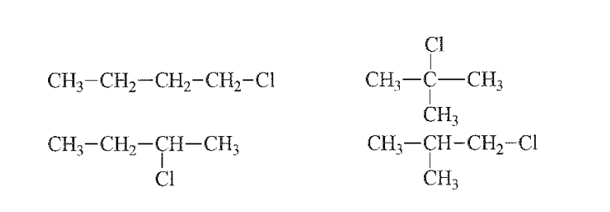
Số đồng phân cấu tạo có thể có của hợp chất có công thức phân tử C4H9Cl là?
 Xem đáp án
Xem đáp án
C4H9Cl có đồng phân cấu tạo về mạch carbon và vị trí nhóm thế (nhóm –Cl) trên mạch.
Câu 28:
Thực hiện phản ứng tổng hợp ammonia từ và với hiệu suất h%, thu được hỗn hợp X chứa 10% (về thể tích). Cho X tác dụng với CuO dư, nung nóng. Sau khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp Y (gồm khí và hơi) và hỗn hợp rắn Z có khối lượng giảm đi so với khối lượng CuO ban đầu là 12,8 gam. Làm lạnh Y, còn 7,437 lít khí (đkc) không bị ngưng tụ. Giá trị của h là?
 Xem đáp án
Xem đáp án
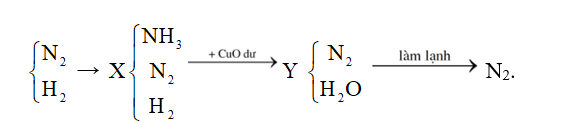
Sau khi ngưng tụ còn lại khí N2 ⟹ = 0,3 mol = (ban đầu).
N2 + 3H2 ⇌ 2NH3
3CuO + 2NH3 3Cu + N2 + 3H2O
CuO + H2 Cu + H2O
mchất rắn giảm = mO phản ứng = 12,8 gam ⟹ nO phản ứng = 0,8 mol.
Bảo toàn electron toàn bộ quá trình: (ban đầu) = 2nO phản ứng ⟹ (ban đầu) = 0,8 (mol).
Ta thấy: ⟹ Hiệu suất tính theo H2.
N2 + 3H2 ⇌ 2NH3
Ban đầu: 0,3 0,8 (mol)
Phản ứng: x 3x 2x (mol)
Sau: (0,3 − x) (0,8 − 3x) 2x (mol)
⟹ nSau = (0,3 − x) + (0,8 − 3x) + 2x = 1,1 − 2x (mol)
Mà = 10% ⟹ = 1,1 ⟹ x = 0,05.
