Đề kiểm tra Hóa 11 GK1 THPT chuyên Lê Quý Đôn - Đà Nẵng
-
1460 lượt thi
-
30 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
Chất nào sau đây là muối axit?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
NaHSO4 là muối axit (muối mà gốc axit vẫn còn H có khả năng phân li ra H+).
NaHSO4 → Na+ + HSO4-
HSO4- → H+ + SO42-
Chú ý: Một cách gần đúng, coi HSO4- phân li hoàn toàn.
Câu 2:
Xét các phát biểu sau về N₂
a) Trong phòng thí nghiệm khí N₂ được thu bằng phương pháp đẩy nước.
b) Phân tử N₂ có liên kết 3 rất bền.
c) N₂ không duy trì sự cháy và sự hô hấp.
d) Ở điều kiện thường, N₂ khá trơ về mặt hóa học.
e) N₂ có nhiệt độ hóa lỏng thấp hơn O₂.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Cả 5 phát biểu đều đúng.
Câu 3:
Hình bên là nitơ lỏng.

Ứng dụng của nitơ lỏng là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Ứng dụng của nitơ lỏng là bảo quản máu.
Câu 4:
Cho dãy các chất sau: Al(OH)₃, NaHCO₃, (NH₄)₂CO₃, NH₄Cl, CaCO₃, K₂SO₄. Có bao nhiêu chất trong dãy vừa tác dụng được với dung dịch HCl, vừa tác dụng được với dung dịch NaOH?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Những chất vừa tác dụng được với dung dịch HCl, vừa tác dụng được với dung dịch NaOH là Al(OH)3, NaHCO3, (NH4)2CO3
Câu 5:
100 mL dung dịch Ba(OH)₂ nồng độ 0,05M có pH bằng
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
pH = 14 + log(0,05. 2) = 13
Câu 6:
Ở 25⁰C, tích số ion nước có giá trị bằng?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Ở 250C, tích số ion nước có giá trị bằng 10-14.
Câu 7:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
pH = 13 → [OH-] = 0,1M
→ OH- còn dư → quỳ tím chuyển sang màu xanh.
Câu 8:
Phát biểu nào sau đây về khí amoniac KHÔNG đúng?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Khí amoniac tan nhiều trong nước.
Câu 9:
Nitơ là nguyên tố thuộc chu kì II, nhóm VA trong bảng HTTH. Cấu hình electron lớp ngoài cùng của nguyên tử N là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Cấu hình electron của nitơ là 1s22s22p3.
Câu 10:
Khí nitơ tác dụng với khí oxi (tia lửa điện) sinh ra khí không màu là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Câu 11:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Khí X là NO2. Khí NO2 là một trong các nguyên nhân gây nên ô nhiễm không khí.
Câu 12:
Trong phòng thí nghiệm, khí NH₃ được điều chế bằng cách
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Trong phòng thí nghiệm, khí NH3 được điều chế bằng cách đun nóng muối amoni với dung dịch bazơ.
2NH4Cl + Ca(OH)2 2NH3↑ + CaCl2 + 2H2O
Câu 13:
Vào tháng 8 năm 2020, hai vụ nổ xảy ra tại bến cảng của thành phố Beirut, thủ đô Liban gây ra rất nhiều thiệt hại. Nguyên nhân của vụ nổ là 2750 tấn phân bón amoni nitrat, bị tịch thu từ con tàu bỏ hoang MV Rhosus và được cất giữ tại cảng suốt sáu năm mà không có biện pháp phòng ngừa nào. Công thức amoni nitrat là

 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Công thức của amoni nitrat là NH4NO3
Câu 14:
Phương trình điện li nào sau đây đúng?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Phương trình điện ly đúng là
A sai, sửa lại: KNO3 → K+ + NO3-
C sai, vì HClO là chất điện li yếu.
D sai, vì NaF là chất điện li mạnh.
Câu 15:
Trong dãy các chất sau: NaHCO₃, K₂HPO₄, NaHSO₄,Ca(HSO₃)₂, Na₂SO₃. Số chất là muối axit bằng?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Muối axit là muối mà gốc axit vẫn còn hiđro có thể phân li ra H+.
Các chất là muối axit là: NaHCO3, K2HPO4, NaHSO4, Ca(HSO3)2
Câu 16:
Dung dịch axit nitric khi có ánh sáng bị phân hủy một phần giải phóng khí
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Câu 17:
Chỉ số pH bình thường của dạ dày là từ 1,6 đến 2,4. Môi trường trong dạ dày là môi trường gì?
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Môi trường axit có pH < 7.
Môi trường trong dạ dày là môi trường axit
Câu 18:
Dùng axit nitric dư để hòa tan hoàn toàn 16 gam hỗn hợp Mg, Fe (tỉ lệ mol 1:1), thu được dung dịch Y (chỉ chứa hai muối và axit dư) và V lít (đktc) hỗn hợp khí X (gồm NO và N₂O). Tỉ khối của X đối với H₂ bằng 16,4. Giá trị của V là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Ta có: 24nMg + 56nFe = 16
Mà nMg = nFe
→ nMg = nFe = 0,2 mol
Gọi số mol khí NO và N2O lần lượt là x và y
→ V = 5,6 lít
Câu 19:
Chất nào sau đây là hiđroxit lưỡng tính?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Zn(OH)2 là hiđroxit lưỡng tính.
Câu 20:
Cho dung dịch Ba(NO₃)₂ tác dụng vừa đủ với 100 mL dung dịch Na₂SO₄ 0,5 M. Khối lượng kết tủa thu được bằng
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Ba(NO3)2 + Na2SO4 → BaSO4↓ + 2NaNO3
Theo phương trình:
Câu 21:
Cho 25ml dung dịch (NH₄)₂SO₄ 1 M tác dụng với lượng dư NaOH. Thể tích khí NH₃ (đktc) thu được bằng
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
(NH4)2SO4 + 2NaOH → 2NH3 + Na2SO4 + 2H2O
Theo phương trình:
lít
Câu 22:
Nhỏ từ từ đến dư dung dịch NaOH loãng vào mỗi dung dịch sau: Ba(HCO₃)₂, FeCl₃, CuCl₂, AlCl₃, Mg(NO₃)₂. Sau khi các phản ứng xảy ra hoàn toàn, số trường hợp thu được kết tủa là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Các chất phản ứng sinh ra kết tủa là: Ba(HCO3)2 FeCl3, CuCl2, Mg(NO3)2.
Loại AlCl3 vì:
AlCl3 + 3NaOH → Al(OH)3↓ + 3NaCl
Al(OH)3 + NaOH dư → NaAlO2 + 2H2O
Câu 23:
Cho từng chất: Fe, CuO, Cu(OH)₂, Fe(OH)₃, Fe₃O₄, Fe₂O₃, Fe(NO₃)₂, Fe(NO₃)₃, CuS, Fe₂(SO₄)₃, FeCO₃ lần lượt phản ứng với dung dịch HNO₃ đặc, nóng. Số trường hợp xảy ra phản ứng oxi hoá – khử là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Các chất phản ứng với HNO3 đặc, nóng xảy ra phản ứng oxi hóa – khử là: Fe, Fe3O4, Fe(NO3)2, CuS, FeCO3
Câu 24:
Xét các phản ứng dưới đây:
a) NH₃ + H₂O + NaHCO₃.
b) NaHCO₃ + NaOH.
c) KHCO₃ + NH₄HSO₄.
d) Ca(HCO₃)₂ + Ca(OH)₂.
e) NaHCO₃ + Ba(OH)₂
Số phản ứng có phương trình ion thu gọn HCO₃⁻ + OH⁻ → H₂O + CO₃²⁻ là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Các phản ứng có phương trình ion thu gọn HCO₃⁻ + OH⁻ → H₂O + CO₃²⁻ là: (b)
Câu 25:
Các dung dịch sau đây có cùng nồng độ mol/L, dung dịch nào dẫn điện tốt nhất?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Loại A vì glucozơ là dung dịch không điện li.
Loại C vì NH3 dẫn điện kém.
Xét 2 chất điện li mạnh: Na2SO4 và K3PO4, do có cùng nồng độ mol nên dung dịch nào phân li ra nhiều ion hơn sẽ dẫn điện tốt hơn.
Vậy dung dịch K3PO4 dẫn điện tốt nhất.
Câu 26:
Chất nào sau đây là chất điện li mạnh?
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
NaF là chất điện ly mạnh.
NaF → Na+ + F-.
Câu 27:
Xét các phản ứng dưới đây
a) 4NH₃ + 5O₂ → 4NO + 6H₂O (t⁰ cao, xúc tác Pt)
b) NH₃ + HCl → NH₄Cl
c) 8NH₃ + 3Cl₂ → N₂ + 6NH₄Cl
d) 4NH₃ + 3O₂ → 2N₂ + 6H₂O (t⁰)
Số phản ứng mà NH₃ KHÔNG thể hiện tính khử là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Các phản ứng mà NH3 không thể hiện tính khử là: (b)
Do ở phản ứng này, số oxi hóa của N không thay đổi sau phản ứng.
Câu 28:
Hòa tan 35,2 gam Fe₂O₃ vào dd HNO₃ loãng, dư thu được m gam muối nitrat. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Bảo toàn nguyên tố Fe:
→ m = 106,48 gam
Câu 29:
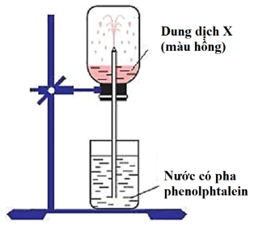
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Dung dịch phun lên thành tia màu hồng, chứng tỏ dung dịch X có môi trường bazơ.
Thí nghiệm chứng minh tính bazơ và tan nhiều trong nước của NH3.
Câu 30:
Cho các phản ứng sau:
(a) FeS + 2HCl → FeCl₂ + H₂S;
(b) Na₂S + 2HCl → 2NaCl + H₂S;
(c) 2AlCl₃ + 3Na₂S + 6H₂O → 2Al(OH)₃ + 3H₂S + 6NaCl;
(d) KHSO₄ + KHS → K₂SO₄ + H₂S;
(e) BaS + H₂SO₄ (loãng) → BaSO₄ + H₂S.
Số phản ứng có phương trình ion rút gọn S²⁻ + 2H⁺ → H₂S là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Phản ứng có phương trình ion rút gọn S²⁻ + 2H⁺ → H₂S là: (b).
