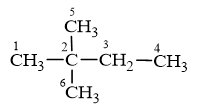
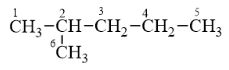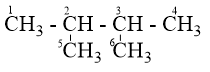Phản ứng thế và phản ứng oxi hóa ankan
-
1279 lượt thi
-
25 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
Sản phẩm của phản ứng thế clo (1:1, ánh sáng) vào 2,2-đimetylpropan là :
(1) (CH3)3CCH2Cl (2) CH3C(CH2Cl)2CH3 (3) CH3ClC(CH3)3
 Xem đáp án
Xem đáp án
2,2-đimetylpropan: (CH3)3C-CH3=>chỉ có 1 vị trí thế Cl
(CH3)3C-CH3+ Cl2→ (CH3)3C-CH2Cl + HCl
Đáp án cần chọn là: D
Câu 2:
Cho neo-pentan tác dụng với Cl2theo tỉ lệ số mol 1 : 1, số sản phẩm monoclo tối đa thu được là :
 Xem đáp án
Xem đáp án
Neo-pentan:
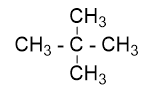
=>4 vị trí nhóm CH3là như nhau =>thế monoclo thu được 1 sản phẩm duy nhất
Đáp án cần chọn là: D
Câu 3:
Khi clo hóa C5H12với tỉ lệ mol 1:1 thu được 3 sản phẩm thế monoclo. Danh pháp IUPAC của ankan đó là
 Xem đáp án
Xem đáp án
C5H12có 3 đồng phân:
\[\mathop C\limits^1 \,{H_3} - \mathop C\limits^2 \,{H_2} - \mathop C\limits^3 \,{H_2} - C{H_2} - C{H_3}\]: có 3 vị trí thế Clo (1, 2, 3), vị trí C4 giống C2 và C5 giống C1
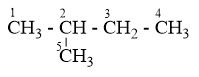
có 4 vị trí thế Clo (1, 2, 3, 4), vị trí C5 giống C1
(CH3)3C – CH3: chỉ có 1 vị trí thế Clo vì 4 nhóm CH3đều giống nhau
Đáp án cần chọn là: C
Câu 4:
khi clo hóa một ankan có công thức phân tử C6H14, người ta chỉ thu được 2 sản phẩm thế monoclo. Danh pháp IUPAC của ankan đó là :
 Xem đáp án
Xem đáp án
2,2-đimetylbutan:
| Có 3 vị trí thế clo (C1, C3, C4) vì vị trí C1, C5, C6 là giống nhau và vị trí C2 không có H |
2-metylpentan
| Có 5 vị trí thế Cl (C1, C2, C3, C4, C5) vì vị trí C1và C6là giống nhau |
n-hexan \[\mathop C\limits^1 \,{H_3} - \mathop C\limits^2 \,{H_2} - \mathop C\limits^3 \,{H_2} - C{H_2} - C{H_2} - C{H_3}\] | Có 3 vị trí thế clo (C1, C2, C3) |
2,3-đimetylbutan
| Có 2 vị trí thế clo (C1 và C2) vì C2 và C3 giống nhau; C1, C4, C5, C6 giống nhau |
Đáp án cần chọn là: D
Câu 5:
Hiđrocacbon mạch hở X trong phân tử chỉ chứa liên kết σ và có hai nguyên tử cacbon bậc ba trong một phân tử. Đốt cháy hoàn toàn 1 thể tích X sinh ra 6 thể tích CO2(ở cùng điều kiện nhiệt độ, áp suất). Khi cho X tác dụng với Cl2(theo tỉ lệ số mol 1 : 1), số dẫn xuất monoclo tối đa sinh ra là :
 Xem đáp án
Xem đáp án
- Đốt cháy 1 thể tích X sinh ra 6 thể tích CO2=>trong X có 6 nguyên tử C
- Vì X chỉ chứa liên kết σ và có hai nguyên tử cacbon bậc ba trong một phân tử
=>X là ankan C6H14có công thức phân tử là (CH3)2- CH – CH(CH3)2
=>có 2 vị trí thế monoclo
Đáp án cần chọn là: C
Câu 6:
Ankan Y phản ứng với clo tạo ra 2 dẫn xuất monoclo có tỉ khối hơi so với H2bằng 46,25. Tên của Y là :
 Xem đáp án
Xem đáp án
Đặt CTPT của ankan là CnH2n+2
Phản ứng của CnH2n+2 với clo tạo ra dẫn xuất monoclo :
\[{C_n}{H_{2n + 2}} + C{l_2}\mathop \to \limits^{{\rm{as}}} {C_n}{H_{2n + 1}}Cl + HCl\] (1)
Theo giả thiết ta thấy CnH2n+1Cl gồm hai đồng phân và
\[{M_{{C_n}{H_{2n + 1}}Cl}} = 46,25.2 = 92,5\,\,gam/mol\]
=>14n + 36,5 = 92,5 =>n = 4 =>CTPT của ankan là C4H10
+) Vì phản ứng tạo 2 dẫn xuất =>X là butan hoặc isobutan
Phương trình phản ứng :
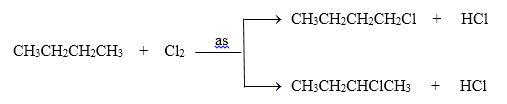
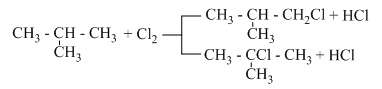
Đáp án cần chọn là: D
Câu 7:
Khi clo hóa một ankan X chỉ thu được một dẫn xuất monoclo duy nhất có tỉ khối hơi đối với hiđro là 53,25. Tên của ankan X là :
 Xem đáp án
Xem đáp án
Đặt CTPT của ankan là CnH2n+2
Phản ứng của CnH2n+2 với clo tạo ra dẫn xuất monoclo :
\(\) \[{C_n}{H_{2n + 2}}\,\,\,\,\, + \,\,\,\,\,\,C{l_2}\,\,\mathop \to \limits^{{\rm{as}}} \,\,\,{C_n}{H_{2n + 1}}Cl\,\,\,\,\, + \,\,\,\,\,HCl\] (1)
Theo giả thiết \[{M_{{C_n}{H_{2n + 1}}Cl}} = 53,25.2 = 106,5\,\]
=>14n + 36,5 = 106,5 =>n = 5
=>CTPT của ankan là C5H12
Vì phản ứng chỉ tạo ra một sản phẩm duy nhất nên ankan X là 2,2-đimetylpropan.
Phương trình phản ứng :
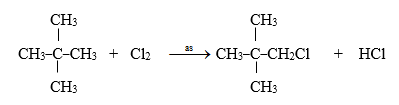
Đáp án cần chọn là: C
Câu 8:
Khi cho ankan X (trong phân tử có phần trăm khối lượng cacbon bằng 83,72%) tác dụng với clo theo tỉ lệ số mol 1:1 (trong điều kiện chiếu sáng) chỉ thu được 2 dẫn xuất monoclo đồng phân của nhau. Tên của X là :
 Xem đáp án
Xem đáp án
Đặt CTPT của ankan X là CnH2n+2. Theo giả thiết ta có :
\[\frac{{12n}}{{2n + 2}} = \frac{{83,72}}{{16,28}} \Rightarrow n = 6\]
=>CTPT của ankan X là C6H14
Vì X phản ứng với Cl2theo tỉ lệ mol 1:1 chỉ thu được hai sản phẩm thế monoclo nên X có tên là 2,3-đimetylbutan. Phương trình phản ứng :
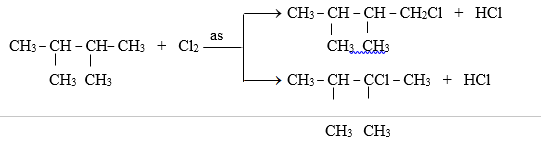
Đáp án cần chọn là: B
Câu 9:
Khi tiến hành phản ứng thế giữa ankan X với hơi brom có chiếu sáng người ta thu được hỗn hợp Y chỉ chứa hai chất sản phẩm. Tỉ khối hơi của Y so với không khí bằng 4. Tên của X là :
 Xem đáp án
Xem đáp án
Đặt CTPT của ankan là CnH2n+2.
Phản ứng của CnH2n+2 với brom tạo ra hai chất sản phẩm :
\[{C_n}{H_{2n + 2}} + xB{r_2}\mathop \to \limits^{{\rm{as}}} {C_n}{H_{2n + 2 - x}}B{r_x} + xHBr\]
mol: 1 1 x
Hỗn hợp Y gồm hai chất là : CnH2n+2-xBrxvà HBr
Theo giả thiết và (1) ta có
\[\frac{{1.(14n + 2 + 79x) + 81x}}{{1 + x}} = 4.29 \Rightarrow 14n + 44x = 114 \Rightarrow \left\{ {\begin{array}{*{20}{c}}{n = 5}\\{x = 1}\end{array}} \right.\]
Vì phản ứng chỉ tạo ra 2 sản phẩm nên suy ra chỉ có một sản phẩm thế duy nhất =>X là 2,2-đimetylpropan
Phương trình phản ứng :
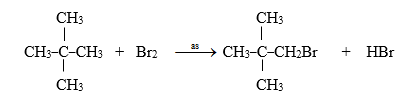
Đáp án cần chọn là: A
Câu 10:
Ankan X là chất khí ở điều kiện thường. X phản ứng với clo (có askt) tạo 2 dẫn xuất monoclo. Có bao nhiêu chất thỏa mãn điều kiện trên ?
 Xem đáp án
Xem đáp án
Ankan X là chất khí ở điều kiện thường nên số nguyên tử C ≤ 4
→ X phản ứng với clo tạo ra 2 dẫn xuất monoclo
→ X có thể có các công thức cấu tạo:
CH3-CH2-CH3
CH3-CH2-CH2-CH3
(CH3)3CH
Vậy có 3 chất thỏa mãn điều kiện trên.
Đáp án cần chọn là: B
Câu 11:
Ankan X có một nguyên tử cacbon bậc III, một nguyên tử cacbon bậc II, còn lại là các nguyên tử cacbon bậc I. Khi cho X tác dụng với clo (askt) thu được bao nhiêu dẫn xuất monoclo là đồng phân cấu tạo của nhau ?
 Xem đáp án
Xem đáp án
Ankan X có một nguyên tử cacbon bậc III, một nguyên tử cacbon bậc II, còn lại là các nguyên tử cacbon bậc 1. Do đó X có công thức cấu tạo là :
CH3-CH(CH3)-CH2-CH3
Vậy khi cho X tác dụng với clo tỉ lệ 1:1:
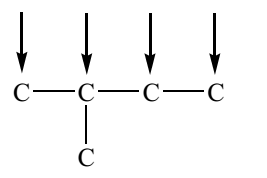
Có 4 vị trí nguyên tử Cl có thể thế vào. Vậy có 4 dẫn xuất monoclo là đồng phân cấu tạo của nhau.
Đáp án cần chọn là: C
Câu 12:
Cho 5,6 lít ankan thể tích đo ở 27,3oC và 2,2 atm tác dụng hết với clo ngoài ánh sáng thu được một dẫn xuất clo duy nhất có khối lượng 49,5 gam. Công thức phân tử của ankan là:
 Xem đáp án
Xem đáp án
Số mol ankan bằng số mol dẫn xuất và bằng:
\[n = \frac{{PV}}{{RT}} = \frac{{5,6.2,2}}{{\frac{{22,4}}{{273}}.(273 + 27,3)}} = 0,5\]. (Hằng số \[{\rm{R}} = \frac{{22,4}}{{273}} \approx 0,082.\].)
Công thức dẫn xuất là CnH2n+2-xClxcó khối lượng phân tử: 14n + 2 - x + 35,5x = 99.
Vậy x = 2, n = 2 là phù hợp.
Đáp án cần chọn là: D
Câu 13:
Hiđrocacbon Y mạch hở có 19 liên kết σ trong phân tử (ngoài ra không còn liên kết nào khác). Khi đem Y tham gia phản ứng thế với clo thì thu được 2 sản phẩm thế monoclo. Tên gọi của Y là:
 Xem đáp án
Xem đáp án
Hiđrocacbon Y mạch hở chỉ chứa liên kết σ =>Y là ankan
Đặt công thức của Y là CnH2n+2 (n≥1)
Trong phân tử ankan, liên kết C-C và C-H đều chứa 1 liên kết σ
+ n nguyên tử C tạo thành (n-1) liên kết C-C
+ (2n+2) nguyên tử H tạo thành (2n+2) liên kết C-H
=>∑ σ = (n-1) + (2n+2) = 19 =>n = 6
Vậy công thức ankan là C6H14.
Khi đem C6H14tham gia phản ứng thế với clo thì thu được 2 sản phẩm thế monoclo nên công thức cấu tạo của C6H14thỏa mãn là
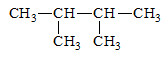
Chất Y có tên là 2,3-đimetylbutan.
Đáp án cần chọn là: D
Câu 14:
Đốt cháy hoàn toàn m gam hỗn hợp X gồm CH4, C3H6và C4H10thu được 17,6 gam CO2và 10,8 gam H2O. Giá trị của m là
 Xem đáp án
Xem đáp án
- nCO2= 0,4 mol; nH2O= 0,6 mol
- Áp dụng định luật bảo toàn nguyên tố: nC= nCO2= 0,4 mol; nH= 2.nH2O= 1,2 mol
- Bảo toàn khối lượng: mankan= mC + mH = 12.0,4 + 1.1,2 = 6 gam
Đáp án cần chọn là: C
Câu 15:
Đốt cháy một hỗn hợp hiđrocacbon ta thu được 2,24 lít CO2(đktc) và 2,7 gam H2O thì thể tích O2đã tham gia phản ứng cháy (đktc) là :
 Xem đáp án
Xem đáp án
nCO2= 0,1 mol; nH2O= 0,15 mol
Bảo toàn nguyên tố
\[2.{n_{{O_2}}} = 2.{n_{C{O_2}}} + {n_{{H_2}O}} = >\,\,{n_{{O_2}}} = \frac{{2.{n_{C{O_2}}} + {n_{{H_2}O}}}}{2} = \frac{{2.0,1 + 0,15}}{2} = 0,175\,\,mol\]
=>VO2= 0,175.22,4 = 3,92 lít
Đáp án cần chọn là: D
Câu 16:
Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai hiđrocacbon thuộc cùng dãy đồng đẳng cần dùng 6,16 lít O2và thu được 3,36 lít CO2 (các thể tích khí đo ở đktc). Giá trị của m là
 Xem đáp án
Xem đáp án
nO2= 0,275 mol ; nCO2= 0,15 mol
Bảo toàn nguyên tố O :
\[2.{n_{{O_2}}} = 2.{n_{C{O_2}}} + {n_{{H_2}O}} = >\,\,{n_{{H_2}O}} = 2.{n_{{O_2}}} - 2.{n_{C{O_2}}} = 2.0,275 - 2.0,15 = 0,25mol\]
Bảo toàn nguyên tố C và H : nC (trong X)= nCO2= 0,15 mol ; nH (trong X)= 2.nH2O= 0,5 mol
Bảo toàn khối lượng : mX= mC (trong X)+ mH (trong X) = 12.0,15 + 0,5 = 2,3 gam
Đáp án cần chọn là: A
Câu 17:
Đốt cháy hoàn toàn 0,15 mol hỗn hợp 2 ankan thu được 9,45 gam H2O. Cho sản phẩm cháy vào dung dịch Ca(OH)2dư thì khối lượng kết tủa thu được là
 Xem đáp án
Xem đáp án
Đốt cháy ankan ta có nCO2= nH2O – nankan= 0,525 – 0,15 = 0,375 mol=>mkết tủa= 0,375.100= 37,5 gam
Đáp án cần chọn là: A
Câu 18:
Đốt cháy hoàn toàn 0,2 mol hiđrocacbon X. Hấp thụ toàn bộ sản phẩm cháy vào nước vôi trong được 20 gam kết tủa. Lọc bỏ kết tủa rồi đun nóng phần nước lọc lại có 10 gam kết tủa nữa. Vậy X không thể là :
 Xem đáp án
Xem đáp án
CO2+ Ca(OH)2→ CaCO3↓ + H2O
2CO2+ Ca(OH)2→ Ca(HCO3)2
Ca(HCO3)2→ CaCO3↓ + CO2+ H2O
Từ các phản ứng, ta có: nCO2 sinh ra= nCaCO3+ 2.nCa(HCO3)2 = 0,2 + 2.0,1 = 0,4 mol
=>số C trong \[\frac{{{n_{C{O_2}}}}}{{{n_{ankan}}}} = \frac{{0,4}}{{0,2}} = 2\]
=>X không thể là CH4
Đáp án cần chọn là: C
Câu 19:
Đốt cháy hoàn toàn một hiđrocacbon X thu được 0,11 mol CO2và 0,132 mol H2O. Khi X tác dụng với khí clo thu được 4 sản phẩm monoclo. Tên gọi của X là :
 Xem đáp án
Xem đáp án
Vì đốt cháy hiđrocacbon X thu được nH2O>nCO2=>X là ankan
nX= nH2O– nCO2= 0,132 – 0,11 = 0,022 mol
=>số C trong \[X = \frac{{{n_{C{O_2}}}}}{{{n_{ankan}}}} = 5\]=>X là C5H12
C5H12+ Cl2→ 4 sản phẩm monoclo =>X có CTCT: (CH3)2CH-CH2-CH3(2-metylbutan)
Đáp án cần chọn là: A
Câu 20:
Đốt cháy hoàn toàn một hiđrocacbon A. Sản phẩm thu được hấp thụ hoàn toàn vào 200 ml dung dịch Ca(OH)20,2M thấy thu được 3 gam kết tủa. Lọc bỏ kết tủa, cân lại phần dung dịch thấy khối lượng tăng lên so với ban đầu là 0,28 gam. Hiđrocacbon trên có CTPT là
 Xem đáp án
Xem đáp án
Theo giả thiết ta có : Do đó có hai trường hợp xảy ra :
TH1:Ca(OH)2dư, chỉ xảy ra phản ứng tạo kết tủa :
CO2+ Ca(OH)2→ CaCO3+ H2O (1)
0,03 0,03 0,03
mdung dịch tăng = \[{m_{{H_2}O}} + {m_{C{O_2}}} - {m_{CaC{O_3}}} = 0,28\,\,gam \Rightarrow {m_{{H_2}O}} = 0,28 + 3 - 0,03.44 = \,\,1,96\,\,gam\]
\[ \Rightarrow {n_{{H_2}O}} = 0,1088\,\,mol \Rightarrow {n_H} = 0,217\,\,mol \Rightarrow {n_C}:{n_H} = 0,03:0,217 = 1:7,3\,.\](loại)
TH2 : Ca(OH)2phản ứng hết :
CO2+ Ca(OH)2→ CaCO3+ H2O (1)
0,03 0,03 0,03
2CO2+ Ca(OH)2→ Ca(HCO3)2(2)
0,02 0,01
\[ \Rightarrow {n_{C{O_2}}} = 0,05\,\,mol.\].
mdung dịch ăng= \[{m_{{H_2}O}} + {m_{C{O_2}}} - {m_{CaC{O_3}}} = 0,28\,\,gam \Rightarrow {m_{{H_2}O}} = 0,28 + 3 - 0,05.44 = \,\,1,08\,\,gam\]
\[ \Rightarrow {n_{{H_2}O}} = 0,06\,\,mol \Rightarrow {n_H} = 0,12\,\,mol \Rightarrow {n_C}:{n_H} = 0,05:0,12 = 5:12\,\]
Vậy CTPT của ankan là C5H12
Đáp án cần chọn là: A
Câu 21:
Trộn 2 thể tích bằng nhau của C3H8và O2rồi bật tia lửa điện đốt cháy hỗn hợp. Sau phản ứng làm lạnh hỗn hợp (để hơi nước ngưng tụ) rồi đưa về điều kiện ban đầu. Thể tích hỗn hợp sản phẩm khi ấy (V2) so với thể tích hỗn hợp ban đầu (V1) là :
 Xem đáp án
Xem đáp án
Phương trình phản ứng :
\[\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,{C_3}{H_8}\,\,\, + \,\,\,\,\,5{O_2}\,\,\,\mathop \to \limits^{{t^o}} \,\,\,\,\,3C{O_2}\,\,\,\,\,\,\, + \,\,\,\,\,\,4{H_2}O\,\,\,\,\,\,\,\,\,(1)\]
Bđ (lit): \[x\,\,\,\,\,\,\, \to \,\,\,\,\,x\,\,\,\,\,\,\,\,\,\,\,\,\,\,\]
Pứ (lit): \[\frac{x}{5}\,\,\,\,\, \leftarrow \,\,\,\,\,x\,\,\,\,\,\,\,\,\,\,\, \to \,\,\,\,\frac{{3x}}{5}\,\,\,\,\,\,\, \to \,\,\,\,\,\,\,\,\frac{{4x}}{5}\]
Spứ (lit): \[\,\frac{{4x}}{5}\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,0\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\frac{{3x}}{5}\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\frac{{4x}}{5}\]
Sau phản ứng hơi nước bị ngưng tụ nên hỗn hợp khí còn lại gồm C3H8và CO2sinh ra sau phản ứng. Ta có :
Đáp án cần chọn là: D
Câu 22:
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2(ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là :
 Xem đáp án
Xem đáp án
\[{n_{C{O_2}}} = \frac{{7,84}}{{22,4}} = 0,35\,\,mol;\,\,{n_{{H_2}O}} = \frac{{9,9}}{{18}} = 0,55\,\,mol.\]
Bảo toàn nguyên tố O: 2.nO2= 2.nCO2+ nH2O =>2x = 0,35.2 + 0,55 =>x = 0,625
Thể tích không khí cần dùng là nhỏ nhất =>oxi trong không khí phản ứng vừa đủ
=>VO2(đktc)= 0,625.22,4 = 14 lít
=>Vkhông khí (đktc)= 5.14 = 70 lít
Đáp án cần chọn là: A
Câu 23:
Đốt cháy hoàn toàn hỗn hợp X gồm hai ankan kế tiếp trong dãy đồng đẳng được 24,2 gam CO2và 12,6 gam H2O. Công thức phân tử 2 ankan là :
 Xem đáp án
Xem đáp án
Bước 1: Tính số mol của ankan
- nCO2= 0,55 mol ; nH2O= 0,7 mol
- nankan= nH2O– nCO2= 0,7 – 0,55 = 0,15 mol
Bước 2: Xác định CTPT của 2 ankan
- Số C trung bình = nCO2/ nankan= 0,55 / 0,15 = 3,66
- Vì 2 ankan liên tiếp =>2 ankan là C3H8và C4H10
Đáp án cần chọn là: C
Câu 24:
X là hỗn hợp 2 ankan. Để đốt cháy hết 10,2 gam X cần 25,76 lít O2(đktc). Hấp thụ toàn bộ sản phẩm cháy vào nước vôi trong dư được m gam kết tủa. Giá trị m là:
 Xem đáp án
Xem đáp án
nO2= 25,76/22,4 = 1,15 mol
Đặt nCO2= x và nH2O= y (mol)
+ BTKL: mCO2+ mH2O= mX+ mO2
=>44x + 18y = 10,2 + 1,15.32 (1)
+ BTNT "O": 2nCO2+ nH2O= 2nO2
=>2x + y = 2.1,15 (2)
Giải hệ thu được x = 0,7 và y = 0,9
Hấp thụ sản phẩm cháy vào nước vôi trong dư thì :
CO2+ Ca(OH)2→ CaCO3↓ + H2O
Ta thấy: nCaCO3= nCO2= 0,7 mol
Suy ra m = mCaCO3= 0,7.100 = 70 gam
Đáp án cần chọn là: C
Câu 25:
Hỗn hợp Z gồm một hiđrocacbon A và oxi (lượng oxi trong Z gấp đôi lượng oxi cần thiết để đốt cháy hết A). Bật tia lửa điện để đốt cháy hỗn hợp Z, đến khi kết thúc phản ứng thì thể tích khí và hơi sau khi đốt không đổi so với ban đầu. Nếu cho ngưng tụ hơi nước của hỗn hợp sau khi đốt thì thể tích giảm đi 40% (biết rằng các thể tích khí và hơi đều đo ở cùng điều kiện nhiệt độ và áp suất). Trong một thí nghiệm khác, đốt cháy hoàn toàn 8,96 lít khí A (đo ở đktc) rồi cho toàn bộ sản phẩm vào dung dịch chứa 22,2 gam Ca(OH)2thì khối lượng của dung dịch tăng m gam. Công thức phân tử của A và giá trị của m là?
 Xem đáp án
Xem đáp án
1. Đặt công thức của A là: CxHy (trong đó x và y chỉ nhận giá trị nguyên, dương) và thể tích của A đem đốt là a (lít), (a >o). Phản ứng đốt cháy A.
CxHy+ (x+y/4)O2→ xCO2+ y/2 H2O (1)
a a(x+y/4) ax ay/2 (lít)
\[ \Rightarrow a + 2a(x + \frac{y}{4}) = ax + a\frac{y}{2} + a(x + \frac{y}{4}) \Leftrightarrow y = 4\](I)
Sau khi ngưng tụ hơi nước thì thể tích giảm 40% do vậy:
\[{V_{{H_2}O}} = \frac{{40}}{{100}}[a + 2a(x + \frac{y}{4})]\]
Mặt khác theo (1) thì \[{V_{{H_2}O}} = a\frac{y}{2}\]. Nên ta có phương trình:
\[a\frac{y}{2} = \frac{{40}}{{100}}[a + 2a(x + \frac{y}{4})]\] (II)
Thay (I) vào (II) ta có =>x = 1 =>Công thức phân tử của A là CH4
\[{n_{C{H_4}}} = \frac{{8,96}}{{22,4}} = 0,4(mol);{n_{Ca{{(OH)}_2}}} = \frac{{22,2}}{{74}} = 0,3(mol)\]
nCO2= nCH4= 0,4 mol (mol). Xét tỷ lệ \[\frac{{{n_{C{O_2}}}}}{{{n_{Ca{{(OH)}_2}}}}}\] ta thấy \[1 \le \frac{{0,4}}{{0,3}} \le 2\].
CH4+ 2O2→ CO2+ 2H2O (2)
0,4 0,4 0,8 (mol)
Ca(OH)2+ CO2→ CaCO3+ H2O (3)
0,3 0,3 0,3 (mol)
CaCO3+ CO2+ H2O → Ca(HCO3)2(4)
0,1 0,1 0,1 (mol)
Theo (3) nCaCO3= nCO2= nCa(OH)2= 0,3 mol
Số mol CO2tham gia phản ứng ở (4) là: (0,4 - 0,3) = 0,1 (mol). Theo (4) =>nCaCO3= nCO2= 0,1 mol.
Vậy số mol CaCO3không bị hòa tan sau phản ứng (4) là:
nCaCO3= 0,3 - 0,1 = 0,2 mol.
Ta có: Δm dd= mCO2+ mH2O- mCaCO3= 0,4.44 + 0,8.18 - 0,2.100 = 12 gam >0
=>m = 12 gam.
Đáp án cần chọn là: B