Bài tập amin
-
703 lượt thi
-
44 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
 Xem đáp án
Xem đáp án
(CH3)2NH là amin bậc 2 có lực bazơ mạnh hơn amin bậc 1 và mạnh hơn amoniac
→ Chất có lực bazơ mạnh nhất là (CH3)2NH
Đáp án cần chọn là: D
Câu 2:
So sánh tính bazơ của các hợp chất hữu cơ sau : NH3, CH3NH2, (C2H5)2NH, C2H5NH2, (CH3)2NH ?
 Xem đáp án
Xem đáp án
Gốc C2H5- đẩy e mạnh hơn gốc CH3- do đó lực bazơ của C2H5NH2>CH3NH2 và (C2H5)2NH >(CH3)2NH
Do tính bazơ của amin bậc 2 mạnh hơn amin bậc 1 nên
→ thứ tự sắp xếp là : (C2H5)2NH >(CH3)2NH >C2H5NH2>CH3NH2>NH3
Đáp án cần chọn là: B
Câu 3:
 Xem đáp án
Xem đáp án
Vì gốc C6H5- hút e nên lực bazơ của (C6H5)3N < (C65)2NH < C6H5NH2 NH3không có gốc đẩy hay hút e → thứ tự sắp xếp theo lực bazơ giảm là (4), (1), (3), (2) Đáp án cần chọn là: A
Câu 4:
 Xem đáp án
Xem đáp án
Gốc C6H5CH2- là gốc đẩy e yếu
Vì CH3- (gốc đẩy e) đính vào vòng nên p-CH3C6H4- hút e yếu hơn gốc C6H5-
→ lực bazơ của C6H5NH2 yếu hơn p-CH3C6H4NH2
(C6H5)2NH có 2 gốc C6H5- hút e nên lực bazơ của (C6H5)2NH yếu hơn C6H5NH2
→ Chất có tính bazơ yếu nhất là (C6H5)2NH
Đáp án cần chọn là: B
Câu 5:
 Xem đáp án
Xem đáp án
(1) NH3 không có gốc đẩy hay hút e
(2) C6H5NH2có nhóm C6H5- hút e
(3) p-NO2C6H4NH2:
Vì NO2- (gốc hút e) đính vào vòng nên p-NO2C6H4- hút e mạnh hơn gốc C6H5-
→ lực bazơ của p-NO2C6H4NH2 yếu hơn C6H5NH2 → (3) < (2)
(4) p-CH3C6H4NH2
Vì CH3- (gốc đẩy e) đính vào vòng nên p-CH3C6H4- hút e yếu hơn gốc C6H5-
→ lực bazơ của p-CH3C6H4NH2 mạnh hơn C6H5NH2 → (2) < (4)
(5) CH3NH2có nhóm đẩy e
(6) (CH3)2NH có 2 nhóm CH3- đẩy e → lực bazơ mạnh hơn CH3NH2 → (5) < (6)
→ thứ tự sắp xếp là : 3 < 2 < 4 < 1 < 5 < 6
Đáp án cần chọn là: A
Câu 6:
 Xem đáp án
Xem đáp án
Sắp xếp theo chiều tính bazơ tăng : các chất xếp sau có tính bazơ mạnh hơn chất trước
A, B sai vì đimetylamin có 2 gốc CH3- đẩy e nên tính bazơ mạnh hơn etylamin chỉ có 1 gốc C2H5- đẩy e
C sai vì NH3không có gốc đẩy hay hút e nên tính bazơ mạnh hơn p-nitroanilin có gốc p-NO2C6H4hút e
D đúng vì
p-nitroanilin có gốc NO2- (gốc hút e) đính vào vòng nên p-NO2C6H4- hút e mạnh hơn gốc C6H5-
→ lực bazơ của p-NO2C6H4NH2 yếu hơn C6H5NH2
đimetylamin có 2 gốc CH3- đẩy e nên tính bazơ mạnh hơn etylamin chỉ có 1 gốc C2H5- đẩy e
Đáp án cần chọn là: D
Câu 7:
 Xem đáp án
Xem đáp án
(1) NH3không có gốc đẩy hay hút e
(2) CH3NH2 có gốc CH3- đẩy e → (2) >(1)
(3) KOH là bazơ mạnh nên có tính bazơ mạnh nhất trong các chất
(4) C6H5NH2có gốc C6H5- hút e → (1) >(4)
(5) (CH3)2NH có 2 gốc CH3- đẩy e → lực bazơ mạnh hơn CH3NH2 → (5) >(2)
→ thứ tự sắp xếp theo chiều giảm dần là : (3), (5), (2), (1), (4)
Đáp án cần chọn là: B
Câu 8:
 Xem đáp án
Xem đáp án
Đimetylamin có 2 gốc CH3- đẩy e → lực bazơ mạnh hơn metylamin → (1) < (4)
Điphenylamin có 2 gốc C6H5- hút e → lực bazơ yếu hơn phenylamin → (3) < (2)
→ thứ tự tăng dần lực bazơ là : (3) < (2) < (1) < (4)
Đáp án cần chọn là: A
Câu 9:
 Xem đáp án
Xem đáp án
CH3NH2, (CH3)2NH, (CH3)3N đều có tính bazơ mạnh hơn amoniac → làm xanh giấy quỳ tím
C6H5NH2không làm đổi màu quỳ
Đáp án cần chọn là: C
Câu 10:
 Xem đáp án
Xem đáp án
C6H5NH2không làm đổi màu quỳ
CH3NH2, (C2H5)2NH có tính bazơ mạnh hơn amoniac → làm quỳ chuyển xanh
NH4Cl là muối tạo bởi bazơ yếu và axit mạnh → có tính axit → làm quỳ chuyển đỏ
NaOH là bazơ mạnh → làm quỳ chuyển xanh
K2CO3 là muối tạo bởi axit yếu và bazơ mạnh → có tính bazơ → làm quỳ chuyển xanh
→ có 5 dung dịch làm quỳ chuyển màu
Đáp án cần chọn là: B
Câu 11:
 Xem đáp án
Xem đáp án
Đáp án A, B, D đều là phản ứng thể hiện tính bazơ của amin
Chỉ có đáp án C là phản ứng oxi hóa - khử, không phải là phản ứng axit - bazơ
Đáp án cần chọn là: C
Câu 12:
C2H5NH2trong nước không phản ứng với chất nào trong số các chất sau ?
 Xem đáp án
Xem đáp án
NaOH là dung dịch kiềm nên không tác dụng với C2H5NH2
Đáp án cần chọn là: C
Câu 13:
 Xem đáp án
Xem đáp án
Amin X no, mạch hở có CTPT dạng CnH2n+2+kNk(k là số chức amin)
Bảo toàn nguyên tố ta có :
\[{n_{C{O_2}}} = {n_C}\,\, \to \,\,x = \,na(mol)\]
\[{n_{{H_2}O}} = \frac{{{n_H}}}{2}\,\, \to \,\,y = \,na + a + a.\frac{k}{2}\,\,\,mol;\,\]
\[{n_{{N_2}}} = \frac{{{n_N}}}{2} \to \,\,\,z = a.\frac{k}{2}\,\,mol\]
→ y = x + a + z hay a = y – x – z
Đáp án cần chọn là: A
Câu 14:
Tiến hành thí nghiệm theo các bước sau đây:
Bước 1: Cho 1 ml C6H5NH2(D = 1,02g/cm3) vào ống nghiệm có sẵn 2 ml H2O, lắc đều, sau đó để yên ống nghiệm.
Bước 2: Nhỏ tiếp 2 ml dung dịch HCl đặc (10M) vào ống nghiệm, lắc đều sau đó để yên.
Bước 3: Nhỏ tiếp 2 ml dung dịch NaOH 2M vào ống nghiệm, lắc đều sau đó để yên.
Phát biểu nào sau đây đúng?
 Xem đáp án
Xem đáp án
Bước 1: C6H5NH2không tan trong nước nên tách thành 2 lớp
Bước 2: C6H5NH2+ HCl → C6H5NH3Cl
Với C6H5NH3Cl là chất tan tốt trong nước nên dung dịch thu được đồng nhất, trong suốt
Bước 3: NaOH + C6H5NH3Cl → C6H5OH + NaCl + H2O
⟹ C6H5NH2lại tách lớp với dung dịch
A sai vì bước 2 ống nghiệm không tách lớp
B đúng
C sai vì chỉ tách lớp và tổn tại dạng chất lỏng chứ không có kết tủa rắn
D sai vì CO2không phản ứng với C6H5NH3Cl nên không có hiện tượng gì
Đáp án cần chọn là: B
Câu 15:
 Xem đáp án
Xem đáp án
Cách 1: lập tỉ lệ nc : nH
Theo giả thiết ta có
\[{n_C} = {n_{C{O_2}}} = \frac{{8,96}}{{22,4}} = 0,4\,\,mol;\,\,{n_H} = 2.{n_{{H_2}O}} = 2.\frac{{9,9}}{{18}} = 1,1\,\,mol;\,\,\]
→ nC : nH= 0,4 : 1,1 = 4 : 11
Dựa vào đáp án → CTPT của amin là C4H11N
Cách 2:
Vì amin no, mạch hở, đơn chức nên \[{n_{{H_2}O}} - {n_{C{O_2}}} = 1,5{n_{a\min }}\]
\[ \to {n_{a\min }} = \frac{{{n_{{H_2}O}} - {n_{C{O_2}}}}}{{1,5}} = \frac{{0,55 - 0,4}}{{1,5}} = 0,1\,\,mol\]
→ Số C trong amin = \[\frac{{{n_{C{O_2}}}}}{{{n_X}}} = \frac{{0,4}}{{0,1}} = 4\]
Số H trong amin = \[\frac{{2{n_{{H_2}O}}}}{{{n_X}}} = \frac{{0,55.2}}{{0,1}} = 11\]
Vậy CTPT của X là C4H11N
Đáp án cần chọn là: B
Câu 16:
Khi đốt cháy hoàn toàn một amin đơn chức X, thu được 16,8 lít khí CO2; 2,8 lít khí N2(các thể tích khí đo ở điều kiện tiêu chuẩn) và 20,25 gam H2O. CTPT của X là
 Xem đáp án
Xem đáp án
Cách 1 : lập tỉ lệ mol nC: nH: nN
Theo giả thiết ta có :
\[\begin{array}{*{20}{l}}{{n_C} = {n_{C{O_2}}} = \frac{{16,8}}{{22,4}} = 0,75\,\,mol;\,\,{n_H} = 2.{n_{{H_2}O}} = 2.\frac{{20,25}}{{18}} = 2,25\,\,mol;\,\,}\\{{n_N} = 2.{n_{{N_2}}} = 2.\frac{{2,8}}{{22,4}} = 0,25\,\,mol.}\end{array}\]
\[ \Rightarrow {n_C}:{n_H}:{n_N} = 0,75:2,25:0,25 = 3:9:1\]
Vậy CTPT của X là C3H9N.
Cách 2 : bảo toàn nguyên tố N : \[{n_X} = {n_N} = 2{n_{{N_2}}}\]
Đối với các amin đơn chức thì phân tử có một nguyên tử N :
Bảo toàn nguyên tử N : \[{n_X} = {n_N} = 2{n_{{N_2}}} = 0,25\,\,mol\]
→ Số C trong amin= \[\frac{{{n_{C{O_2}}}}}{{{n_X}}} = \frac{{0,75}}{{0,25}} = 3\]
Số H trong amin = \[\frac{{2{n_{{H_2}O}}}}{{{n_X}}} = \frac{{2,25}}{{0,25}} = 9\]
Vậy CTPT của X là C3H9N
Đáp án cần chọn là: D
Câu 17:
Đốt cháy một hỗn hợp amin A cần V lít O2 (đktc) thu được N2và 31,68 gam CO2và 7,56 gam H2O. Giá trị V là
 Xem đáp án
Xem đáp án
\[{n_{C{O_2}}} = \frac{{31,68}}{{44}} = 0,72\,\,mol;\,\,\,{n_{{H_2}O}} = \frac{{7,56}}{{18}}\]
Bảo toàn nguyên tử oxi ta có :
\[2{n_{{O_2}}} = 2{n_{C{O_2}}} + {n_{{H_2}O}} \to \,\,{n_{{O_2}}} = \frac{{2{n_{C{O_2}}} + {n_{{H_2}O}}}}{2} = \frac{{2.0,72 + 0,42}}{2} = 0,93\,\,mol\]
\[ \to \,\,{V_{{O_2}}} = 22,4.0,93 = 20,832\]
Đáp án cần chọn là: C
Câu 18:
 Xem đáp án
Xem đáp án
\[{n_C} = {n_{C{O_2}}} = \frac{{17,6}}{{44}} = 0,4\,\,mol;\,\,{n_H} = 2.{n_{{H_2}O}} = 2.\frac{{12,6}}{{18}} = 1,4\,\,mol\]
Áp dụng định luật bảo toàn nguyên tố đối với oxi suy ra :
\[{n_{{O_2}{\kern 1pt} (kk)}} = \frac{{2.{n_{C{O_2}}} + {n_{{H_2}O}}}}{2} = 0,75\,\,mol \Rightarrow {n_{{N_2}{\kern 1pt} (kk)}} = 0,75.4 = 3\,\,mol.\,\]
\[ \to \,\,{n_{N{\kern 1pt} (hchc)}} = 2.(\frac{{69,44}}{{22,4}} - 3) = 0,2\,mol\, \Rightarrow {n_C}:{n_H}:{n_N} = 0,4:1,4:0,2 = 2:7:1.\]
Căn cứ vào các phương án ta thấy công thức của X là C2H5NH2.
Đáp án cần chọn là: A
Câu 19:
 Xem đáp án
Xem đáp án
Nito không bị hấp thụ bởi Ca(OH)2=>khí thoát ra khỏi bình là khí N2
Bảo toàn nguyên tử N : \[{n_{N{\kern 1pt} {\kern 1pt} (trong{\kern 1pt} {\kern 1pt} X)}} = 2{n_{{N_2}}} = \frac{{0,448}}{{22,4}}\, = 0,02\,mol\]
mkết tủa=\[{m_{CaC{{\rm{O}}_3}}} = \frac{4}{{100}} = 0,04\,\,mol\,\, \to \,\,{n_{C{O_2}}} = 0,04\,\,mol\]
mbình tăng = \[{m_{C{O_2}}} + {m_{{H_2}O}} = 3,2\,\,gam\,\, \to \,\,{m_{{H_2}O}} = 3,2 - 0,04.44 = 1,44\,\,gam\,\, \to \,\,{n_{{H_2}O}} = 0,08\,\,mol\]
→ nC: nH: nN= 0,04 : 0,16 : 0,04 = 1 : 4 : 1
=>CTĐGN của X là CH4N
=>CTPT của X là C2H8N2
Đáp án cần chọn là: A
Câu 20:
 Xem đáp án
Xem đáp án
Công thức chung của ankylamin là CnH2n+3N (\[n \ge 1\])
\[\frac{{{V_{C{O_2}}}}}{{{V_{{H_2}O}}}} = \frac{n}{{n + 1,5}}\]
Khi n = 1 =>a = 0,4
Khi \[n \to + \infty \,\, \Rightarrow a = 1\]
Đáp án cần chọn là: C
Câu 21:
 Xem đáp án
Xem đáp án
\[{n_{{O_2}}} = \frac{{10,08}}{{22,4}} = 0,45\,\,mol\]
Gọi số mol của CO2, H2O và N2lần lượt là a, b, c mol
Bảo toàn nguyên tố oxi : \[2{n_{C{O_2}}} + {n_{{H_2}O}} = 2{n_{{O_2}}} \to {\rm{ }}2a{\rm{ }} + {\rm{ }}b{\rm{ }} = {\rm{ }}0,9\] (1)
Bảo toàn khối lượng : mamin= mC+ mH+ mN→ 12a + 2b + 28c = 6,2 (2)
Vì đốt cháy amin no, mạch hở, đơn chức nên ta có :
\[{n_{{H_2}O}} - {n_{C{O_2}}} = 1,5{n_{a\min }}\]và\[{n_{{N_2}}} = \frac{1}{2}{n_{a\min }} \to {n_{{H_2}O}} - {n_{C{O_2}}} = 3{n_{{N_2}}}\]
→ b – a = 3c (3)
Từ (1), (2) và (3) →\(\left\{ {\begin{array}{*{20}{c}}{a = 0,2}\\{b = 0,5}\\{c = 0,1}\end{array}} \right.\)
→ nC: nH: nN= 0,2 : 0,5.2 : 0,1.2 = 1 : 5 : 1
→ công thức phân tử của amin là CH3NH2
Đáp án cần chọn là: B
Câu 22:
 Xem đáp án
Xem đáp án
Sơ đồ phản ứng :
Mol:0,10,2
Ta có: \[0,2\bar n\, = \,0,1.\frac{{2\bar n\, + \,3}}{2}\, \Rightarrow \,\bar n\, = \,1,5.\]
Vậy công thức phân tử của 2 amin là CH5N và C2H7N.
Đáp án cần chọn là: A
Câu 23:
 Xem đáp án
Xem đáp án
A là đồng đẳng của anilin nên công thức của A là CnH2n-7NH2, (n ≥ 7, nguyên)
B là đồng đẳng của metylamin nên công thức của B là CmH2m+1NH2, (m ≥ 2, nguyên).
Ta có:
\[{n_A} = 2.{n_{{N_2}}} = 2.0,015 = 0,03\,mol \Rightarrow {M_A} = 14n + 9 = \frac{{3,21}}{{0,03}} = 107\,gam/mol\, \Rightarrow n = 7.\]
Sơ đồ phản ứng :
\[{C_m}{H_{2m + 1}}N{H_2}\,\mathop \to \limits^{{O_2},{\kern 1pt} {t^o}} \,mC{O_2} + \frac{{2m + 3}}{2}{H_2}O + \frac{1}{2}{N_2}\]
\[{V_{C{O_2}}}:{V_{{H_2}O}} = 2:3 \Rightarrow m = 3\]
CTCT phù hợp của A, B lần lượt là :
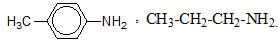
Đáp án cần chọn là: B
Câu 24:
 Xem đáp án
Xem đáp án
Theo giả thiết ta có:
\[{n_{{H_2}O}} = 0,9\,\,mol\,\,;\,\,{n_{C{O_2}}} = 0,6\,\,mol\,\,;\,\,{n_N} = \frac{{11,8 - 0,9.2 - 0,6.12}}{{14}} = 0,2\,\,mol\]
\[ \Rightarrow {n_C}:{n_H}:{n_N} = 0,6:1,8:0,2 = 3:9:1.\]
Vậy công thức phân tử trung bình của ba amin là C3H9N thuộc dạng CnH2n+3N, suy ra ba amin thuộc loại amin no đơn chức và phải có ít nhất một amin có số C lớn hơn 3.
Đáp án cần chọn là: D
Câu 25:
Hỗn hợp X gồm O2và O3có tỉ khối so với H2là 22. Hỗn hợp khí Y gồm metylamin và etylamin có tỉ khối so với H2là 17,833. Để đốt cháy hoàn toàn V1lít Y cần vừa đủ V2lít X (biết sản phẩm cháy gồm CO2, H2O và N2, các chất khí khi đo ở cùng điều kiện nhiệt độ, áp suất). Tỉ lệ V1: V2 là :
 Xem đáp án
Xem đáp án
Đặt CTPT trung bình của 2 amin là \[{C_{\bar n}}{H_{2\bar n + 3}}N\]
Theo giả thiết suy ra :\[14\bar n + 17 = 2.17,833 \Rightarrow \bar n = \frac{4}{3}\]
Quy đổi hỗn hợp O3, O2thành O, theo định luật bảo toàn khối lượng ta có .
Sơ đồ phản ứng :
\[2{C_{\bar n}}{H_{2\bar n + 3}}N\mathop \to \limits^{{t^o}} 2\bar nC{O_2} + (2\bar n + 3){H_2}O + {N_2}\,\,\,\,(1)\]
Mol:1\[\bar n\]\[\frac{{2\bar n + 3}}{2}\]
Theo (1) ta có :
\[{n_{O{\kern 1pt} {\kern 1pt} pu}} = 2\bar n + \frac{{2\bar n + 3}}{2} = 5,5\,\,mol \Rightarrow {m_{\left( {{{\rm{O}}_3},{{\rm{O}}_2}} \right)}} = {m_O} = 5,5.16 = 88\,\,gam \Rightarrow {n_{\left( {{{\rm{O}}_3},{{\rm{O}}_2}} \right)}} = \frac{{88}}{{2.22}} = 2\,\,mol.\] Vậy VY : VX = 1 : 2.
Đáp án cần chọn là: D
Câu 26:
 Xem đáp án
Xem đáp án
Gọi CTPT trung bình cho 2 amin là \[{C_{\bar n}}{H_{2\bar n + 3}}N\]
Giả sử lấy 1 mol amin
Bảo toàn nguyên tố C : \[{n_{C{O_2}}} = \bar n\]
Bảo toàn nguyên tố H :\[{n_{{H_2}O}} = \frac{{2\bar n + 3}}{2}\]
Vì \[{n_{C{O_2}}}:{n_{{H_2}O}} = {\rm{ }}7{\rm{ }}:{\rm{ }}10{\rm{ }} \to 10\bar n{\rm{\;}} = {\rm{\;7}}{\rm{.}}\frac{{2\bar n + 3}}{2} \Rightarrow \bar n = 3,5\]
→ 2 amin là C3H7NH2và C4H9NH2
Đáp án cần chọn là: C
Câu 27:
 Xem đáp án
Xem đáp án
Khối lượng bình 2 tăng 21,12 gam →\[ \to {m_{C{O_2}}} = 21,12gam\,\, \to \,\,{n_{C{O_2}}} = 0,48\,\,mol\]
namin = 0,3 mol
\[ \to \,\,\bar C = \frac{{{n_{C{O_2}}}}}{{{n_{a\min }}}} = \frac{{0,48}}{{0,3}} = 1,6\]
Vậy 2 amin là CH3NH2và C2H5NH2
Đáp án cần chọn là: A
Câu 28:
 Xem đáp án
Xem đáp án
CnH2n+3N →→nCO2+ (n+1,5)H2O + 0,5 N2
x nx (n+1,5)x 0,5x
Vì N2là khí trơ nên dung dịch NaOH chỉ hấp thụ CO2và H2O
=>mdd tăng =\[{m_{C{O_2}}} + {m_{{H_2}O}} = 44n{\rm{x}} + 18x(n + 1,5) = \,\,(62n + 27)x = 24\,\,\,\,(1)\]
mX=(14n+17)x =7,6 (2)
Từ (1) và (2) =>\(\left\{ {\begin{array}{*{20}{c}}{nx = 0,3}\\{x = 0,2}\end{array}} \right. \to \left\{ {\begin{array}{*{20}{c}}{n = 1,5}\\{x = 0,2}\end{array}} \right.\)
Theo định luật BTKL
\[\begin{array}{*{20}{l}}{{m_X} + {m_{{O_2}}} = {m_{C{O_2}}} + {m_{{H_2}O}} + {m_{{N_2}}} \to 7,6 + 32.{n_{{O_2}}} = 24 + 2,8}\\{ \to {n_{{O_2}}} = 0,6\,\,mol}\end{array}\]
Trong không khí : O2a mol, N24a mol
Hỗn hợp Y gồm: \[{n_{{O_2}}} = a - 0,6\,\,\,mol;\,\,\,\,{n_{{N_2}}} = 4a + 0,1\,\,\,mol\]
\[{n_{{O_2}}}:{n_{{N_2}}} = 1:9 \to 9(a - 0,6) = 4{\rm{a}} + 0,1 \to a = 1,1\,mol\]
\[{n_Y} = 1,1 - 0,6 + 4.1,1 + 0,1 = 5mol \to V = 22,4.5 = 112\,\,lit\]
Đáp án cần chọn là: B
Câu 29:
 Xem đáp án
Xem đáp án
Gọi CTPT của anken là CnH2n
CTPT trung bình của 2 amin là \[{C_{\bar m}}{H_{2\bar m + 3}}N\]
PTHH :
\[{\rm{\;}}{C_n}{H_{2n}} + \frac{{3n}}{2}{O_2} \to nC{O_2} + n{H_2}O\]
a\( \to \)\[\frac{{3na}}{2}\]\( \to \)an
\[{C_{\bar m}}{H_{2\bar m + 3}}N + \frac{{6\bar m + 3}}{4}{O_2} \to \bar mC{O_2} + \frac{{2\bar m + 3}}{2}{H_2}O + \frac{1}{2}{N_2}\]
b\( \to \)\[\frac{{(6\bar m + 3)b}}{2}\]\( \to \)\(b\overline m \)
\(\left\{ {\begin{array}{*{20}{c}}{{n_{C{O_2}}} = 0,1 = an + b\overline m }\\{0,2025 = \frac{{3an}}{2} + \frac{{(6\overline m + 3)b}}{4}}\end{array}} \right. \Rightarrow b = 0,07 \Rightarrow an + 0,07\overline m = 0,1 \Rightarrow \overline m < 2\)
→ 2 amin là CH5N và C2H7N
Đáp án cần chọn là: C
Câu 30:
 Xem đáp án
Xem đáp án
\[{n_{C{O_2}}} = \frac{{19,05}}{{22,4}} = 0,85\,\,mol;\,\,{n_{{N_2}}} = \frac{{0,56}}{{22,4}} = 0,025\,\,mol\]
Bảo toàn khối lượng : mhhA= mC+ mH + mN→ 0,85.12 + mH + 0,025.2.14 = 12,95
→ nH= 2,05 mol
\[ \to \,\,{n_{{H_2}O}} = \frac{{{n_H}}}{2} = 1,025\,\,mol\,\, \to \,\,{m_{{H_2}O}} = 18,45\,\,gam\]
Đáp án cần chọn là: B
Câu 31:
 Xem đáp án
Xem đáp án
Ta có : \[{V_{{H_2}O}} = {\rm{ }}375{\rm{ }}--{\rm{ }}175{\rm{ }} = {\rm{ }}200{\rm{ }}ml;\,{V_{C{O_2}}} + {V_{{N_2}}} = 175\,\,ml\]
\[{V_{{H_2}O}} - {V_{C{O_2}}} - {V_{{N_2}}} = 25\,\,ml\, = \,\,\frac{1}{2}\]nhỗn hợp
→ 2 hiđrocacbon chỉ có thể là anken và Vamin= Vanken= 25 ml
Đặt công thức chung của 2 anken là \[{C_{\bar n}}{H_{2\bar n + 2}}\]
\[{V_{C{O_2}}} = 25\bar n + 3.25 = 25\bar n + 75;\,\,\,\,\,\,\,{V_{{N_2}}} = 0,5.25 = 12,5\]
\[ \to \,\,\,25\bar n + 75 + 12,5 = 175\,\, \to \,\,\bar n = 3,5\]
Vậy 2 hiđrocacbon là C3H6và C4H8
Đáp án cần chọn là: C
Câu 32:
 Xem đáp án
Xem đáp án
\[{n_{C{O_2}}} = \frac{{17,92}}{{22,4}} = 0,8\,\,mol;\,\,{n_{{H_2}O}} = \frac{{21,6}}{{18}} = 1,2\,\,mol;\,\,{n_{{N_2}}} = \frac{{123,2}}{{22,4}} = 5,5\,\,mol\]
Gọi CTPT của ancol là CmH2m+2O; CTPT của amin là CnH2n+3N
nkhông khí = 6,75 mol
\[ \to \,\,{n_{{O_2}}} = \frac{{6,75}}{5} = 1,35\,\,mol;\,\,{n_{{N_2}(kk)}} = 6,75 - 1,35 = 5,4\,\,mol\]
Bảo toàn nguyên tố N :
\[{n_{{C_n}{H_{2n + 3}}N}} = 2{n_{{N_2}}} = {\rm{ }}0,2{\rm{ }}mol\]
Bảo toàn nguyên tố O :
\[{n_{{C_m}{H_{2m + 2}}O}} = 2{n_{C{O_2}}} + {n_{{H_2}O}} - 2{n_{{O_2}}} = 2.0,8 + 1,2 - 2.1,35 = 0,1\,\,mol\]
Bảo toàn nguyên tố C: \[{n_{C{O_2}}} = n.{n_{{C_n}{H_{2n + 3}}N}} + m.{n_{{C_m}{H_{2m + 2}}O}}\]
→ 0,2n + 0,1m = 0,8 → 2n + m = 8
→ m = 2 và n = 3 phù hợp với đáp án
Vậy CTPT của ancol và amin là C2H6O vàC3H9N
Đáp án cần chọn là: B
Câu 33:
 Xem đáp án
Xem đáp án
namin= 0,12 mol ; nX= 0,4 mol
Bảo toàn oxi : 2nO2= 2nCO2+ nH2O=>nH2O= 0,94 mol
TQ : CnH2n+3N ; CmH2m+2; CtH2t
=>nH2O– nCO2= 1,5namin+ nankan
=>nankan= 0,2 mol =>nanken= 0,08 mol
Bảo toàn C : 0,12n + 0,2m + 0,08t = 0,56
=>n = m = 1 ; t = 3
=>CH5N ; CH4; C3H6
=>%mC3H6= 32,6%
Đáp án cần chọn là: D
Câu 34:
 Xem đáp án
Xem đáp án
Đặt công thức của hh 2 amin no, đơn chức, kế tiếp nhau trong dãy đồng đẳng là: \[{C_{\bar n}}{H_{2\bar n + 3}}N\]
PTHH: \[{C_{\bar n}}{H_{2\bar n + 3}}N + {O_2}\mathop \to \limits^{{t^0}} \bar nC{O_2} + (\bar n + 1,5){H_2}O\]nCO2(đktc)= 1,568/22,4 = 0,07 (mol)
nH2O= 1,8/18 = 0,1 (mol)
Ta có: namin= (nH2O– nCO2)/1,5 = 0,02 (mol)
\[\bar n = \frac{{{n_{C{O_2}}}}}{{n\,a\min }} = \frac{{0,07}}{{0,02}} = 3,5\]
Vì 2 amin đồng đẳng kế tiếp nên CTPT 2 amin là C3H9N và C4H11N
CTCT amin bậc 2 của C3H9N: CH3CH2-NH-CH3
CTCT amin bậc 2 của C4H11N: CH3-CH2-CH2-NH-CH3; CH3-CH(CH3)-NH-CH3; C2H5-NH-C2H5
→ Tổng có 4 CTCT thỏa mãn.
Đáp án cần chọn là: A
Câu 35:
 Xem đáp án
Xem đáp án
Bảo toàn nguyên tố N có: nC2H5NH2= 2nN2= 0,1 mol
⟹ mC2H5NH2= 0,1.45 = 4,5 gam
Đáp án cần chọn là: C
Câu 36:
 Xem đáp án
Xem đáp án
Dùng bảo toàn khối lượng ta có: mHCl= mmuối- mamin= 9,125 (g)
→ nHCl= 0,25 (mol) → nAmin= nHCl= 0,25 mol
Gọi công thức chung của 2 amin có dạng CxH2x+3N
→ M2 amin= m : n = 13,35 : 0,25 = 53,4 (g/mol)
⟹ 14x + 3 + 14 = 53,4 ⟹ x = 2,6
Khi đốt hỗn hợp X thì:
CxH2x+3N + (1,5x + 0,75) O2→ xCO2+ (2x+3)/2 H2O + ½ N2
Vậy \[\frac{{{V_{C{O_2}}}}}{{{V_{{H_2}O}}}} = \frac{{{n_{C{O_2}}}}}{{{n_{{H_2}O}}}} = \frac{x}{{x + 1,5}} = \frac{{2,6}}{{2,6 + 1,5}} = \frac{{26}}{{41}}\]
Đáp án cần chọn là: B
Câu 37:
 Xem đáp án
Xem đáp án
Ta có: nCH3NH2= 6,2/31 = 0,2 mol
PTHH: CH3NH2+ 2,25 O2→ CO2+ 2,5 H2O + 0,5 N2
0,2 → 0,2 → 0,5 (mol)
Bình đựng dung dịch Ca(OH)2hấp thụ cả CO2và H2O
⟹ mbình tăng= mCO2+ mH2O= 0,2. 44 + 0,5.18 = 17,8 gam
Đáp án cần chọn là: D
Câu 38:
 Xem đáp án
Xem đáp án
nCO2= 6,72 : 22,4 = 0,3 mol; nH2O= 9,45 : 18 = 0,525 mol; nN2= 1,68 : 22,4 = 0,075 mol
Amin no đơn chức mạch hở có dạng CnH2n+3N
Bảo toàn nguyên tố O: 2nO2= 2nCO2+ nH2O→ nO2= 0,5625 mol
Bảo toàn khối lượng: mamin+ mO2= mCO2+ mH2O+ mN2
→ mamin= 44.0,3 + 18.0,525 + 28.0,075 - 0,5625.32 = 6,75 gam
Đáp án cần chọn là: A
Câu 39:
 Xem đáp án
Xem đáp án
Ta có: nO2= 0,6 mol; nCO2= 0,3 mol
BTNT O =>2nO2= 2nCO2+ nH2O→ nH2O= 0,6 mol
Đặt công thức chung của 2 amin no, đơn chức, mạch hở X và Y là CnH2n+3N
CnH2n+3N + (3n/2+3/4) O2→ nCO2+ (2n+3)/2 H2O
=>nM= (nH2O- nCO2)/1,5 = 0,2 mol
Suy ra số nguyên tử C = nCO2/nM =0,3: 0,2 = 1,5
=>X là CH5N và Y là C2H7N (etylamin).
Đáp án cần chọn là: A
Câu 40:
 Xem đáp án
Xem đáp án
Công thức amin no đơn chức là CnH2n+3N
Phản ứng cháy có nCO2 : nH2O= 4 : 7
=>nC : nH= 2 : 7 = n : (2n + 3) =>n = 2
=>Amin đơn chức là C2H7N
Amin bậc 2 =>CH3NHCH3(đimetyl amin)
Đáp án cần chọn là: C
Câu 41:
Hỗn hợp khí E gồm một amin bậc III no, đơn chức, mạch hở và hai ankin X, Y (MX< MY</>). Đốt cháy hoàn toàn 0,15 mol hỗn hợp E cần dùng 11,2 lít O2(đktc), thu được hỗn hợp F gồm CO2, H2O và N2. Dẫn toàn bộ F qua bình đựng dung dịch KOH đặc, dư đến phản ứng hoàn toàn thấy khối lượng bình bazơ nặng thêm 20,8 gam. Số cặp công thức cấu tạo ankin X, Y thỏa mãn là
 Xem đáp án
Xem đáp án
Đặt a, b là số mol CO2, H2O
mBình nặng= mCO2+ mH2O=>44a + 18b = 20,8 (1)
BTNT O: 2nO2= 2nCO2+ nH2O=>2a+ b = 2.0,5 (2)
Từ (1) và (2) =>a = 0,35 và b = 0,3 (mol)
Hỗn hợp E gồm:
\(\left\{ {\begin{array}{*{20}{c}}{{C_m}{H_{2m}}_{ + 3}N:vmol}\\{{C_{\overline n }}{H_{2\overline n - 2}}:umol}\end{array}} \right.\)
Ta có:
\(\left\{ {\begin{array}{*{20}{c}}{{n_E} = v + u = 0,15}\\{{n_{CO2}} = mv + \overline n u = 0,35}\\{{n_{{H_2}O}} = v(m + 1,5) + u(\overline n - 1) = 0,3}\end{array}} \right. \Rightarrow \left\{ {\begin{array}{*{20}{c}}{v = 0,04}\\{u = 0,11}\end{array}} \right.\)
Vì \[m{\rm{ }} \ge {\rm{ }}3\]và
\( \Rightarrow \left\{ {\begin{array}{*{20}{c}}{m = 3}\\{\overline n = \frac{{23}}{{11}}}\end{array}} \right.\) là nghiệm duy nhất thỏa mãn
Vậy 2 cặp ankin thỏa mãn là: (Vì MX< MY</>
và các chất ở thể khí)
=>Các cặp CTCT thỏa mãn là:
Cặp 1: CH≡ CH và CH≡C-CH3
Cặp 2: CH≡ CH và CH≡ C-CH2-CH3
Cặp 3: CH≡ CH và CH3- C≡C -CH3
Đáp án cần chọn là: C
Câu 42:
 Xem đáp án
Xem đáp án
3,17gZ\(\left\{ {\begin{array}{*{20}{c}}{{C_n}{H_{2n + 3}}N:z}\\{{C_m}{H_{2m + 2 - 2\overline k }}:5z}\end{array}} \right. + {O_2}: + 0,3125mol\)
\( \to \left\{ {\begin{array}{*{20}{c}}{C{O_2}:a}\\{{H_2}O:b}\\{{N_2}:0,5z}\end{array}} \right. + NaOH \to \Delta m = 12,89gam\)
\( \Rightarrow \left\{ {\begin{array}{*{20}{c}}{{m_{C{O_2}}} + {m_{{H_2}O}} = \Delta m = 12,892}\\{{m_{C{O_2}}} + {m_{{H_2}O}} = 2{n_{{O_2}}}(BTNT)}\end{array}} \right.\)
\( \Rightarrow \left\{ {\begin{array}{*{20}{c}}{44a + 18b = 12,892}\\{a + b = 2.0,3125}\end{array}} \right. \Rightarrow \left\{ {\begin{array}{*{20}{c}}{a = 0,205}\\{b = 0,215}\end{array}} \right.\)
\[{m_Z} = {m_C} + {m_H} + {m_N} \Rightarrow {m_N} = 3,17 - (12.0,205 + 2.0,215) = 0,28gam\]
\[ \Rightarrow {n_N} = 0,02mol \Rightarrow z = 0,02 \Rightarrow {n_Y} = 5z = 0,1\]
\[{n_{{H_2}O}} - {n_{C{O_2}}} = 0,01 = 1,5z + 5z.(1 - \overline k ) \Rightarrow \overline k = 1,2\]
\[{n_Z} = 6z = 0,12mol \Rightarrow \overline C = \frac{{{n_{CO2}}}}{{{n_Z}}} = 1,708;\overline H = \frac{{{n_H}}}{{{n_Z}}} = 3,583\]
Vì X chứa 2 amin C2H7N và C3H9N, đều có số nguyên tử C >1,708 và H >3,583
→ Y chứa một hiđrocacbon có số nguyên tử C < 1,708 → Y chứa CH4
.Hai hiđrocacbon trong Y có số liên kết pi nhỏ hơn 3, mà CH4(k=0) và = 1,2
→ hiđrocacbon còn lại Y2có k = 2 và số nguyên tử H < 3,583 → Y2
: C2H2\[\overline k = 1,2 \Rightarrow \frac{{{n_{CH4}}(k = 0)}}{{{n_{{Y_2}}}(k = 2)}} = \frac{{|2 - 1,2|}}{{|0 - 1,2|}} = \frac{2}{3}\]
\[ \Rightarrow {n_{C{H_4}}} = 2z = 0,04;{n_{{Y_2}}} = 0,06mol\]
\[{n_{C{O_2}}} = 0,205 = n.x + {n_{C{H_4}}} + 2{n_{{C_2}{H_2}}} \Rightarrow n = \frac{{0,205 - 0,04 - 2.0,06}}{{0,02}} = 2,25\]
X\(\left\{ {\begin{array}{*{20}{c}}{{C_2}{H_7}N:x}\\{{C_3}{H_9}N:y}\end{array}} \right. \Rightarrow \left\{ {\begin{array}{*{20}{c}}{x + y = 0,02}\\{2x + 3y = 2,25.0,02 = {n_C}}\end{array}} \right. \Rightarrow \left\{ {\begin{array}{*{20}{c}}{x = 0,015}\\{y = 0,005}\end{array}} \right.\)
\[ \Rightarrow \% {C_2}{H_7}N(X) = 0\frac{{,015.45}}{{0,015.45 + 0,005.59}}.100\% = 69,59\% \]
Đáp án cần chọn là: B
Câu 43:
 Xem đáp án
Xem đáp án
\[TN1:1,22gX + HCl:0,04mol \to \Rightarrow {n_{N(hh1)}} = {n_{HCl}} = 0,04mol.\]
TN2:0,09molX + O2 \( \to \left\{ {\begin{array}{*{20}{c}}{C{O_2}}\\{{H_2}O}\\{{N_2}}\end{array}} \right. + Ba{(OH)_2}\)
\( \to \left\{ {\begin{array}{*{20}{c}}{mg \downarrow BaC{O_3}}\\{0,06mol \uparrow }\end{array}} \right.\)
\[ \Rightarrow {n_{{N_2}}} = 0,06 \Rightarrow {n_{N(hh2)}} = 0,12mol = 3{n_{N(hh1)}}\]
\[ \Rightarrow {m_{X(TN2)}} = 3{m_{X(TN1)}} = 3,66gam.\]Ntb= 0,12/0,09 = 4/3 → X có chứa 1 amin đơn chức RNH2(a mol); amin còn lại là amin đa chức R’(NH2)n(b mol) (Xét trong 3,66 gam X)
Tỉ lệ mol của 2 amin là 1: 2 → có 2 TH:
\[ + TH1:\left\{ {\begin{array}{*{20}{c}}{a + b = 0,09}\\{b = 2a}\end{array}} \right. \Rightarrow \left\{ {\begin{array}{*{20}{c}}{a = 0,03}\\{b = 0,06}\end{array}} \right.\]
\[ \Rightarrow {n_N} = 0,12 = 0,03.1 + 0,06.n \Rightarrow n = 1,5(loai)\]
\[ + TH2:\left\{ {\begin{array}{*{20}{c}}{a + b = 0,09}\\{a = 2b}\end{array}} \right. \Rightarrow \left\{ {\begin{array}{*{20}{c}}{a = 0,06}\\{b = 0,03}\end{array}} \right.\]
\( \Rightarrow \left\{ {\begin{array}{*{20}{c}}{{n_N} = 0,12 = 0,06.1 + 0,03.n}\\{0,06(R + 16) + 0,03(R\prime + 16n) = 3,66}\end{array}} \right.\)
\( \Rightarrow \left\{ {\begin{array}{*{20}{c}}{n = 22}\\{R + R\prime = 58}\end{array}} \right.\)
\( \Rightarrow \left\{ {\begin{array}{*{20}{c}}{n = 2}\\{R = 15;R\prime = 28}\end{array}} \right.\)
\( \Rightarrow X\left\{ {\begin{array}{*{20}{c}}{C{H_3}N{H_2}:0,06mol}\\{{C_2}{H_4}{{(N{H_2})}_2}:0,03mol}\end{array}} \right. + {O_2} \to 0,12molC{O_2} + Ba{(OH)_2} \to mgBaC{O_3}\)
⇒m = 0,12.197 = 23,64gam
Đáp án cần chọn là: A
Câu 44:
 Xem đáp án
Xem đáp án
5,46gE\(\left\{ {\begin{array}{*{20}{c}}{{C_n}{H_{2n - 2}}:x}\\{{C_m}{H_{2m + 3}}N:y}\end{array}} \right. + {O_2}:0,495mol \to \left\{ {\begin{array}{*{20}{c}}{C{O_2}:a}\\{{H_2}O:a}\\{{N_2}}\end{array}} \right.\)
\[BTNToxi:2n{O_2} = 2{n_{C{O_2}}} + {n_{{H_2}O}} \Rightarrow 0,495.2 = 2a + a \Rightarrow a = 0,33mol\]
\[5,46 = {m_E} = {m_C} + {m_H} + {m_N} = 0,33.12 + 0,33.2 + {m_N}\]
\[ \Rightarrow {m_N} = 0,84 \Rightarrow y = 0,06mol\]\[{n_{{H_2}O}} - {n_{C{O_2}}} = 0 \Rightarrow x = 1,5y = 0,09mol\]
\(\left\{ {\begin{array}{*{20}{c}}{nx + my = nCO2 = 0,33}\\{2 < n < 3}\end{array}} \right. \Rightarrow \left\{ {\begin{array}{*{20}{c}}{0,09n + 0,06m = 0,33}\\{2 < n < 3}\end{array}} \right.\)
\[ \Rightarrow 1 < m < 2,5 \Rightarrow n = 2 \Rightarrow Amin:{C_2}{H_7}N\]
Đáp án cần chọn là: A
