Đề trắc nghiệm tổng ôn môn Hóa lớp 12 Cánh diều (Đề số 5)
-
136 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
 Xem đáp án
Xem đáp án
Chọn đáp án B
Câu 2:
Cobalt(II) chloride màu xanh được tẩm vào mảnh giấy lọc. Khi giấy này tiếp xúc với mẫu vật có nước thì giấy chuyển từ màu xanh sang màu hồng do hình thành phức chất aqua của Co(II) có dạng hình học là bát diện. Với mô tả trên thì phát biểu nào dưới đây là không đúng?
 Xem đáp án
Xem đáp án
Chọn đáp án C
Câu 3:
Acetic acid là một acid yếu, ở 25 °C, hằng số cân bằng của acid này là 1,75.10-5. Giá trị pH của dung dịch CH3COOH 0,1 M gần nhất với giá trị pH của
 Xem đáp án
Xem đáp án
Chọn đáp án C
Câu 4:
 Xem đáp án
Xem đáp án
Chọn đáp án C
Câu 5:
X là alcohol no, mạch hở, có nhiều ứng dụng trong mĩ phẩm, thực phẩm. Trong phân tử có phần trăm khối lượng carbon và hydrogen lần lượt bằng 39,13% và 8,70%, còn lại là oxygen. Phát biểu nào sau đây về X là không đúng?
 Xem đáp án
Xem đáp án
Chọn đáp án D
Câu 6:
Tách kim loại kẽm từ khoáng vật sphalerite (ZnS) bằng phương pháp nhiệt luyện thường được tiến hành theo hai bước chính ZnS(s) → X(s)→ Zn(g) theo nguyên tắc
 Xem đáp án
Xem đáp án
Chọn đáp án C
Câu 7:
Xét phản ứng sau: X(s) + FeSO4(aq) → XSO4(aq) + Fe. X là kim loại nào sau đây?
 Xem đáp án
Xem đáp án
Chọn đáp án B
Câu 8:
Cho các dung dịch riêng rẽ của các chất sau: methylamine, aniline, glycine, glutamic acid. Dung dịch làm đổi màu quỳ tím thành đỏ là dung dịch của
 Xem đáp án
Xem đáp án
Chọn đáp án B
Câu 9:
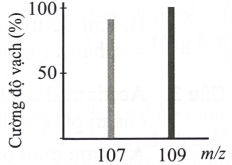
Cho biết phổ khối lượng (MS) của bạc như hình bên (z = 1), tính nguyên tử khối trung bình của bạc. Biết cường độ vạch 107Ag bằng 92% cường độ của vạch 109Ag và tỉ lệ số nguyên tử tỉ lệ với cường độ vạch.
 Xem đáp án
Xem đáp án
Chọn đáp án D
Câu 10:
Đặc điểm nào sau đây không phải là của các muối nitrate của kim loại nhóm IIA?
 Xem đáp án
Xem đáp án
Chọn đáp án C
Câu 11:
Thuỷ phân ester E có công thức phân tử C4H8O2 với xúc tác acid vô cơ loãng, thu được hai sản phẩm hữu cơ X và Y. Từ X có thể điều chế trực tiếp ra Y. Ester E có tên là
 Xem đáp án
Xem đáp án
Chọn đáp án B
Câu 12:
Phản ứng chuyển từ chất R thành chất T có giá trị biến thiên enthalpy âm và đi qua giai đoạn tạo chất trung gian S duy nhất như sau:
R → S H > 0; S→T H<0
Tiến trình phản ứng trên được minh hoạ theo sơ đồ nào dưới đây ?
 Xem đáp án
Xem đáp án
Chọn đáp án B
Câu 13:
Khi bảo quản thực phẩm trong tủ lạnh, người ta thường sử dụng hộp kín. Có bao nhiêu phát biểu dưới đây là đúng về mục đích của việc này?
(a) Hạn chế sự xâm nhập của vi sinh vật ở xung quanh vào thực phẩm.
(b) Giảm tốc độ bay hơi của nước từ thực phẩm.
(c) Giảm tốc độ oxi hoá thực phẩm.
(d) Hạn chế sự phát triển của vi khuẩn trong thực phẩm.
 Xem đáp án
Xem đáp án
Chọn đáp án D
Câu 15:
 Xem đáp án
Xem đáp án
Chọn đáp án A
Câu 16:
Trong phân tử hydrocarbon X, phần trăm khối lượng carbon bằng 83,33%. Phát biểu nào về X sau đây là đúng?
 Xem đáp án
Xem đáp án
Chọn đáp án C
Câu 17:
Sự phát triển của công nghệ tạo ra nhiều phương pháp tổng hợp polymer nhằm phục vụ đời sống, bên cạnh việc khai thác các polymer sẵn có từ thiên nhiên. Phát biểu nào sau đây về các phương pháp điều chế polymer là đúng?
 Xem đáp án
Xem đáp án
Chọn đáp án C
Câu 20:
 Xem đáp án
Xem đáp án
Đúng
Câu 21:
c. Thiếu nước ảnh hưởng đến khả năng vận chuyển oxygen và chất dinh dưỡng đến các tế bào.
 Xem đáp án
Xem đáp án
Đúng
Câu 22:
d. Nước lưu giữ các phân tử methane ở các mỏ dầu do sự tạo liên kết hydrogen với khí methane.
 Xem đáp án
Xem đáp án
Sai
Câu 25:
d. Chất X có cả liên kết cộng hoá trị theo kiểu cho – nhận và kiểu ghép đôi electron, không có liên kết ion.
 Xem đáp án
Xem đáp án
Sai
Câu 26:
 Xem đáp án
Xem đáp án
Sai
Câu 27:
 Xem đáp án
Xem đáp án
Đúng
Câu 28:
b. Khi cho acetone vào dung dịch iodine trong NaOH thấy có kết tủa màu vàng xuất hiện.
 Xem đáp án
Xem đáp án
Đúng
Câu 29:
 Xem đáp án
Xem đáp án
Đúng
Câu 32:
b. Thuỷ phân hoàn toàn các disaccharide đều thu được hỗn hợp glucose và fructose.
 Xem đáp án
Xem đáp án
Sai
Câu 33:
c. Để phân biệt các dung dịch riêng rẽ của glucose, fructose có thể dùng nước bromine làm thuốc thử.
 Xem đáp án
Xem đáp án
Đúng
Câu 34:
d. Thuỷ phân hoàn toàn tinh bột và cellulose đều thu được cùng một sản phẩm là glucose.
 Xem đáp án
Xem đáp án
Đúng
Câu 35:
Trong quá trình luyện quặng pyrite (90% FeS2 về khối lượng), lượng sulfur dioxide sinh ra được tận dụng để sản xuất sulfuric acid theo sơ đồ sau:
pyrite (1)→ sulfur dioxide (2)→ sulfur trioxide (3)→ sulfuric acid.
Biết hiệu suất của các quá trình (1), (2), (3) lần lượt là 80%, 60% và 90%. Từ 1 tấn quặng pyrite ban đầu, khối lượng sulfuric acid 98% tổng hợp được là bao nhiêu kg?
 Xem đáp án
Xem đáp án
\(4{\rm{Fe}}{{\rm{S}}_2} + 11{{\rm{O}}_2} \to 2{\rm{F}}{{\rm{e}}_2}{{\rm{O}}_3} + 8{\rm{S}}{{\rm{O}}_2}\)
\(2{\rm{S}}{{\rm{O}}_2} + {{\rm{O}}_2} \to 2{\rm{S}}{{\rm{O}}_3}\)
\({\rm{S}}{{\rm{O}}_3} + {{\rm{H}}_2}{\rm{O}} \to {{\rm{H}}_2}{\rm{S}}{{\rm{O}}_4}\)
Khối lượng H2SO4 98% là: \(\frac{{1 \cdot 0,9 \cdot 2 \cdot 98}}{{120 \cdot 0,98}} \cdot 0,8 \cdot 0,6 \cdot 0,9 = 0,648\)(tấn) = 648 kg.
Câu 36:
Một hỗn hợp gồm 0,04 mol hydrogen và 0,04 mol iodine chứa trong một bình kín có thể tích 2 dm3. Tính nồng độ hydrogen iodide khi phản ứng đạt trạng thái cân bằng ở 650 K. Biết hằng số cân bằng của phản ứng KC=64 ở 650 K. (Làm tròn kết quả đến hàng phần trăm).
 Xem đáp án
Xem đáp án
Trước phản ứng: \(\left[ {{{\rm{H}}_2}} \right] = \left[ {{{\rm{I}}_2}} \right] = \frac{{0,04}}{2} = 0,02({\rm{M}})\)
|
Ban đầu |
0,02 |
0,02 |
|
M |
|
Phản ứng |
x |
x |
2x |
M |
|
cân bằng |
0,02-x |
0,02-x |
2x |
M |
\({{\rm{K}}_{\rm{c}}} = \frac{{{{[{\rm{HI}}]}^2}}}{{\left[ {{{\rm{H}}_2}} \right]\left[ {{{\rm{I}}_2}} \right]}} = \frac{{{{(2{\rm{x}})}^2}}}{{(0,02 - {\rm{x}})(0,02 - {\rm{x}})}} = 64\)
\( \Rightarrow {\rm{x}} = 0,016{\rm{M}} \Rightarrow [{\rm{HI}}] = 2{\rm{x}} = 0,032\)M. Làm tròn: \([{\rm{HI}}] = 0,03{\rm{M}}\)
Câu 37:
NO là một chất khí độc, có thể bị loại bỏ nhờ phản ứng sau đây:
2H2(g) + 2NO(g) → 2H2O(g) + N2(g)
Tốc độ của phản ứng này có dạng v=k[H2][NO]2.
Giữ nguyên nhiệt độ, để tăng tốc độ loại bỏ NO, người ta tăng gấp 2 nồng độ H2, hỏi tốc độ phản ứng loại bỏ NO tăng lên bao nhiêu lần?
 Xem đáp án
Xem đáp án
Đáp án: 2
Câu 38:
Cho các thuốc thử: nước bromine, nước, dung dịch NaOH. Để phân biệt các chất lỏng riêng rẽ là ethanol, dung dịch phenol và diethyl ether có thể dùng bao nhiêu thuốc thử trong các thuốc thử đã cho?
 Xem đáp án
Xem đáp án
Dùng bromine. Vì ethanol tan trong nước bromine; diethyl ether ít tan nên tách lớp; phenol tạo kết tủa trắng.
Đáp án: 1
