310 câu Lý thuyết Crom - Sắt - Đồng có lời giải chi tiết (P5)
-
11090 lượt thi
-
30 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
Sản phẩm của phản ứng nhiệt phân hoàn toàn AgNO3 là
 Xem đáp án
Xem đáp án
Chọn đáp án B
Nhiệt phân hoàn toàn AgNO3:
Câu 2:
Cho Fe tác dụng với dung dịch H2SO4 loãng tạo thành khí X; nhiệt phân tinh thể KNO3 tạo thành khí Y; cho tinh thể KMnO4 tác dụng với dung dịch HCl đặc tạo thành khí Z. Các khí X, Y và Z lần lượt là
 Xem đáp án
Xem đáp án
Chọn đáp án C
Nhiệt phân KNO3:
Vậy các khí X, Y, Z lần lượt là H2, O2, Cl2.
Câu 3:
Có 4 dung dịch muối riêng biệt: CuCl2, ZnCl2, FeCl3, AlCl3. Nếu thêm dung dịch KOH (dư) vào 4 dung dịch trên, thêm tiếp dung dịch NH3 đặc (dư) vào thì sau khi kết thúc các phản ứng số chất kết tủa thu được là
 Xem đáp án
Xem đáp án
Chọn đáp án D
Cho KOH dư lần lượt vào các chất sau, sau đó lại thêm NH3 dư vào, ta có PTHH
|
1. CuCl2 |
|
|
2. ZnCl2 |
|
|
3. FeCl3 |
|
|
4. AlCl3 |
|
Vậy cuối cùng chỉ có FeCl3 là tạo kết tủa.
Câu 4:
Tổng hệ số (các số nguyên, tối giản) của tất cả các chất trong phương trình phản ứng giữa Cu với dung dịch HNO3 đặc, nóng là
 Xem đáp án
Xem đáp án
Chọn đáp án B
Tổng hệ số tất cả các chất trong phương trình là: 1 + 4 + 1 + 2 + 2 = 10
Câu 5:
Kim loại nào sau đây không phản ứng với dung dịch H2SO4 loãng?
 Xem đáp án
Xem đáp án
Chọn đáp án C
+ Vì Cu đứng sau H trong dãy hoạt động hóa học.
⇒ Cu không tác dụng với H2SO4 loãng ⇒ Chọn C
Câu 6:
Cặp chất không xảy ra phản ứng hóa học là
 Xem đáp án
Xem đáp án
Chọn đáp án D
Ta có dãy điện hóa:
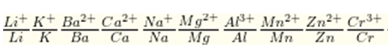
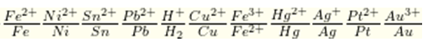
⇒ Cu không tác dụng với dung dịch muối Fe2+ ⇒ Chọn D
Câu 7:
Cho dung dịch muối X đến dư vào dung dịch muối Y, thu được kết tủa Z. Cho Z vào dung dịch HNO3 (loãng, dư), thu được chất rắn T và khí không màu hóa nâu trong không khí. Hai muối X và Y lần lượt là
 Xem đáp án
Xem đáp án
Chọn đáp án C
Hòa tan Z vào HNO3 dư vẫn có chất rắn T không tan ⇒ T là AgCl
⇒ Z gồm Ag và AgCl.
⇒ Chọn A vì: FeCl2 + 2AgNO3 → Fe(NO3)2 + 2AgCl↓
Sau đó: Fe(NO3)2 + AgNO3 → Fe(NO3)3 + Ag↓.
⇒ Chọn C
Câu 8:
Cho dung dịch muối X đến dư vào dung dịch muối Y, thu được kết tủa Z
 Xem đáp án
Xem đáp án
Chọn đáp án D
Vì CuSO4 + 2NaOH → Cu(OH)2↓xanh lam + Na2SO4
⇒ Chọn D
Câu 9:
Nhiệt phân hỗn hợp gồm NH4NO3, Cu(NO3)2, AgNO3, Fe(NO3)2 đến phản ứng hoàn toàn thì chất rắn thu được sau phản ứng là
 Xem đáp án
Xem đáp án
Chọn đáp án B
Ta có các phản ứng khi nhiệt phân như sau:
NH4NO3 → N2O↑ + 2H2O↑ (hơi nước)
2AgNO3 → 2Ag + 2NO2↑ + O2↑
4Fe(NO3)2 → 2Fe2O3 + 8NO2↑ + O2↑
2Cu(NO3)2 → 2CuO +4NO2↑ + O2↑ → 2KNO2 + O2↑
⇒ Chất rắn còn lại có Fe2O3, CuO và Ag
⇒ Chọn B
Câu 10:
Phản ứng: Cu + 2FeCl3 → 2FeCl2 + CuCl2 chứng tỏ
 Xem đáp án
Xem đáp án
Đáp án C
Phản ứng trên chứng tỏ Fe3+ có tính oxh maạnh hơn Cu2+
Câu 11:
Phản ứng nào sau đây không tạo ra muối sắt (III) ?
 Xem đáp án
Xem đáp án
Đáp án D
A → 3FeO + 10HNO3 → 3Fe(NO3)3 + NO↑ + 5H2O.
B → Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O.
C → Fe(OH)3 + 3HCl → FeCl3 + 3H2O.
D → Fe + H2SO4 loãng → FeSO4 + H2↑
Câu 12:
Cho hỗn hợp Cu và Fe2O3 vào dung dịch HCl dư. Sau khi phản ứng xảy ra hoàn toàn, thu được dung dịch X và một lượng chất rắn không tan. Muối trong dung dịch X là
 Xem đáp án
Xem đáp án
Đáp án B
Vì có kim loại dư ⇒ đó là Cu.
Ta có các phản ứng: Fe2O3 + 6HCl → 2FeCl3 + 3H2O.
Sau đó: Cu + 2FeCl3 → 2FeCl2 + CuCl2 (Vì Cu dư ⇒ FeCl3 hết).
⇒ Muối trong dung dịch X gồm có FeCl2 và CuCl2
Câu 13:
Công thức của sắt (II) hiđroxit là
 Xem đáp án
Xem đáp án
Đáp án C
Công thức của sắt (II) hiđroxit là Fe(OH)2
Câu 14:
Để thu được kim loại Cu từ dung dịch CuSO4 bằng phương pháp thủy luyện, ta không thể dùng kim loại nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án B
Để đẩy Cu ra khỏi dung dịch muối CuSO4 ta cần 1 kim loại có tính khử mạnh hơn Cu nhưng không phản ứng mãnh liệt với nước ở điều kiện thường.
⇒ Mg, Fe, Zn có thể đẩy được Cu ra khỏi muối CuSO4.
Câu 15:
Kim loại Fe tác dụng với hóa chất nào sau đây giải phóng khí H2?
 Xem đáp án
Xem đáp án
Đáp án C
Với H2SO4 đặc nóng thì sản phẩm khử có thể là SO2, S hoặc H2S.
HNO3 có thể tạo ra các sản phẩm khử: NO2, NO, N2O, N2 hoặc NH4NO3.
Câu 16:
Cho kim loại Fe lần lượt phản ứng với các dung dịch: FeCl3, Cu(NO3)2, AgNO3, MgCl2. Số trường hợp xảy ra phản ứng hóa học là:
 Xem đáp án
Xem đáp án
Đáp án B
Số dung dịch tác dụng được với Fe gồm:
FeCl3, Cu(NO3)2 và AgNO3
Câu 17:
Cho một kim loại M vào dung dịch CuSO4 dư thu được chất rắn X. Biết X tan hết trong dung dịch H2SO4 loãng và các phản ứng xảy ra hoàn toàn. Vậy M là kim loại nào trong các kim loại dưới đây?
 Xem đáp án
Xem đáp án
Đáp án D
Loại Mg và Zn vì phản ứng tạo ra Cu không tan trong H2SO4 loãng.
Loại Ba vì tạo ra kết tủa BaSO4 không tan trong H2SO4 loãng
Câu 18:
Kim loại nào sau đây không phản ứng với dung dịch CuSO4?
 Xem đáp án
Xem đáp án
Đáp án D
Chọn D do Cu2+/Cu > Ag+/Ag ⇒ Ag không khử được ion Cu2+
Câu 19:
Cho phản ứng của Fe với oxi như hình vẽ sau

Vai trò của lớp nước ở đáy bình là
 Xem đáp án
Xem đáp án
Đáp án C
Câu 20:
Thực hiện các thí nghiệm sau:
(a) Cho Fe3O4 vào dung dịch HCl.
(b) Cho Fe3O4 vào dung dịch HNO3 dư, tạo sản phẩm khử duy nhất là NO.
(c) Sục khí SO2 đến dư vào dung dịch NaOH.
(d) Cho Fe vào dung dịch FeCl3 dư.
(e) Cho hỗn hợp Cu và FeCl3 (tỉ lệ mol 1 : 1) vào H2O dư.
(f) Cho Al vào dung dịch HNO3 loãng (không có khí thoát ra).
Sau khi các phản ứng xảy ra hoàn toàn, số thí nghiệm thu được dung dịch chứa hai muối là
 Xem đáp án
Xem đáp án
Đáp án B
(a) Fe3O4 + 8HCl → 2FeCl3 + FeCl2 + 4H2O ⇒ chứa 2 muối là FeCl3 và FeCl2.
(b) 3Fe3O4 + 28HNO3 dư → 9Fe(NO3)3 + NO + 14H2O ⇒ chứa 1 muối Fe(NO3)3.
(c) NaOH + SO2 dư → NaHSO3 ⇒ chứa 1 muối NaHSO3.
(d) Fe + 2FeCl3 dư → 3FeCl2 ⇒ chứa 2 muối là FeCl2 và FeCl3 dư.
(e) Cu + 2FeCl3 → CuCl2 + 2FeCl2 ⇒ chứa 2 muối là CuCl2 và FeCl2.
(f) Do không có khí thoát ra ⇒ sản phẩm khử duy nhất của N+5 là NH4NO3.
8Al + 30HNO3 → 8Al(NO3)3 + 3NH4NO3 + 9H2O ⇒ chứa 2 muối là Al(NO3)3 và NH4NO3.
⇒ chỉ có (b) và (c) không thỏa
Câu 21:
Kim loại X phản ứng với dung dịch FeCl3, không phản ứng được với dung dịch HCl. Vậy kim loại X là
 Xem đáp án
Xem đáp án
Đáp án C
► Ta có dãy điện hóa:
Mg2+/Mg > Fe2+/Fe > H+/H2 > Cu2+/Cu > Fe3+/Fe2+ > Ag+/Ag.
||⇒ để thỏa yêu cầu đề bài thì phải nằm giữa cặp H+/H2 và Fe3+/Fe2+.
⇒ X là Đồng (Cu)
Câu 22:
Phản ứng nào sau đây viết đúng?
 Xem đáp án
Xem đáp án
Đáp án B
A. Sai, phương trình đúng: Fe + 2HCl → FeCl2 + H2↑.
B. Đúng ⇒ chọn B.
C. Sai, phương trình đúng: FeCl3 + Ag → không phản ứng.
D. Sai, phương trình đúng: Cu + 2FeCl3 → CuCl2 + 2FeCl2.
Câu 23:
Cho các phát biểu sau
(1) Các kim loại Fe, Ni, Zn đều có thể điều chế bằng phương pháp điện phân dung dịch muối của nó.
(2) Trong dung dịch Na, Fe đều khử được AgNO3 thành Ag.
(3) Cho Fe vào dung dịch FeCl3 dư sau phản ứng thu được dung dịch chứa hai muối.
(4) Hỗn hợp Na và Al có thể tan hoàn toàn trong nước.
(5) Tính oxi hóa của Ag+ > Fe3+ > Cu2+ > Fe2+.
Tổng số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án C
(1) Đúng vì các kim loại sau Al trong dãy điện hóa đều có thể điều chế bằng phương pháp điện phân dung dịch.
(2) Sai vì Na không khử được AgNO3 do tác dụng với H2O trước.
(3) Đúng vì: Fe + 2FeCl3 → 3FeCl2 ||⇒ dung dịch chứa 2 muối là FeCl2 và FeCl3 dư.
(4) Đúng vì nếu với tỉ lệ thích hợp thì: 2Na + 2H2O → 2NaOH + H2↑ || 2NaOH + 2Al + 2H2O → 2NaAlO2 + 3H2↑.
(5) Đúng.
||⇒ chỉ có (2) sai
Câu 24:
Có thể dùng một hóa chất để phân biệt Fe2O3 và Fe3O4. Hóa chất này là
 Xem đáp án
Xem đáp án
Đáp án D
Chọn D vì Fe2O3 chỉ xảy ra phản ứng trao đổi, nhưng Fe3O4 xảy ra phản ứng oxi hóa khử.
Mặt khác: Fe3O4 có tính khử trung bình ⇒ sản phẩm khử là chất khí ⇒ phân biệt được!.
Câu 25:
Hòa tan hoàn toàn Fe3O4 trong dung dịch HCl (dư) thu được dung dịch X. Cho lượng dư bột Fe vào dung dịch X (trong điều kiện không có không khí) đến khi phản ứng xảy ra hoàn toàn, thu được dung dịch Y chứa chất tan là
 Xem đáp án
Xem đáp án
Đáp án B
Fe3O4 + 8HCl → 2FeCl3 + FeCl2 + 4H2O.
||⇒ dung dịch X chứa FeCl2, FeCl3 và HCl dư.
► Fe DƯ + dung dịch X thì:
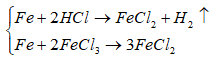
||⇒ dung dịch Y chỉ chứa chất tan là FeCl2
Câu 26:
Cho hỗn hợp Fe(NO3)2 và Al2O3 vào dung dịch H2SO4 (loãng, dư) thu được dung dịch X. Cho dung dịch KOH dư vào X thu được kết tủa Y. Kết tủa Y có
 Xem đáp án
Xem đáp án
Đáp án D
6Fe(NO3)2 + 9H2SO4 → 10HNO3 + 3Fe2(SO4)3 + NO + 4H2O.
Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O.
||⇒ KOH DƯ + X thì chỉ thu được ↓ là Fe(OH)3 (do Al(OH)3 tan trong KOH dư)
Câu 28:
Có 2 kim loại X, Y thỏa mãn các tính chất sau:
|
Dung dịch |
Kim loại |
|
|
X |
Y |
|
|
HCl |
Tác dụng |
Tác dụng |
|
HNO3 đặc nguội |
Không tác dụng |
Tác dụng |
X, Y lần lượt là
 Xem đáp án
Xem đáp án
Đáp án C
X không tác dụng với HNO3 đặc nguội ⇒ Loại A.
Y không tác dụng với HNO3 đặc nguội ⇒ Loại B và D
