Bộ 20 đề thi học kì 1 Hóa 12 có đáp án_ đề 14
-
3699 lượt thi
-
30 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
Este có công thức cấu tạo: CH2=CHCOOC2H5 có tên gọi là
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Cho este R-COO-R’
- Nếu gốc ancol là đơn chức: Tên este = tên gốc hiđrocacbon R’ + tên gốc axit (“ic” → “at”)
- Nếu gốc ancol là đa chức: Tên este = tên ancol + tên gốc axit (“ic” → “at”)
Giải chi tiết:
Este CH2=CHCOOC2H5 có tên gọi là etyl acrylat
Câu 2:
Chất nào sau đây được dùng trong y học để chế tạo “xi măng sinh học”, làm răng giả?
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Plexiglas có những tính chất ưu việt nên được dùng làm kính máy bay, ô tô, kính trong các máy móc nghiên cứu, kính xây dựng, đồ dùng gia đình, trong y học (dùng làm răng giả, xương giả), kính bảo hiểm,…
Giải chi tiết:
Poli (metyl metacrylat) (thủy tinh hữu cơ plexiglas) được ứng dụng trong y học để chế tạo “xi măng sinh học”, làm răng giả.
Câu 3:
Chất nào sau đây thuộc loại amin đơn chức bậc hai?
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Bậc của amin được tính bằng số nguyên tử H trong phân tử NH3 được thay thế bằng gốc hiđrocacbon. Theo đó các amin được phân loại thành: amin bậc I, amin bậc II và amin bậc III
Giải chi tiết:
CH3NH2 và H2NCH2CH2NH2 là amin bậc I
(CH3)2NH là amin bậc II
(CH3)3N là amin bậc III
Câu 4:
Trong các kim loại: Al, Cu, Fe và Ag. Kim loại có tính dẫn điện cao nhất là
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
Các kim loại dẫn điện tốt nhất theo thứ tự giảm dần: Ag, Cu, Au, Al, Fe,…
Giải chi tiết:
Kim loại có tính dẫn điện cao nhất là Ag
Câu 5:
Cacbohiđrat nào sau đây thủy phân trong môi trường axit thu được 2 sản phẩm?
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Saccarozơ thủy phân khi có mặt axit xúc tác sinh ra 1 phân tử glucozơ và 1 phân tử fructozơ
Mantozơ thủy phân khi có mặt axit xúc tác sinh ra 2 phân tử glucozơ
Tinh bột và xenlulozơ thủy phân hoàn toàn khi có mặt axit xúc tác sinh ra các phân tử glucozơ
Giải chi tiết:
Tinh bột và xenlulozơ thủy phân hoàn toàn khi có mặt axit xúc tác sinh ra các phân tử glucozơ
Saccarozơ thủy phân khi có mặt axit xúc tác sinh ra 1 phân tử glucozơ và 1 phân tử fructozơ
Fructozơ không bị thủy phân
Câu 6:
α-amino axit nào sau đây làm quỳ tím hóa xanh?
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Hợp chất có dạng (NH2)xR(COOH)y
+ Nếu x < y → dung dịch có môi trường axit → quỳ tím chuyển đỏ
+ Nếu x > y → dung dịch có môi trường bazơ → quỳ tím chuyển xanh
+ Nếu x = y → dung dịch có môi trường trung tính → không đổi màu quỳ tím
Giải chi tiết:
H2NCH2COOH không làm đổi màu quỳ tím
H2NCH2CH2CH(NH2)COOH và H2NCH2CH(NH2)CH2COOH làm quỳ tím chuyển sang màu xanh
Nhưng đề cho α-amino axit nên là H2NCH2CH2CH(NH2)COOH
Câu 7:
Với lượng dư dung dịch nào sau đây tác dụng với kim loại sắt không tạo thành muối sắt (III)?
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Viết phương trình hóa học và kết luận.
Giải chi tiết:
Câu 8:
Cho các dung dịch: glixerol, abumin, saccarozơ, glucozơ. Số dung dịch phản ứng với Cu(OH)2 trong môi trường kiềm là
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Các chất có khả năng phản ứng với Cu(OH)2 trong môi trường kiềm
+ Tripeptit trở lên
+ Protein
+ Các chất có nhóm OH- kề nhau
+ Có nhóm chức CHO trong phân tử
Giải chi tiết:
Abumin là phản ứng màu biure thu được dung dịch có màu xanh tím
Glixerol, saccarozơ, glucozơ tạo phức xanh do phân tử có nhiều nhóm OH- kề nhau.
Câu 9:
Công thức phân tử của axit 2,6 – điaminohexanoic là
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
- Viết công thức cấu tạo
- Kết luận công thức phân tử
Giải chi tiết:
2,6-điaminohexanoic có công thức cấu tạo H2NCH2CH2CH2CH2CH(NH2)COOH
→ CTPT: C6H14N2O2
Câu 10:
Chất hữu cơ X (chứa vòng benzen) có công thức là CH3COOCH2C6H4OH. Khi đun nóng, a mol X tác dụng được với tối đa bao nhiêu mol NaOH trong dung dịch?
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
- Viết PTHH
- Kết luận
Giải chi tiết:
Vậy nNaOH = 2nX = 2a (mol)
Câu 11:
Thủy phân hoàn toàn 1 mol pentapeptit X, thu được 2 mol Gly, 2 mol Ala và 1 mol Val. Nếu thủy phân không hoàn toàn X thì thu được hỗn hợp sản phẩm trong đó có Ala-Gly-Ala, Gly-Val, nhưng không có Val-Ala. Amino axit ở đầu X và đầu N trong X tương ứng là
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
- Xác định số lượng các mắt xích có trong X
- Xác định thứ tự các mắt xích trong X
- Kết luận.
Giải chi tiết:
X có dạng (Gly)2(Ala)2(Val)
Trong X có các đoạn Ala-Gly-Ala, Gly-Val nhưng không có đoạn Val-Ala
→ X là Ala-Gly-Ala-Gly-Val
→ Amino axit đầu C và đầu N lần lượt là Val và Ala
Câu 12:
Phản ứng nào sau đây là phản ứng điều chế kim loại theo phương pháp thủy luyện?
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Cơ sở của phương pháp thủy luyện: Dùng những dung dịch thích hợp để hòa tan kim loại hoặc hợp chất của kim loại và tách ra phần không tan. Sau đó dùng các kim loại mạnh hơn (như Mg, Al) để khử ion kim loại thành kim loại cần điều chế.
Giải chi tiết:
Đáp án A điều chế kim loại bằng phương pháp thủy luyện
Đáp án B, D điều chế kim loại bằng phương pháp điện phân
Đáp án C điều chế kim loại bằng phương pháp nhiệt luyện
Câu 13:
Lòng trắng trứng là chất dịch không màu hoặc màu trắng ngà bên trong một quả trứng (trứng gà, trứng vịt). Lòng trắng trứng là nguồn thực phẩm giàu protein, bị đông tụ khi đun nóng hoặc tác dụng với axit, bazơ và một số muối. Lòng trắng trứng chứa loại protein nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Giải chi tiết:
Abumin có trong lòng trắng trứng
Câu 14:
Thể tích khí H2 (đktc) cần dùng để tác dụng vừa đủ với 0,1 mol triolein là
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
- Viết PTHH
- Tính số mol H2
- Tính thể tích H2
Giải chi tiết:
PTHH:
Theo phương trình hóa học:
Câu 15:
Cho m gam hỗn hợp X gồm axit fomic và metyl fomat (có tỷ lệ mol 1:1) tác dụng với lượng dư AgNO3 trong môi trường NH3, thu được 43,2 gam kim loại Ag. Phần trăm khối lượng của metyl fomat có trong hỗn hợp X là
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
- Giả sử số mol các chất ban đầu là 1 mol
- Tính % khối lượng các chất trong hỗn hợp X.
Giải chi tiết:
Giả sử số mol của axit fomic và metyl fomat đều là 1 mol
Câu 16:
Đốt cháy hoàn toàn m gam hỗn hợp gồm Cu, Fe cần vừa đủ 4,48 lít khí Cl2 (đktc), thu được 23 gam hỗn hợp muối. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
- Tính số mol và khối lượng của khí Cl2
- Áp dụng bảo toàn khối lượng tìm m.
Giải chi tiết:
Áp dụng bảo toàn khối lượng: mFe + mCu + mCl2 = mmuối
→ m + 14,2 = 23 → m = 8,8
Câu 17:
Polime nào sau đây không được tổng hợp bằng phản ứng trùng ngưng?
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
- Trùng hợp là quá trình kết hợp nhiều phân tử nhỏ (monome), giống nhau hay tương tự nhau thành phân tử rất lớn (polime)
- Trùng ngưng là quá trình kết hợp nhiều phân tử nhỏ (monome) thành phân tử lớn (polime) đồng thời giải phóng những phân tử nhỏ khác (như H2O…)
Giải chi tiết:
Tơ nitron không được tổng hợp bằng phản ứng trùng ngưng
Câu 18:
Đốt cháy hoàn toàn amin đơn chức X, thu được 4,48 lít CO2 (đktc); 6,3 gam H2O và 1,12 lít N2 (đktc). Công thức phân tử của X là
 Xem đáp án
Xem đáp án
Đáp án C
Bảo toàn nguyên tố N:
Số C =
Số H =
Vậy X là C2H7N.
Câu 19:
Đốt cháy hoàn toàn 13,728 gam triglixerit X, thu được a mol hỗn hợp Y gồm CO2 và H2O. Cho toàn bộ hỗn hợp Y qua cacbon nung đỏ, thu được 2,364 mol hỗn hợp Z gồm CO, H2 và CO2. Cho hỗn hợp Z qua dung dịch Ba(OH)2 dư thu được 202,516 gam kết tủa. Cho 13,728 gam X tác dụng được tối đa với 0,032 mol Br2 trong dung dịch. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án C
Giải chi tiết:
Dẫn hỗn hợp Z qua dung dịch Ba(OH)2 dư thì
mol
Xét quá trình trao đổi electron của phản ứng giữa C với CO2 và H2O
C → C+4 + 4eC+4 + 2e → C+2
2H+ + 2e → H2
Áp dụng bảo toàn electron:
→ a = 2,364 – 0,668 = 1,696 mol
Quy đổi hỗn hợp X thành (HCOO)3C3H5 (x mol), CH2 (y mol) và H2 (-0,032 mol)
→ mX = 176x + 14y – 0,032.2 = 13,728 (1)
(2)
Từ (1) và (2) → x = 0,016 mol; y = 0,784 mol
Ta có: nNaOH = 3x = 0,048 mol;
Áp dụng bảo toàn khối lượng cho phản ứng: mX + mNaOH = mmuối + mglixerol
→ mmuối = 13,728 + 0,048.40 – 92.0,016 = 14,176 gam
Câu 20:
Cho m gam bột sắt vào dung dịch HNO3, sau khi phản ứng hoàn toàn, thu được 2,24 lít khí NO (sản phẩm khử duy nhất của N+5 ở đktc) và 2,4 gam chất rắn. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án D
Vì sau phản ứng còn dư 2,4 gam chất rắn nên muối thu được là muối sắt (II)
Áp dụng bảo toàn electron: 2nFe pu = 3nNO
→ nFe pu = 0,15 mol → mFe pu = 0,15.56 = 8,4 gam
→ m = 8,4 + 2,4 = 10,8 gam
Câu 21:
Cho các sơ đồ phản ứng sau:
X (C8H14O4) + 2NaOH → X1 + X2 + H2O
X1 + H2SO4 → X3 + Na2SO4
nX5 + nX3 → poli (hexametylen ađipamit) + 2nH2O
2X2 + X3 ⇄ X6 + 2H2O
Phân tử khối của X6 là
 Xem đáp án
Xem đáp án
Đáp án D
Từ phản ứng (2) và (3) → X3 là C4H8(COOH)2
Từ phản ứng (1) → X là C2H5OOC-C4H8-COOH
→ X2 là C2H5OH
→ X6 là C4H8(COOC2H5)2
Câu 22:
Kết quả thí nghiệm của các chất X, Y, Z với các thuốc thử được ghi ở bảng sau: 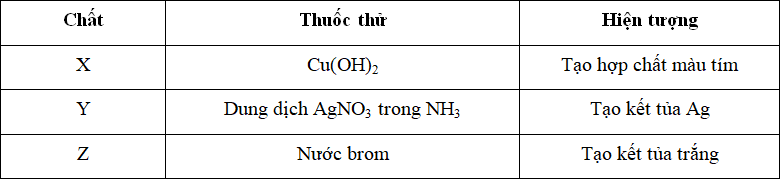
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
- Chất tạo phức màu tím với Cu(OH)2 là tripeptit trở lên
- Chất tác dụng với AgNO3 trong NH3 tạo kết tủa Ag phải có nhóm CHO
- Chất tác dụng với nước brom tạo kết tủa trắng là phenol hoặc anilin
Giải chi tiết:
Chất X tác dụng với Cu(OH)2 tạo hợp chất màu tím → X là Gly – Ala – Gly
Chất Y tác dụng với dung dịch AgNO3 trong NH3 tạo kết tủa Ag → Y là etyl fomat
Chất Z tác dụng với nước brom tạo kết tủa trắng → Z là anilin
Câu 23:
Cho hỗn hợp X gồm Gly, Ala, Val và Glu. Để tác dụng hết với 0,2 mol X cần 100 ml dung dịch chứa hỗn hợp gồm NaOH 1M và KOH 1,4M. Đốt cháy hoàn toàn 0,2 mol X cần V lít O2 (đktc), hấp thụ sản phẩm cháy vào dung dịch NaOH dư, khối lượng dung dịch sau phản ứng tăng 56,88 gam. Giá trị của V là
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
- Quy đổi hỗn hợp thành C2H5NO, CH2 và CO2
- Lập phương trình biểu diễn số mol bazơ (1)
- Lập phương trình tổng khối lượng CO2 và H2O (2)
- Từ (1) và (2) tìm được số mol các chất
- Tính số mol O2
- Tính V
Giải chi tiết:
Quy đổi X thành C2H5NO (0,2 mol), CH2 (a mol) và CO2 (b mol)
→ 0,2 + b = 0,24 (1)
(2)
Từ (1) và (2) → a = 0,46; b = 0,04
→ V = 1,14.22,4 = 25,536 lít
Câu 24:
Ancol etylic được điều chế bằng cách lên men tinh bột theo sơ đồ sau:
(C6H10O5)n → C6H12O6 → C2H5OH
Để điều chế 10 lít ancol etylic 46o cần m kg gạo (chứa 75% tinh bột, còn lại là tạp chất). Biết hiệu suất của cả quá trình là 80% và khối lượng riêng của ancol etylic nguyên chất là 0,8 g/ml. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
- Tính thể tích C2H5OH
- Tính khối lượng C2H5OH
- Tính số mol C2H5OH
- Suy ra số mol tinh bột
- Tính khối lượng tinh bột, suy ra khối lượng gạo.
Giải chi tiết:
lít
0,04 ← 0,08
→ mgạo =
Câu 25:
Thí nghiệm điều chế và thử tính chất của khí X được thực hiện như hình vẽ:
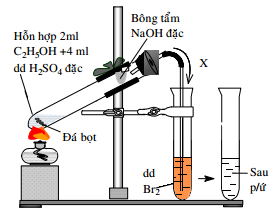
Cho các phát biểu sau về thí nghiệm trên:
(a) Đá bọt có tác dụng không cho chất lỏng trào lên trên
(b) Dung dịch NaOH có tác dụng hấp thụ khí SO2
(c) Dung dịch Br2 bị nhạt màu dần
(d) Khí X đi vào dung dịch Br2 là C2H2
(e) Nếu thay dung dịch Br2 thành dung dịch KMnO4 thì sẽ có kết tủa.
(g) Nên hơ đều bình cầu rồi sau đó mới đun tập trung.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
Dựa vào lý thuyết về tính chất và điều chế các chất hữu cơ.
Giải chi tiết:
(a) Đúng, đá bọt giúp chất lỏng sôi êm dịu hơn
(b) Đúng, SO2 là sản phẩm phụ, cần được loại bỏ
(c) Đúng
(d) Sai, X là C2H4
(e) Đúng
(g) Đúng, việc này giúp mình nóng đều, tránh bị vỡ
Câu 26:
Cho các phát biểu sau:
(a) Dầu chuối (chất tạo hương liệu mùi chuối chín) có chứa isoamyl axetat.
(b) Thủy tinh hữu cơ được ứng dụng làm cửa kính phương tiện giao thông.
(c) Glucozơ có vị ngọt thấy đầu lưỡi mát lạnh do xảy ra phản ứng lên men rượu
(d) Nhỏ dung dịch I2 vào lát cắt của củ khoai lang thì xuất hiện màu xanh tím
(e) Nicotin là một amin độc, có trong thuốc lá
(f) Sau khi lưu hóa, cao su chịu nhiệt và đàn hồi tốt hơn.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Xem lại lý thuyết tổng hợp về hóa học hữu cơ.
Giải chi tiết:
(a) Đúng
(b) Đúng
(c) Sai
(d) Đúng
(e) Đúng
(f) Đúng
Câu 27:
Hợp chất hữu cơ X (C8H15O4N) tác dụng với dung dịch NaOH dư, đun nóng, thu được sản phẩm hữu cơ gồm muối đinatri glutamat và ancol. Số công thức cấu tạo của X là
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Viết các CTCT thỏa mãn yêu cầu đề bài.
Giải chi tiết:
C8H15O4N + NaOH → NaOOC-CH2-CH2CH(NH2)COONa + ancol
Các cấu tạo của C8H15O4N
CH3CH2CH2OOCCH2CH2CH(NH2)COOH
(CH3)2CHOOCCH2CH2CH(NH2)COOH
HOOCCH2CH2CH(NH2)COOCH2CH2CH3
HOOCCH2CH2CH(NH2)COOCH(CH3)2
CH3OOCCH2CH2CH(NH2)COOC2H5
C2H5OOCCH2CH2CH(NH2)COOCH3
Câu 28:
Cho 2,7 gam hỗn hợp bột X gồm Fe và Zn tác dụng với dung dịch CuSO4. Sau mọt thời gian, thu được dung dịch Y và 2,84 gam chất rắn Z. Cho toàn bộ Z vào dung dịch H2SO4 loãng dư. Sau khi các phản ứng kết thúc thì khối lượng chất rắn giảm 0,28 gam và dung dịch thu được chỉ chứa một muối duy nhất. Phần trăm khối lượng của Fe trong X là
 Xem đáp án
Xem đáp án
Vì mZ > mX nên Zn phản ứng hết, Fe phản ứng một phần
Đặt a, b là số mol Zn và Fe đã phản ứng.
Ta có: mX = 65a + 56b + 0,28 = 2,7
Và mZ = 64(a + b) + 0,28 = 2,84
→ a = b = 0,02
Câu 29:
 Xem đáp án
Xem đáp án
Đáp án D
Mà nancol = 0,08 mol
→ ancol là CH3OH
Đặt công thức este là CnH2n+1COOCH3 (a mol) và CmH2m-1COOCH3 (b mol)
→ a = 0,06 và b = 0,02 và an + bm = 0,08
→ 3n + m = 4
Vì axit không no có đồng phân hình học nên gốc ít nhất có 3C. Vậy m = 3 và n = 1/3
Câu 30:
Cho hỗn hợp gồm hai muối có công thức C4H14O3N2 và C5H14O4N2 tác dụng với dung dịch NaOH vừa đủ (đun nóng) thu được m gam hỗn hợp X gồm hai muối Y, Z (Y là chất vô xơ, MY < MZ) và 2,24 lít (đktc) hỗn hợp E gồm hai amin no, đơn chức, kế tiếp trong dãy đồng đẳng. Tỷ khối của E so với H2 là 16,9. Khối lượng của muối Z trong X là
 Xem đáp án
Xem đáp án
Đáp án D
E gồm CH5N (0,08 mol) và C2H7N (0,02 mol)
C4H14O3N2 là CH3NH3CO3NH3C2H5 (x mol)
Do số mol của CH5N lớn hơn số mol C2H7N nên C5H14O4N2 là CH2(COONH3CH3)2 (y mol)
→ y = 0,03
Muối Z là CH2(COONa)2 (0,03 mol)
→ mZ = 4,44 gam
