Đề thi cuối kì 2 Hóa 12 có đáp án (Đề 9)
-
11674 lượt thi
-
32 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
NaHCO3không tác dụng với CO2.
NaHCO3+ HCl → NaCl + CO2+ H2O
NaHCO3+ NaOH → Na2CO3+ H2O
2NaHCO3+ 2KOH → Na2CO3+ K2CO3+ 2H2O
Câu 2:
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
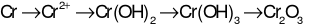


Câu 3:
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
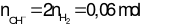
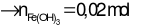
→ m = 0,02. 107 = 2,14 gam
Câu 4:
Chất không có tính chất lưỡng tính là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
AlCl3không có tính lưỡng tính.
Câu 5:
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
2Al + Cr2O3→ Al2O3+ 2Cr
Theo lí thuyết:
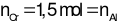
Do H = 90% nên: 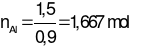
→ mAl= 45g
Câu 6:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Hai chất được dùng để làm mềm nước cứng vĩnh cửu là Na2CO3và Na3PO4
Câu 7:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
B sai, ăn mòn hóa học không phát sinh dòng điện; ăn mòn điện hóa học mới phát sinh dòng điện.
Câu 8:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
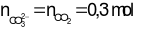
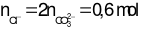
→ mKL= 32,3 – 0,6.35,5 = 11 gam
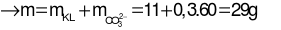
Câu 10:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
K, Na tác dụng với H2O hay với H2SO4đều sinh H2như nhau nên 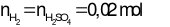
→ V = 0,448 lít
Câu 11:
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
2Al + 2NaOH + 2H2O → 2NaAlO2+ 3H2
Câu 12:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Các trường hợp thu được kết tủa là: FeCl3, CuCl2, FeSO4
Chú ý: Al(OH)3tan trong NaOH dư.
Câu 13:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
CO2+ Ca(OH)2dư → CaCO3(↓ trắng) + H2O
Câu 14:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
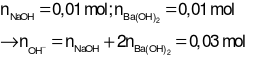
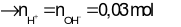
→ nHCl= 0,03 mol → VHCl= 0,1 lít = 100 ml
Câu 15:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Thêm lượng dư NaOH vào dung dịch K2Cr2O7thì dung dịch chuyển từ màu da cam sang màu vàng.
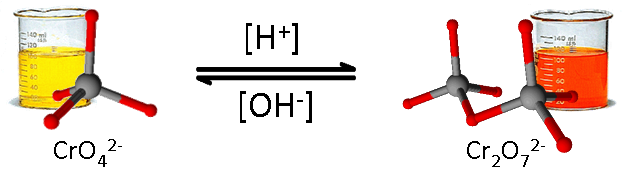
Câu 16:
Dung dịch chứa muối X không làm đổi màu quỳ tím, dung dịch chứa muối Y làm quỳ tím hóa xanh. Trộn hai dung dịch trên với nhau thấy tạo kết tủa. Vậy X và Y có thể là cặp chất nào trong các cặp chất dưới đây
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
X là Ba(NO3)2và Y là Na2CO3
Ba(NO3)2+ Na2CO3→ BaCO3↓ + 2NaNO3
Chú ý: Na2CO3là muối tạo bởi kim loại mạnh và gốc axit yếu nên bị thủy phân tạo môi trường bazơ.
Câu 17:
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Có 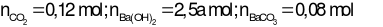
Vì  nên sản phẩm sau phản ứng gồm BaCO3và Ba(HCO3)2
nên sản phẩm sau phản ứng gồm BaCO3và Ba(HCO3)2
Áp dụng định luật bảo toàn nguyên tố cho C ta có:

Do đó 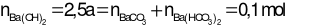
→ a = 0,04
Câu 18:
 Xem đáp án
Xem đáp án
Đáp án đúng là : A
Khí SO2và NO2đều là nguyên nhân gây mưa axit
Câu 19:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
TH1: Ba(OH)2dư, CO2hết
Ba(OH)2+ CO2→ BaCO3↓+ H2O
0,1 ← 0,1mol
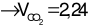 lít
lít
TH2: Ba(OH)2hết, CO2dư nhưng không hòa tan hết kết tủa
Ba(OH)2+ CO2→ BaCO3+ H2O
0,1 ← 0,1 ← 0,1mol
Ba(OH)2+ 2CO2→ Ba(HCO3)2
(0,3 - 0,1)→ 0,4
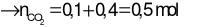
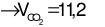 lít
lít
Câu 20:
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Để khử ion Fe3+trong dung dịch thành ion Fe2+có thể dùng một lượng dư kim loại Cu
Cu + 2Fe3+→ Cu2++ 2Fe2+
Câu 21:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Hai kim loại Al và Cu đều phản ứng được với dung dịch HNO3loãng.
Al + 4HNO3→ Al(NO3)3+ NO + 2H2O
3Cu + 8HNO3→ 3Cu(NO3)2+ 2NO + 4H2O
Câu 22:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Bảo toàn nguyên tố Fe: 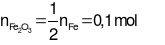
Bảo toàn nguyên tố Mg: nMgO= nMg= 0,1 mol
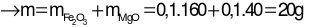
Câu 23:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Bảo toàn e: 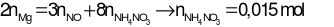
→ mmuối 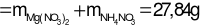
Câu 24:
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Al và Cr giống nhau ở điểm cùng bị thụ động trong HNO3đặc, nguội.
Câu 25:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Ta có: 
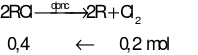
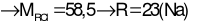
Câu 26:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Bảo toàn nguyên tố Ba: 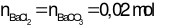
→ V = 0,01 lít
Câu 27:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Be không khử được nước ở nhiệt độ thường.
Câu 28:
D. ZnSO4
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Chất không có tính lưỡng tính là ZnSO4
Câu 29:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Để xử lý sơ bộ nước thải trên, người ta sử dụng Ca(OH)2, các ion kim loại nặng bị lắng xuống dưới dạng kết tủa:
Hg2++ 2OH-→ Hg(OH)2↓
Pb2++ 2OH-→ Pb(OH)2↓
Fe3++ 3OH-→ Fe(OH)3↓
Câu 30:
Cho phản ứng hoá học : Fe + CuSO4FeSO4+ Cu. Trong phản ứng trên xảy ra
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Fe có số oxi hóa tăng lên sau phản ứng nên đóng vai trò là chất khử, vậy Cu2+là chất oxi hóa.
Vậy trong phản ứng trên xảy ra sự oxi hoá Fe và sự khử Cu2+.



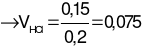 lít
lít