ĐGNL ĐH Bách khoa - Vấn đề thuộc lĩnh vực hóa học - Alkane
-
820 lượt thi
-
30 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
 Xem đáp án
Xem đáp án
Trả lời:
Ankan hoà tan tốt trong dung môi hữu cơ =>tan tốt trong benzen
Đáp án cần chọn là: B
Câu 2:
C2H6 (I)
C3H8 (II)
n-C4H10 (III)
i-C4H10 (IV)
Nhiệt độ sôi tăng dần theo dãy là :
 Xem đáp án
Xem đáp án
Trả lời:
Vì phân tử i-C4H10 có cấu trúc cồng kềnh hơn n-C4H10 nên tos nhỏ hơn: (IV) < (III)
Nhiệt độ sôi tăng dần khi tăng khối lượng phân tử =>(I) < (II) < (IV) < (III)
Đáp án cần chọn là: C
Câu 3:
Cho các chất sau :
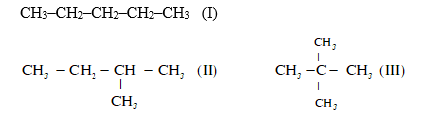
Thứ tự tăng dần nhiệt độ sôi của các chất là :
 Xem đáp án
Xem đáp án
Trả lời:
Cả 3 chất đều có 5C =>tos phụ thuộc vào cấu trúc phân tử. Phân tử càng cồng kềnh thì nhiệt độ sôi càng thấp
=>(III) có cấu trúc cồng kềnh nhất =>(III) < (II) < (I)
Đáp án cần chọn là: C
Câu 4:
 Xem đáp án
Xem đáp án
Trả lời:
Dãy sắp xếp theo nhiệt độ sôi tăng dần là: etan< propan< isobutan< butan
Đáp án cần chọn là: B
Câu 5:
 Xem đáp án
Xem đáp án
Trả lời:
Gọi công thức phân tử của ankan Y có dạng CnH2n+2
\[ \Rightarrow \% C = \frac{{12n}}{{12n + 2n + 2}}.100\% = 82,76\% \]
\[ \Rightarrow n = 4\]
=>Công thức phân tử của Y là C4H10
Đáp án cần chọn là: C
Câu 6:
Ankan Y phản ứng với clo tạo ra 2 dẫn xuất monoclo có tỉ khối hơi so với H2 bằng 46,25. Tên của Y là:
 Xem đáp án
Xem đáp án
Trả lời:
Đặt CTPT của ankan là CnH2n+2
Phản ứng của CnH2n+2 với clo tạo ra dẫn xuất monoclo :
\[{C_n}{H_{2n + 2}} + C{l_2}\mathop \to \limits^{as} {C_n}{H_{2n + 1}}Cl + HCl\] (1)
Theo giả thiết ta thấy CnH2n+1Cl gồm hai đồng phân và
\[{M_{{C_n}{H_{2n + 1}}Cl}} = 46,25.2 = 92,5gam/mol\]
=>14n + 36,5 = 92,5
=>n = 4
=>CTPT của ankan là C4H10
+) Vì phản ứng tạo 2 dẫn xuất =>X là butan hoặc isobutan
Phương trình phản ứng :
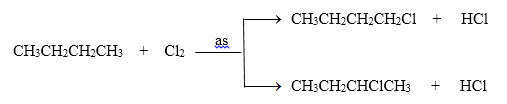
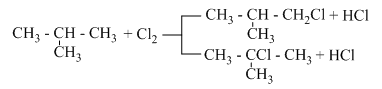
Đáp án cần chọn là: D
Câu 7:
 Xem đáp án
Xem đáp án
Trả lời:
Đặt CTPT của ankan là CnH2n+2
Phản ứng của CnH2n+2 với clo tạo ra dẫn xuất monoclo :
\[{C_n}{H_{2n + 2}} + C{l_2}\mathop \to \limits^{as} {C_n}{H_{2n + 1}}Cl + HCl\] (1)
Theo giả thiết
\[{M_{{C_n}{H_{2n + 1}}Cl}} = 53,25.2 = 106,5\]
=>14n + 36,5 = 106,5
=>n = 5
=>CTPT của ankan là C5H12
Vì phản ứng chỉ tạo ra một sản phẩm duy nhất nên ankan X là 2,2-đimetylpropan.
Phương trình phản ứng :
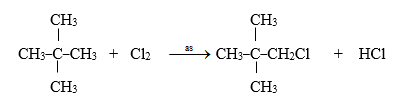
Đáp án cần chọn là: C
Câu 8:
 Xem đáp án
Xem đáp án
Trả lời:
Gọi CTTQ của ankan là CnH2n+2
CnH2n+2 + Br2 → CnH2n+1Br + HBr
M dẫn xuất = 75,5 . 2 = 151
Ta có: 14n + 81 = 151 <=>n = 5
Ankan có CTPT là C5H12
C5H12 có 3 đồng phân:
C1H3 – C2H2 – C3H2 – C4H2 – C5H3 : có 3 vị trí thế Clo (1, 2, 3), vị trí C4 giống C2 và C5 giống C1
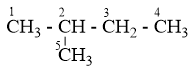
có 4 vị trí thế Clo (1, 2, 3, 4), vị trí C
5 giống C1(CH3)3C – CH3 : chỉ có 1 vị trí thế Clo vì 4 nhóm CH3 đều giống nhau
Đáp án cần chọn là: D
Câu 9:
 Xem đáp án
Xem đáp án
Trả lời:
- nCO2 = 0,4 mol; nH2O = 0,6 mol
- Áp dụng định luật bảo toàn nguyên tố: nC = nCO2 = 0,4 mol; nH = 2.nH2O = 1,2 mol
- Bảo toàn khối lượng: mankan = mC + mH = 12.0,4 + 1.1,2 = 6 gam
Đáp án cần chọn là: C
Câu 10:
 Xem đáp án
Xem đáp án
Trả lời:
nO2 = 0,275 mol ; nCO2 = 0,15 mol
Bảo toàn nguyên tố O :
\[2.{n_{{O_2}}} = 2.{n_{C{O_2}}} + {n_{{H_2}O}}\]
\[ \Rightarrow {n_{{H_2}O}} = 2.{n_{{O_2}}} - 2.{n_{C{O_2}}}\]
= 2.0,275 – 2.0,15 = 0,25 mol
Bảo toàn nguyên tố C và H : nC (trong X) = nCO2 = 0,15 mol ; nH (trong X) = 2.nH2O = 0,5 mol
Bảo toàn khối lượng : mX = mC (trong X) + mH (trong X) = 12.0,15 + 0,5 = 2,3 gam
Đáp án cần chọn là: A
Câu 11:
 Xem đáp án
Xem đáp án
Trả lời:
CO2 + Ca(OH)2 → CaCO3↓ + H2O
2CO2 + Ca(OH)2 → Ca(HCO3)2
Ca(HCO3)2 → CaCO3↓ + CO2 + H2O
Từ các phản ứng, ta có: nCO2 sinh ra = nCaCO3 + 2.nCa(HCO3)2 = 0,2 + 2.0,1 = 0,4 mol
=>số C trong
\[X = \frac{{{n_{C{O_2}}}}}{{{n_{ankan}}}} = \frac{{0,4}}{{0,2}} = 2\]
=>X không thể là CH4
Đáp án cần chọn là: C
Câu 12:
Đốt cháy hoàn toàn một lượng hiđrocacbon X. Hấp thụ toàn bộ sản phẩm cháy vào dung dịch Ba(OH)2 dư tạo ra 29,55 gam kết tủa, dung dịch sau phản ứng có khối lượng giảm 19,35 gam so với dung dịch Ba(OH)2 ban đầu. Công thức phân tử của X là
 Xem đáp án
Xem đáp án
Trả lời:
mdung dịch giảm = mkết tủa – (mCO2 + mH2O) =>mCO2 + mH2O = mkết tủa - mdung dịch giảm = 29,55 – 19,35 = 10,2 gam
Bảo toàn nguyên tố C: nC = nCO2 = nBaCO3 = 0,15 mol
=>mH2O = 10,2 – mCO2 = 10,2 – 0,15.44 = 3,6 gam =>nH2O = 0,2 mol
Bảo toàn nguyên tố H: nH = 2nH2O = 2.0,2 = 0,4 mol=>nC : nH = 0,15 : 0,4 = 3 : 8 =>X là C3H8
Đáp án cần chọn là: D
Câu 13:
 Xem đáp án
Xem đáp án
Trả lời:
Theo giả thiết ta có : Do đó có hai trường hợp xảy ra :
TH1: Ca(OH)2 dư, chỉ xảy ra phản ứng tạo kết tủa :
CO2 + Ca(OH)2 → CaCO3 + H2O (1)
0,03 0,03 0,03
mdung dịch tăng = \[{m_{{H_2}O}} + {m_{C{O_2}}} - {m_{CaC{O_3}}} = 0,28gam\]
\[ \Rightarrow {m_{{H_2}O}} = 0,28 + 3 - 0,03.44 = 1,96gam\]
\[ \Rightarrow {n_{{H_2}O}} = 0,1088mol\]
\[ \Rightarrow {n_H} = 0,217mol\]
\[ \Rightarrow {n_C}:{n_H} = 0,03:0,217 = 1:7:3\] (loai)
TH2 : Ca(OH)2 phản ứng hết :
CO2 + Ca(OH)2 → CaCO3 + H2O (1)
0,03 0,03 0,03
2CO2 + Ca(OH)2 → Ca(HCO3)2 (2)
0,02 0,01
\[ \Rightarrow {n_{C{O_2}}} = 0,05mol\]
mdung dịch tăng = \[{m_{{H_2}O}} + {m_{C{O_2}}} - {m_{CaC{O_3}}} = 0,28gam\]
\[ \Rightarrow {m_{{H_2}O}} = 0,28 + 3 - 0,05.44 = 1,08gam\]
\[ \Rightarrow {n_{{H_2}O}} = 0,06mol\]
\[ \Rightarrow {n_H} = 0,12mol\]
\[ \Rightarrow {n_C}:{n_H} = 0,05:0,12 = 5:12\] (loaij)
Vậy CTPT của ankan là C5H12
Đáp án cần chọn là: A
Câu 14:
 Xem đáp án
Xem đáp án
Trả lời:
nankan = 0,1 mol
nCO2 = n kết tủa = 0,4 mol
Áp dụng công thức :
nankan = nH2O – nCO2
=>nH2O = 0,1 + 0,4 = 0,5 mol
BTNT C =>nC = nCO2 = 0,4 mol
BTNT H=>nH = 2n H2O = 1 mol
nC : nH = 0,4 : 1 = 4 : 10
Vậy CTPT X là C4H10
Đáp án cần chọn là: B
Câu 15:
Đốt cháy hoàn toàn 4,48 lít hỗn hợp gồm C2H6 và C3H8 (đkc) rồi cho sản phẩm cháy đi qua bình 1 đựng H2SO4 đặc, bình 2 đựng dd nước vôi trong có dư thì thấy khối lượng bình 1 tăng m gam, bình 2 tăng 2,2 gam. Tính m.
 Xem đáp án
Xem đáp án
Trả lời:
Bình 1 chứa H2O; bình 2 chứa CO2
nCO2 = 2,2: 44 = 0,05 mol
Đốt cháy ankan ta có nankan = nH2O – nCO2
=>nH2O = nankan + nCO2 = 0,2 + 0,05 = 0,25 mol=>mH2O = 0,25. 18= 4,5 gam
Đáp án cần chọn là: B
Câu 16:
 Xem đáp án
Xem đáp án
Trả lời:
BTNT C : nCO2 = nBaCO3 = 0,25 mol =>mCO2 = 11 g
mCO2 + mH2O = m↓ - mdd giảm = 49,25 – 32,85 = 16,4 g
=>mH2O = 16,4 – 11 = 5,4 g =>nH2O = 0,3 mol
Nx : nH2O >nCO2 =>X là ankan
nAnkan = nH2O – nCO2 = 0,3 – 0,25 = 0,05 mol
Gọi công thức của ankan là CnH2n+2
BTNT C : 0,05. n = 0,25 =>n = 5.
CTPT của X là C5H12
Đáp án cần chọn là: A
Câu 17:
 Xem đáp án
Xem đáp án
Trả lời:
nO2 = 25,76/22,4 = 1,15 mol
Đặt nCO2 = x và nH2O = y (mol)
+ BTKL: mCO2 + mH2O = mX + mO2
=>44x + 18y = 10,2 + 1,15.32 (1)
+ BTNT "O": 2nCO2 + nH2O = 2nO2
=>2x + y = 2.1,15 (2)
Giải hệ thu được x = 0,7 và y = 0,9
Hấp thụ sản phẩm cháy vào nước vôi trong dư thì :
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
Ta thấy: nCaCO3 = nCO2 = 0,7 mol
Suy ra m = mCaCO3 = 0,7.100 = 70 gam
Đáp án cần chọn là: C
Câu 18:
 Xem đáp án
Xem đáp án
Trả lời:
Ankan ở thể khí là những ankan có số nguyên tử C ≤ 4. Nhưng CH4 và C2H6 không cho phản ứng crackinh, chỉ có C3H8 và C4H10 có khả năng crackinh
Với C3H8: C3H8 \[\mathop \to \limits^{crackinh} \] CH4 + C2H6
Ta có: \[{d_{{C_2}{H_6}/C{H_4}}}\]= 30/16 = 1,875 >1,5 (loại)
Với C4H10:
C4H10 → CH4 + C3H6
C4H10 → C2H6 + C2H4
Ta thấy trong các đáp án chỉ có C3H6 và C2H4 là cặp nghiệm sinh ra từ phản ứng crackinh C4H10 và thỏa mãn điều kiện: \[{d_{{C_2}{H_6}/C{H_4}}}\]= 42/28 = 1,5 (đúng)
Đáp án cần chọn là: C
Câu 19:
 Xem đáp án
Xem đáp án
Trả lời:
Các phản ứng xảy ra :
C3H8 → CH4 + C2H4 (1)
C2H4 + Br2 → C2H4Br2 (2)
Theo (1) và giả thiết ta có :
\[{n_{{C_3}{H_8}}} = {n_{C{H_4}}} = {n_{{C_2}{H_4}}} = \frac{{6,6}}{{44}} = 0,15mol\]
Sau khi qua bình đựng brom khí thoát ra khỏi bình có:
\[\overline M = 1,1875.16 = 19\] nên ngoài CH4 còn có C2H4 dư.
Gọi nC2H4 dư = a mol
\[\overline M = \frac{{16.0,15 + 28a}}{{0,15 + a}} = 19 \Rightarrow a = 0,05mol\]
=>nC2H4 phản ứng với Br2 = 0,15 – 0,05 = 0,1 mol =>nBr2 = 0,1 mol
\[ \Rightarrow {C_{M\,B{r_2}}} = \frac{{0,1}}{{0,4}} = 0,25M\]
Đáp án cần chọn là: B
Câu 20:
Cho etan qua xúc tác (ở nhiệt độ cao) thu được một hỗn hợp X gồm etan, etilen, axetilen và H2. Tỉ khối của hỗn hợp X đối với etan là 0,4. Nếu cho 0,4 mol hỗn hợp X qua dung dịch Br2 dư thì số mol Br2 đã phản ứng là
 Xem đáp án
Xem đáp án
Trả lời:
Phương trình phản ứng :
\[{C_2}{H_6}\mathop \to \limits^{t^\circ ,xt} {C_2}{H_4} + {H_2}\] (1)
\[{C_2}{H_6}\mathop \to \limits^{t^\circ ,xt} {C_2}{H_2} + 2{H_2}\] (2)
\[{C_2}{H_4} + B{r_2} \to {C_2}{H_4}B{r_2}\] (3)
\[{C_2}{H_2} + 2B{r_2} \to {C_2}{H_2}B{r_4}\](4)
Theo các phương trình ta thấy :
+ Số mol khí tăng sau phản ứng bằng số mol H2 sinh ra.
+ Số mol Br2 phản ứng ở (3) và (4) bằng số mol H2 sinh ra ở (1) và (2).
Áp dụng định luật bảo toàn khối lượng ta có :
\[{m_{e\tan }} = {m_X}\]
\[ \Leftrightarrow {n_{e\tan }}.{M_{e\tan }} = {n_X}.{\overline M _X}\]
\[ \Leftrightarrow \frac{{{n_{e\tan }}}}{{{n_X}}} = \frac{{{{\overline M }_X}}}{{{M_{e\tan }}}} = 0,4\]
Với nX = 0,4 mol =>netan = 0,4.0,4 = 0,16 mol
=>ntăng = nH2 sinh ra = nX – netan = 0,4 – 0,16 = 0,24 mol
=>nBr2 phản ứng = nH2 sinh ra = 0,24 mol
Đáp án cần chọn là: A
Câu 21:
 Xem đáp án
Xem đáp án
Trả lời:
Giả sử thực hiện phản ứng đehiđro hóa 1 mol một ankan
CnH2n+2 thì nCnH2n+2 phản ứng = nanken = nH2 = 0,8 mol
Suy ra nX = nanken + nH2 + nankan dư = 0,8 + 0,8 + 0,2 = 1,8 mol
Suy ra Mankan = 1,8.20.2 = 72
→ 12n + 2n + 2 = 72
→ n = 5
→ Công thức phân tử của ankan là C5H12.
Ta có: nO2 = 3,55 mol, nC3H8 = 0,15 mol
Ta có:
nO2 = 8.nC5H12 + 5.nC3H8 = 3,55 mol
→ nC5H12 = 0,35 mol
→ a = 25,2 gam
Đáp án cần chọn là: A
Câu 22:
Cracking 8,8 gam propan trong điều kiện thích hợp thu được hỗn hợp Y gồm CH4, C2H4, C3H6, H2 và C3H8 ( biết có 90% C3H8 đã phản ứng). Nếu cho hỗn hợp Y qua nước brom dư thì còn lại hỗn hợp Z có tỉ khối so với H2 bằng 7,3. Xác định khối lượng hiđrocacbon có khối lượng mol phân tử nhỏ nhất trong Z?
 Xem đáp án
Xem đáp án
Trả lời:
Cracking 0,2 mol C3H8
→ Hỗn hợp Y gồm CH4, C2H4, C3H6, H2 và C3H8 dư (90% C3H8 phản ứng).
Hỗn hợp Y đi qua nước brom dư thì còn lại hỗn hợp Z có dZ/H2 = 7,3
Đặt nH2 = x mol; nCH4 = y mol
Ta có: nC3H8 phản ứng = nH2 + nCH4 = x + y = 0,2. 90% = 0,18 mol
Hỗn hợp Z gồm x mol H2, y mol CH4 và 0,02 mol C3H8 dư.
Ta có hệ phương trình:
\[\left\{ {\begin{array}{*{20}{c}}{x + y = 0,18}\\{\frac{{2x + 16y + 44.0,02}}{{x + y + 0,02}} = 7,3.2}\end{array}} \right.\]
\[ \to \left\{ {\begin{array}{*{20}{c}}{x = 0,06}\\{y = 0,12}\end{array}} \right.\]
Vậy mCH4 = 0,12.16 = 1,92 gam
Đáp án cần chọn là: A
Câu 23:
 Xem đáp án
Xem đáp án
Trả lời:
Trong phòng thí nghiệm, CH4 được điều chế bằng cách nung natri axetat với vôi tôi xút
Đáp án cần chọn là: C
Câu 24:
 Xem đáp án
Xem đáp án
Trả lời:
2CH3COOK + 2NaOH \[\mathop \to \limits^{CaO,t^\circ } \]2CH4 + K2CO3 + Na2CO3
Đáp án cần chọn là: C
Câu 25:
 Xem đáp án
Xem đáp án
Trả lời:
Thành phần chính của khí thiên nhiên là khí metan (CH4)
Đáp án cần chọn là: A
Câu 26:
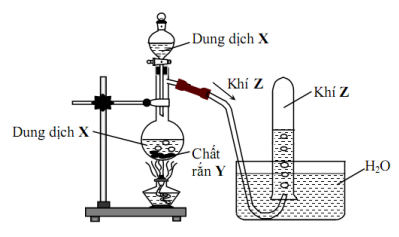
Phương trình hóa học nào sau đây phù hợp với mô hình trên?
 Xem đáp án
Xem đáp án
Trả lời:
Thu khí Z bằng cách đẩy nước nên khí Z phải hầu như không tan trong nước và không phản ứng với nước.
A loại vì CaC2 tác dụng với H2O không cần nhiệt độ, H2O không được gọi là dung dịch
B phù hợp
C loại vì SO2 là khí độc không thu bằng cách đẩy nước
D loại vì chất tham gia đều là chất rắn còn mô hình thí nghiệm là chất rắn tác dụng với chất lỏng
Đáp án cần chọn là: B
Câu 27:
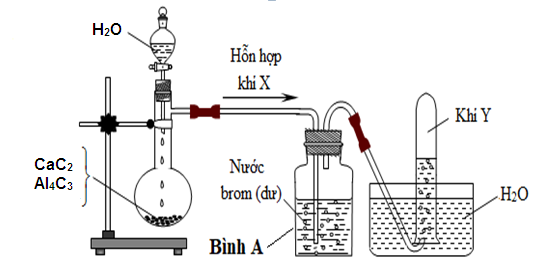
Khí Y là
 Xem đáp án
Xem đáp án
Trả lời:
CaC2 + 2H2O → Ca(OH)2 + C2H2↑
Al4C3 + 12H2O → 4Al(OH)3 + 3CH4↑
Hỗn hợp X gồm C2H2 và CH4. Cho hh này qua bình đựng dd Br2 dư thì C2H2 bị hấp thụ. Khí thoát ra là CH4
C2H2 + 2Br2 → C2H2Br4
Vậy khí Y là CH4
Đáp án cần chọn là: C
Câu 28:
Phản ứng nào sau đây điều chế được CH4 tinh khiết hơn ?
\[A{l_4}{C_3} + 12{H_2}O \to 4Al{\left( {OH} \right)_3} + 3C{H_4} \uparrow \] (1)
\[{C_4}{H_{10}}\mathop \to \limits^{Crackinh} {C_3}{H_6} \uparrow + C{H_4} \uparrow \] (2)
\[C{H_3}COON{a_r} + NaO{H_r}\mathop \to \limits^{CaO,t^\circ } N{a_2}C{O_3} + C{H_4} \uparrow \] (3)
\[C{H_2}{\left( {COONa} \right)_2}_r + 2NaO{H_r}\mathop \to \limits^{CaO,t^\circ } 2N{a_2}C{O_3} + C{H_4} \uparrow \] (4)
\[C + 2{H_2}\mathop \to \limits^{t^\circ } C{H_4} \uparrow \] (5)
 Xem đáp án
Xem đáp án
Trả lời:
Phản ứng điều chế được CH4 tinh khiết hơn là (1)(3)(4)
Đáp án cần chọn là: C
Câu 29:
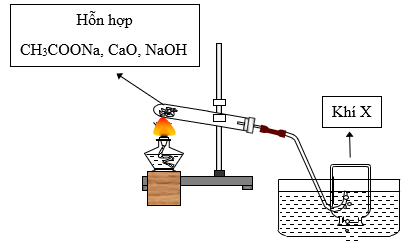
 Xem đáp án
Xem đáp án
Trả lời:
CH3COONa + NaOH CH4 + Na2CO3
Vậy khí X là CH4
Đáp án cần chọn là: B
Câu 30:
Từ CH4 (các chất vô cơ và điều kiện có đủ) có thể điều chế các chất nào sau đây?
 Xem đáp án
Xem đáp án
Trả lời:
\[C{H_4} + C{l_2}\mathop \to \limits^{as} C{H_3}Cl + HCl\]
\[C{H_4}\mathop \to \limits^{1500^\circ C,xt} {C_2}{H_2}\mathop \to \limits^{ + {H_2}\left( {Ni,t^\circ } \right)} {C_2}{H_6}\]
\[C{H_4}\mathop \to \limits^{1500^\circ C,xt} {C_2}{H_2}\mathop \to \limits^{\dim e\,hoa} {C_4}{H_4}\mathop \to \limits^{ + {H_2}\left( {Ni,t^\circ } \right)} {C_4}{H_{10}}\mathop \to \limits^{crackinh} {C_3}{H_6}\mathop \to \limits^{ + {H_2}\left( {Ni,t^\circ } \right)} {C_3}{H_8}\]
Đáp án cần chọn là: D
