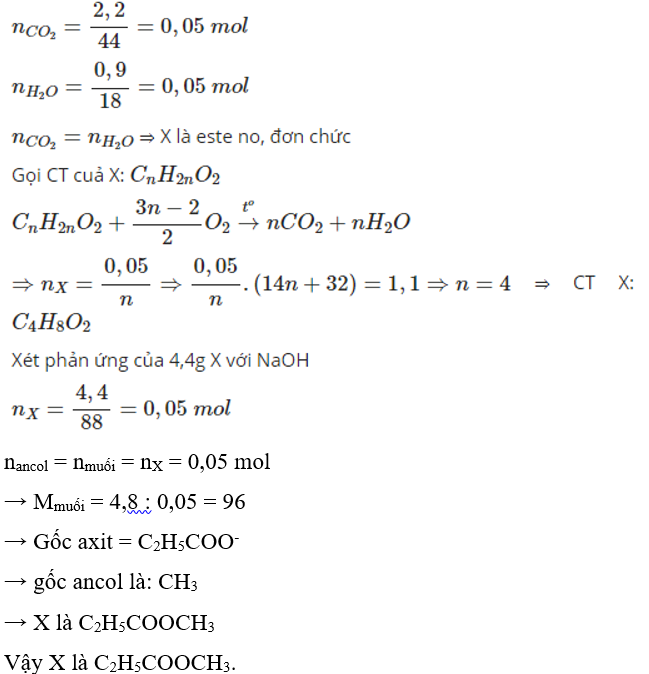Trắc nghiệm tổng hợp Hóa học năm 2023 có đáp án (Phần 11)
-
1809 lượt thi
-
52 câu hỏi
-
60 phút
Danh sách câu hỏi
Câu 1:
Để điều chế một tấn gang chứa 84% Fe, cần phải dùng bao nhiêu tấn quặng hematite? Biết hàm lượng Fe2O3 trong quặng chiếm 65% và hiệu suất quá trình đạt 86%.
 Xem đáp án
Xem đáp án
Sơ đồ phản ứng:
Ta có:
mFe = 1.84% = 0,84 tấn
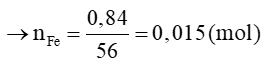
Vì hiệu suất là 86%
(tấn)
→ mquặng = (tấn).
Câu 2:
Để thu được 500 gam dung dịch KOH 25% cần lấy m1 gam dung dịch KOH 35% pha với m2 gam dung dịch KOH 15%. Tìm m1, m2?
 Xem đáp án
Xem đáp án
Ta có mdd sau phản ứng = m1 + m2
Ta có
Câu 3:
Khi cho 2,46 gam hỗn hợp Cu và Al tác dụng với dung dịch HNO3 đặc, dư, đun nóng, sinh ra 2,688 lít duy nhất NO2 (đktc). % khối lượng của Cu và Al trong hỗn hợp lần lượt là?
 Xem đáp án
Xem đáp án
Ta có:
Gọi a là số mol của Cu và b là số mol của Al.
Theo đề bài ta có hệ phương trình:
%mAl = 100% - 78,05% = 21,95%.
Câu 4:
Điều chế: SO2, CaO, H2SO4, NaOH, Al, Fe (gang-thép)
 Xem đáp án
Xem đáp án
* Điều chế SO2:
- Trong PTN:
Na2SO3 + H2SO4 → Na2SO4 + SO2 + H2O
- Trong công nghiệp:
* Điều chế CaO trong công nghiệp:
* Điều chế H2SO4 trong công nghiệp:
(Hoặc )
SO3 + H2O → H2SO4
* Điều chế NaOH trong công nghiệp:
* Điều chế Al trong công nghiệp:
* Điều chế Fe trong công nghiệp:
Mg + FeSO4 → MgSO4 + Fe
* Điều chế gang-thép trong công nghiệp:
- Điều chế gang: Dùng CO khử oxit sắt trong lò cao, sắt nóng chảy kết hợp với cacbon và một số phi kim tạo thành gang.
- Điều chế thép: Oxi hoá bớt một số nguyên tố trong gang như C,Mn,Si,...
Câu 5:
Điều chế O2 trong phòng thí nghiệm bằng cách:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Nguyên tắc điều chế O2 trong phòng thí nghiệm: Nhiệt phân các hợp chất giàu oxi và kém bền với nhiệt. Vậy để điều chế O2 trong phòng thí nghiệm người ta nhiệt phân KClO3 có MnO2 xúc tác.
Phương trình hóa học xảy ra: 2KClO3 2KCl + 3O2
Câu 6:
Để dung dịch axit sunfuric trong không khí một thời gian, nêu hiện tượng và viết phương trình?
 Xem đáp án
Xem đáp án
Axit sunfuric để lâu ngoài không khí sẽ hút ẩm từ không khí, do đó khối lượng tăng lên.
Câu 7:
Khi hoà tan 30,0 g hỗn hợp đồng và đồng (II) oxit trong dung dịch 1,00 M lấy dư, thấy thoát ra 6,72 lít khí NO (đktc). Khối lượng của đồng (II) oxit trong hỗn hợp ban đầu là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O (1)
CuO + 2HNO3 → Cu(NO3)2 + H2O (2)
Theo phản ứng (1), số mol Cu:
→ mCu = 0,45.64 = 28,8 (g)
→ mCuO = 30 – 28,8 = 1,2 (g).
Câu 8:
Cách để xác định được điều kiện bền của nguyên tử là gì?
 Xem đáp án
Xem đáp án
Các hạt nguyên tử bền luôn có số proton, nơtron thoả mãn hệ thức p ≤ n ≤ 1,5p
Trong trường hợp không thoả mãn, nguyên tử đó thuộc về đồng vị phóng xạ của nguyên tố, không bền và dễ bị phân rã thành các hạt nhân khác nhỏ hơn.
Câu 9:
Giải thích các hiện tượng ăn mòn kim loại như:
1. Đinh sắt trong không khí khô không bị ăn mòn.
2. Đinh sắt trong nước có hòa tan khí oxi ăn mòn chậm.
3. Đinh sắt trong dung dịch muối ăn NaCl bị ăn mòn nhanh.
4. Đinh sắt trong nước cất không bị ăn mòn.
 Xem đáp án
Xem đáp án
- Ăn mòn kim loại là sự phá hủy kim loại, hợp kim trong môi trường tự nhiên.
- Nguyên nhân: do kim loại tác dụng với những chất mà nó tiếp xúc trong môi trường (nước, không khí, đất)
Ví dụ:
Fe + 3Cl2 2FeCl3
3Fe + 4H2O Fe3O4 + 4H2
3Fe + 2O2 Fe3O4
- Sự ăn mòn kim loại không xảy ra hoặc xảy ra nhanh hay chậm phụ thuộc vào các chất có trong môi trường.
Ví dụ:
+ Đinh sắt trong không khí khô không bị ăn mòn
+ Đinh sắt trong nước có hòa tan oxi bị ăn mòn chậm
+ Đinh sắt trong dung dịch muối ăn bị hòa tan nhanh
+ Đinh sắt trong nước cất không bị ăn mòn
- Ở nhiệt độ cao sẽ làm cho sự ăn mòn xảy ra nhanh hơn.
Câu 10:
Công thức hóa học điphotpho pentaoxit là:
 Xem đáp án
Xem đáp án
Tiền tố: đi = 2, penta = 5
Nên công thức hóa học điphotpho pentaoxit là P2O5.
Câu 12:
Độ tan của NaCl trong nước ở 20oC là 36 gam. Khi hòa tan 14 gam NaCl vào 40 gam nước thì phải hòa tan thêm bao nhiêu gam NaCl nữa để dung dịch bão hòa?
 Xem đáp án
Xem đáp án
Nồng độ khi dung dịch bão hoà:
Đặt mNaCl thêm = x (g)
Ta có:
Vậy cần thêm 0,42 gam NaCl.
Câu 13:
Độ dinh dưỡng của phân lân là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Độ dinh dưỡng của phân lân được đánh giá theo tỉ lệ phần trăm khối lượng P2O5 tương ứng với lượng P có trong thành phần của nó.
Câu 14:
Đốt 11,2 gam Fe trong không khí, thu được m1 gam chất rắn A. Hòa tan hoàn toàn A trong 800 ml HCl 0,55M thu được dung dịch B (chỉ chứa muối) và 0,448 lít khí H2. Cho dung dịch AgNO3 dư và B thu được m2 gam kết tủa khan. Tính m1 và m2.
 Xem đáp án
Xem đáp án
nFe = 0,2 (mol); nHCl = 0,44 (mol); = 0,02 (mol)
Bảo toàn H:
m1 = mFe + mO = 14,4 gam
nAgCl = nHCl = 0,44 (mol)
Bảo toàn electron: 3nFe = 2nO + 2 + nAg → nAg = 0,16 (mol)
→ m2 = mAgCl + mAg = 80,42 gam.
Câu 15:
Đốt cháy hoàn toàn 4,4 gam một hợp chất hữu cơ X, người ta thu được 8,8 gam CO2 và 3,6 gam H2O. Công thức đơn giản nhất của hợp chất hữu cơ X là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
= 0,2 (mol)⇒ nC = 0,2 (mol) ⇒ mC = 2,4 (g)
= 0,2 (mol) ⇒ nH = 0,4(mol) ⇒ mH = 0,4 (g)
Ta có: mC + mH = 2,8 < 4,4
=> Trong phân tử X có chứa O
CTDC: CxHyOz
mO = 4,4 − 2,8 = 1,6 (g) ⇒ nO = 0,1 (mol)
x : y : z = 0,2 : 0,4 : 0,1 = 2 : 4 : 1
Công thức đơn giản nhất của hợp chất hữu cơ X là C2H4O.
Câu 17:
Hỗn hợp A gồm 2 anken đồng đẳng liên tiếp. Đốt cháy hoàn toàn V lít A thu được 13,44 lít CO2 ở đktc. Mặt khác A làm mất màu vừa hết 40 gam Br2. CTPT của 2 anken và phần trăm thể tích tương ứng là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
→ 2 anken là C2H4 (x mol) và C3H6 ( y mol)
Ta có: x + y = 0,25 và 2x + 3y = 2,4.0,25
→ x = 0,15
Câu 21:
Đốt cháy 3,2 gam lưu huỳnh trong một bình chứa 1,12 lít khí O2 (đktc). Thể tích khí SO2 thu được là bao nhiêu?
 Xem đáp án
Xem đáp án
;
PTHH:
Lập tỉ lệ: → O2 dư, S hết
Theo PTHH:
Câu 22:
Đốt cháy bột Al trong bình khí clo dư, sau khi phản ứng xảy ra hoàn toàn khối lượng chất rắn trong bình tăng 4,26 gam. Khối lượng Al đã phản ứng là?
 Xem đáp án
Xem đáp án
Nhận thấy: Khối lượng chất rắn trong bình tăng bằng chính khối lượng của Cl2 phản ứng.
PTHH: 2Al + 3Cl2 → 2AlCl3
Theo PTHH:
→ mAl = 0,04.27 = 1,08 (g).
Câu 24:
Đốt cháy toàn hoàn 0,1 mol hợp chất hữu cơ (D) cần vừa đủ 14,4 gam oxi thấy sinh ra 13,2 gam CO2 và 7,2 gam nước
a) Tìm phân tử khối của D
b) Xác định công thức phân tử của D
 Xem đáp án
Xem đáp án
Đốt cháy hoàn toàn D thu được CO2; H2O nên D chứa C, H và có thể chứa O.
D có dạng CxHyOz
Bảo toàn nguyên tố O:
Vậy D là C3H8O → MD = 12.3 + 8 + 16 = 60 (g/mol).
Câu 25:
Đốt cháy toàn hoàn 0,1 mol chất hữu cơ D, sản phẩm chỉ gồm 4,48 lít khí CO2 (ở đktc) và 5,4 gam H2O. Viết công thức cấu tạo các chất thoả mãn tính chất trên của D.
 Xem đáp án
Xem đáp án
Số
Số
→ D là C2H6, C2H6O, C2H6O2.
Công thức cấu tạo:
CH3 – CH3
CH3 – CH2 – OH; CH3 – O – CH3
CH2OH – CH2OH.
Câu 26:
Đốt cháy hoàn toàn 0,24g magie (Mg) trong không khí, người ta thu được 0,4g magie oxit. Em hãy tìm công thức hóa học đơn giản của magie oxit.
 Xem đáp án
Xem đáp án
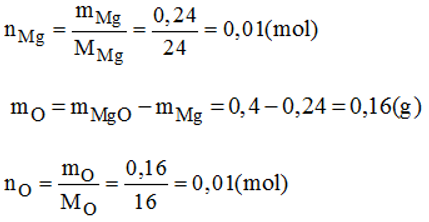
Vậy trong 1 phân tử hợp chất có 0,01 mol nguyên tử Mg; 0,01 mol nguyên tử O. Có nghĩa là 1 mol nguyên tử Mg kết hợp với 1 mol nguyên tử O.
→ Công thức hóa học đơn giản của magie oxit là: MgO.
Câu 27:
Đốt cháy hoàn toàn 0,7 mol hỗn hợp X gồm axit acrylic, vinyl acrylat, axit axetic, metyl axetat (trong đó số mol vinyl acrylat bằng tổng số mol axit axetic và metyl axetat) cần vừa đủ V lít O2, thu được hỗn hợp Y gồm CO2 và 30,6 gam nước. Dẫn Y qua dung dịch chứa 2 mol Ca(OH)2 đến phản ứng hoàn toàn được m gam kết tủa. Giá trị của V và m là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Bảo toàn nguyên tố O
→
Khi cho CO2, H2O tác dụng với Ca(OH)2 thì:
Câu 29:
Đốt cháy hoàn toàn 0,05 mol một anken A thu được 4,48 lít CO2 (đktc). Cho A tác dụng với dung dịch HBr chỉ cho một sản phẩm duy nhất. CTCT của A là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Đặt CTPT của anken là CnH2n (n ≥ 2)
Ta có: . Vậy anken có CTPT là C4H8.
Cho A tác dụng với dung dịch HBr chỉ cho một sản phẩm duy nhất nên A là CH3CH = CHCH3.
Câu 30:
Đốt cháy hoàn toàn 100 ml hỗn hợp khí X gồm trimetylamin và hai hiđrocacbon đồng đẳng kế tiếp bằng một lượng oxi vừa đủ, thu được 750 ml hỗn hợp Y gồm khí và hơi. Dẫn toàn bộ Y đi qua dung dịch H2SO4 đặc (dư). Thể tích khí còn lại là 350 ml. Các thể tích khí và hơi đo cùng điều kiện. Hai hiđrocacbon đó là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Nếu hiđrocacbon là ankan:
Vankan + Vamin = → Loại
Nếu hiđrocacbon là anken CnH2n
Bảo toàn nguyên tố H: 50.9 + 50.2n = 2= 2.400 = 800 → n = 3,5
Vậy hai anken là C3H6 và C4H8.
Câu 31:
Đốt cháy hoàn toàn 11,2 lít khí metan. Hãy tính thể tích khí oxi cần dùng và thể tích khí cacbonic tạo thành. Biết các thể tích khí đo ở điều kiện tiêu chuẩn.
 Xem đáp án
Xem đáp án
Phương trình phản ứng:
Theo phương trình:
Câu 32:
Đốt cháy hoàn toàn 13,5 gam etylamin, thu được H2O, N2 và x mol CO2. Giá trị của x là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Bảo toàn nguyên tố C: C2H5NH2 → 2CO2
→ x = 0,3.2 = 0,6 (mol).
Câu 33:
Đốt hoàn toàn 2,24 lít khí H2 (đktc) trong không khí, tính khối lượng nước thu được?
 Xem đáp án
Xem đáp án
PTHH:
Câu 34:
Đốt cháy hết 4,1 gam chất A thu được 2,65 gam Na2CO3; 1,68 lít CO2 (đktc) và l,35g H2O. Biết trong A chỉ có một nguyên tử Na. Tìm công thức phân tử của chất A:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Vì sản phẩm cháy gồm Na2CO3, CO2 và H2O nên trong A chắc chắn có C, H, Na, có thể có O.
Ta có:
→ nNa = 0,05 (mol)
Vì trong A chỉ có một nguyên tử Na → nA = 0,05 mol
Gọi công thức phân tử của A là CxHyOzNa
Vậy CTPT của A là C2H3O2Na.
Câu 35:
Để đốt cháy hoàn toàn 4,212 gam kim loại R có hóa trị III cần vừa đủ 2,7216 lít Cl2 (đktc). Kim loại R là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
PTHH:
Vậy R là crom (Cr).
Câu 36:
Đốt cháy hoàn toàn 4,48 lít C3H8 (đktc) thu được V lít CO2 (đktc) và m gam nước. Tính m và V.
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
m = 0,8.18 = 14,4 gam
V = 0,6.22,4 = 13,44 lít.
Câu 38:
Đốt cháy hoàn toàn 4,5 gam chất hữu cơ A, sau phản ứng thu được hỗn hợp sản phẩm cháy. Hấp thụ toàn bộ sản phẩm cháy vào dung dịch Ba(OH)2 thì thấy xuất hiện 39,4 gam kết tủa trắng, đồng thời khối lượng dung dịch giảm 24,3 gam. Mặt khác, oxi hoàn toàn 6,75 gam A bằng CuO (to), sau phản ứng thu được 1,68 lít N2 (đktc). Biết A có công thức phân tử (CTPT) trùng với công thức đơn giản nhất (CTĐGN). Vậy CTPT của A là:
 Xem đáp án
Xem đáp án
mdd giảm =
Xét 6,75 gam A phản ứng tạo 0,075 mol N2
→ Vậy 4,5 gam A thì tạo 0,05 mol N2
→ nN(A) = 0,1 mol
Ta có : mA = mC + mH + mO + mN → nO = 0
→ nC : nH : nN = 0,2 : 0,7 : 0,1 = 2 : 7 : 1
→ CTĐG nhất và cũng là CTPT của A là C2H7N.
Câu 39:
Đốt cháy hết 48 gam lưu huỳnh (S) trong oxi (O2) thu được 96 gam lưu huỳnh đioxit (SO2).
a, Viết công thức về khối lượng của phản ứng đã xảy ra
b, Tính khối lượng oxi đã phản ứng.
 Xem đáp án
Xem đáp án
a. Phương trình:
Áp dụng định luật bảo toàn khối lượng:
b. Thay vào trên, ta có:
48 + = 96
→ = 96 – 48 = 48 (g).
Câu 40:
Đốt cháy hoàn toàn 5,1 gam một este X cần vừa đủ 7,28 lít O2 (đktc). CTPT của X là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Đặt công thức của este là CnH2nO2
Vậy CTPT của X là C5H10O2.
Câu 41:
Đốt cháy hoàn toàn 6 gam chất hữu cơ Y chứa các nguyên tố: C, H, O thu được 4,48 lít CO2 (đktc) và 3,6 gam H2O. Công thức phân tử của Y là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Gọi công thức phân tử của Y có dạng: CxHyOz
Ta có x : y : z = nC : nH : nO = 0,2 : 0,4 : 0,2 = 1 : 2 : 1
Vậy công thức đơn giản nhất của Y là: (CH2O)n
Có MY = 60 (g/mol) → 30.n = 60 → n = 2.
Vậy công thức phân tử của Y là: C2H4O2.
Câu 42:
Đốt cháy hoàn toàn 6,72 lít hỗn hợp khí A (đktc) gồm 1 ankan X và 1 anken Y thu được 11,2 lít khí CO2 (đktc) và 10,8 gam H2O. Công thức phân tử của X và Y lần lượt là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Đặt công thức phân tử của ankan X là CnH2n+2, công thức phân tử của anken Y là CmH2m (điều kiện n≥1, m≥2)
Bảo toàn nguyên tố C ta có:
Suy ra n + 2m =5
Vì n≥1, m≥2 nên chỉ có n = 1, m = 2 thỏa mãn. Vậy X là CH4 và Y là C2H4.
Câu 44:
Đốt cháy hoàn toàn 9 gam một hợp chất hữu cơ X, thu được hỗn hợp sản phẩm khí và hơi gồm CO2 và H2O. Dẫn toàn bộ sản phẩm này vào bình đựng nước vôi trong dư, thu được 30 gam kết tủa đồng thời thấy khối lượng bình tăng thêm 18,6 gam. Xác định công thức đơn giản nhất của X.
 Xem đáp án
Xem đáp án
Bảo toàn nguyên tố C:
Khối lượng bình tăng:
Bảo toàn nguyên tố H:
mC + mH = 0,3.12 + 0,6 = 4,2 < mX
Vậy trong X có O
Tỉ lệ: nC : nH : nO = 0,3 : 0,6 : 0,3 = 3 : 6 : 3 = 1 : 2 : 1
Vậy công thức đơn giản nhất là CH2O.
Câu 45:
Đốt cháy a gam photpho trong bình chứa 13,44 lít khí oxi (đktc) tạo thành 28,4 gam điphotphopentaoxit P2O5. Tính a
 Xem đáp án
Xem đáp án
;
P tính theo sản phẩm P2O5, O2 còn dư
→ mP = 0,4.31 = 12,4 (g).
Câu 46:
Đốt cháy hoàn toàn một hidrocacbon X thu được 0,2 mol CO2 và 0,3 mol H2O. Vậy X thuộc dãy đồng đẳng nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Có → ankan.
Câu 47:
Đốt cháy hoàn toàn hỗn hợp khí A chứa CO và H2 cần dùng vừa đủ 5,6 lít khí oxi và sản phẩm tạo thành chứa 3,36 lít khí cacbonic. Các khí ở đktc.
a) Lập các phương trình hóa học
b) Tính thể tích mỗi khí trong hỗn hợp A.
c) Tính % thể tích mỗi khí trong hỗn hợp A.
 Xem đáp án
Xem đáp án
a.
b. Theo phương trình:
c.
Câu 48:
Đốt cháy hoàn toàn hỗn hợp X chứa CH3OH, C2H5OH, C3H7OH và C4H9OH cần dùng vừa đủ 0,6 mol O2, thu được CO2 và 9,9 gam H2O. Mặt khác, cho toàn bộ lượng X trên vào bình đựng Na dư thấy có V lít khí (đktc) thoát ra. Giá trị của V là?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Ta thấy hỗn hợp X đều chứa ancol no, đơn chức nên gọi CTTQ của X là CnH2n+1OH. Có
Theo phương trình, ta có:
Theo phương trình, ta có:
Theo phương trình, ta có:
Câu 49:
Đốt cháy hoàn toàn m gam một amin X bằng lượng không khí vừa đủ thu được 17,6 gam CO2 và 12,6 gam H2O và 69,44 lít nitơ. Giả thiết không khí chỉ gồm nitơ và oxi, trong đó oxi chiếm 20% thể tích. Các thể tích đo ở đktc. Amin X có công thức phân tử là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Nhận thấy đáp án đều là các amin no đơn chức mạch hở nên ta tính ngay được số mol amin bằng việc áp dụng công thức tính nhanh:
→ mamin = mC + mH + mN = 0,4.12 + 0,7.2 + 0,2.14 = 9 (g)
Câu 50:
Đốt cháy hoàn toàn một amin no, đơn chức, mạch hở thu được tỉ lệ khối lượng của CO2 so với nước là 44: 27. Công thức phân tử của amin đó là?
 Xem đáp án
Xem đáp án
Amin no, đơn chức, mạch hở có công thức tổng quát là CnH2n+3N (n≥1)
Tỉ lệ khối lượng của CO2 với H2O là 44 : 27 nên coi khối lượng của CO2 là 44 gam, khối lượng của H2O là 27 gam.
→nC : nH = 1 : 3
⇒ 2n + 3 = 3n ⇒ n = 3
Vậy công thức của amin là C3H9N.
Câu 51:
Đốt cháy hoàn toàn 1 ankan(A) thu được 11 gam C02 và 5,4 gam nước. Khi clo hóa (A) theo (tỉ lệ mol 1:1) tạo thành chất dẫn xuất monoclo duy nhất. Xác định CTPT và viết CTCT đúng của A.
 Xem đáp án
Xem đáp án
Gọi CTTQ của A là CnH2n+2
Ta có:
Vậy CTPT của A là C5H12
Vì khi clo hóa A theo tỉ lệ 1 : 1 chỉ thu được 1 môn duy nhất , do đó :
CTCT của X là
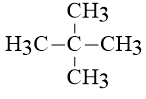
Câu 52:
Đốt cháy hoàn toàn một hidrocacbon X thu được 8,96 lít khí CO2 (đktc) và 9 gam nước. Xác định CTPT của X.
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
→ C : H = 0,4 : 1 = 4 : 10
→ X là C4H10.