Trắc nghiệm tổng hợp Hóa học năm 2023 có đáp án (Phần 8)
-
1805 lượt thi
-
64 câu hỏi
-
49 phút
Danh sách câu hỏi
Câu 1:
Viết công thức cấu tạo và công thức eletron của CH3OH?
 Xem đáp án
Xem đáp án
Công thức cấu tạo của CH3OH
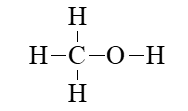
Công thức electron của CH3OH
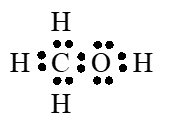
Câu 5:
Có những muối sau: CaCO3, CuSO4, MgCl2. Hãy cho biết muối nào có thể điều chế bằng phương pháp sau :
a) Axit tác dụng với bazơ.
b) Axit tác dụng với kim loại.
c) Muối tác dụng với muối.
d) Oxit bazơ tác dụng với oxit axit.
Viết các phương trình hoá học.
 Xem đáp án
Xem đáp án
a) Muối được điều chế bằng cách cho axit tác dụng với bazơ: CuSO4, MgCl2.
Cu(OH)2 + H2SO4 → CuSO4 + 2H2O
Mg(OH)2 + 2HCl → MgCl2 + 2H2O
b) Muối được điều chế bằng cách cho axit tác dụng với kim loại: MgCl2, CuSO4.
Mg + 2HCl → MgCl2 + H2↑
Cu + 2H2SO4 (đặc) CuSO4 + SO2↑ + H2O
c) Muối được điều chế bằng cách cho muối tác dụng với muối: CaCO3, CuSO4, MgCl2.
CaCl2 + Na2CO3 → CaCO3↓ + 2NaCl
CuCl2 + Ag2SO4 → CuSO4 + 2AgCl↓
BaCl2 + MgSO4 → BaSO4↓ + MgCl2
d) Muối được điều chế bằng cách cho oxit bazơ tác dụng với oxit axit: CaCO3.
Câu 6:
Chỉ dùng H2O và quỳ tím hãy nhận biết các chất rắn: CaCO3, CaO, P2O5, Na2O, NaCl. Viết phương trình phản ứng xảy ra nếu có.
 Xem đáp án
Xem đáp án
- Trích các chất thành các mẫu thử đựng trong các ống nghiệm riêng biệt. Đánh số thứ tự
- Hoà tan các mẫu thử vào nước:
+ Tan: CaO, P2O5, Na2O, NaCl (nhóm I)
+ Không tan: CaCO3
CaO + H2O → Ca(OH)2
P2O5 + 3H2O → 2H3PO4
Na2O + H2O → 2NaOH
- Nhúng quỳ tím vào sản phẩm hoà tan của nhóm I vào nước:
+ Quỳ tím hoá đỏ → chất ban đầu là P2O5
+ Quỳ tím hoá xanh → chất ban đầu là CaO, Na2O (nhóm II)
+ Không đổi màu → NaCl
- Cho sản phẩm hoà tan vào nước của P2O5 vào sản phẩm vào hoà tan của CaO, Na2O vào nước:
+ Tan → chất ban đầu là CaO
+ Không tan → chất ban đầu là Na2O
3Ca(OH)2 + 2H3PO4 → Ca3(PO4)2↓ + 6H2O
Câu 7:
: Khi nung hỗn hợp CaCO3 và MgCO3 thì khối lượng chất rắn thu được sau phản ứng chỉ bằng một nửa khối lượng ban đầu. Xác định thành phần khối lượng các chất trong hỗn hợp ban đầu.
 Xem đáp án
Xem đáp án
Giả sử ban đầu có x mol CaCO3 và y mol MgCO3
→mhh ban đầu = 100x + 84y (g)
→ mhh sau = 56x + 40y (g)
→ 56x + 40y = 50%(100x + 84y) = 50x + 42y
→ 6x = 2y
→ y = 3x
Vậy
Câu 8:
Hãy giải thích vì sao:
a. Khi nung nóng đá vôi (CaCO3) thì thấy khối lượng giảm đi.
b. Khi nung nóng miếng đồng trong không khí (có oxi) thì thấy khối lượng tăng lên.
 Xem đáp án
Xem đáp án
a) Khí CO2 bay đi nên chất rắn còn lại là CaO nên khối lượng giảm đi
PTHH:
b) Khi nung nóng, đồng tác dụng với oxi trong không khí tạo thành đồng (II) oxit nên khối lượng tăng lên
PTHH:
Câu 10:
Phương trình phân tử, phương trình ion thu gọn, phương trình ion đầy đủ:
1.Ca(HCO3)2 + HCl
2.Ca(HCO3)2 + NaOH
3.Ca(HCO3)2 + Ca(OH)2
4.Cu(NO3)2 + Na2SO4
5.CaCl2 + Na3PO4
 Xem đáp án
Xem đáp án
1.Phương trình phân tử:
Phương trình ion đầy đủ:
Phương trình ion rút gọn:
2. Phương trình phân tử:
Phương trình ion đầy đủ:
Phương trình ion rút gọn:
4. Không phản ứng
5. Phương trình phân tử:
Phương trình ion đầy đủ:
Phương trình ion rút gọn:
Câu 11:
Cho một mẫu CaO vào một ống thí nghiệm đựng nước cất, sau đó nhỏ vài giọt dung dịch phenolphtalein vào dung dịch thu được, dung dịch chuyển sang màu gì?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
PTHH: CaO + H2O → Ca(OH)2
Ca(OH)2 có tính bazơ, mà bazơ làm dung dịch phenolphtalein chuyển sang màu đỏ.
Câu 13:
Cặp chất khi phản ứng tạo ra chất khí là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Phương trình phản ứng xảy ra:
Na2CO3 + 2HCl → 2NaCl + H2O + CO2↑
Câu 14:
Cặp chất nào sau đây không phải là đồng phân của nhau?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Metyl fomat và axit axetic có CTPT: C2H4O2.
Mantozơ và saccarozơ có CTPT: C12H22O11.
Fructozơ và glucozơ có CTPT: C6H12O6.
Tinh bột và xenlulozơ đều có CTPT tổng quát là (C6H10O5)n nhưng hệ số n ở tinh bột và xenlulozơ khác nhau → chúng không phải đồng phân của nhau.
Câu 15:
Cần lấy bao nhiêu lít N2 và H2 (đktc) để điều chế được 51 gam NH3. Biết hiệu suất của phản ứng là 25%.
 Xem đáp án
Xem đáp án
Bảo toàn N:
Mà H = 25% →
Bảo toàn H:
Mà H = 25% →
Câu 16:
Cho phản ứng sau:
KMnO4 + KNO2 + H2SO4 → MnSO4 + KNO3 + K2SO4 + H2O
Tổng hệ số cân bằng (tối giản) của phản ứng là?
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
2KMnO4 + 5KNO2 + 3H2SO4 → 2MnSO4 + 5KNO3 + K2SO4 + 3H2O
Tổng hệ số khi cân bằng các chất là 21.
Câu 17:
 Xem đáp án
Xem đáp án
Câu 18:
Cân bằng phương trình oxi hoá khử sau:
1) Cu(NO3)2 → CuO + NO2 + O2
 Xem đáp án
Xem đáp án
1) Cu(NO3)2 → CuO + NO2 + O2
2Cu(NO3)2 2CuO + 4NO2 + O2
Câu 19:
Cân bằng phương trình oxi hoá khử sau:
2) NH4NO2 → N2 + H2O
 Xem đáp án
Xem đáp án
2) NH4NO2 → N2 + H2O
NH4NO2 N2 + 2H2O
Câu 20:
Cân bằng phương trình oxi hoá khử sau:
3) NH4NO3 → N2O + H2O
 Xem đáp án
Xem đáp án
3) NH4NO3 → N2O + H2O
NH4NO3 N2O + 2H2O
Câu 21:
Cân bằng phản ứng oxi hóa khử:
a) Fe3O4 + Al → Al2O3 + Fe
 Xem đáp án
Xem đáp án
a) Fe3O4 + Al → Al2O3 + Fe
3Fe3O4 + 8Al → 4Al2O3 + 9Fe
Câu 22:
Cân bằng phản ứng oxi hóa khử:
b) FeSO4 + KMnO4 + H2SO4 → Fe2(SO4)3 + K2SO4 + MnSO4 + H2O
 Xem đáp án
Xem đáp án
b) FeSO4 + KMnO4 + H2SO4 → Fe2(SO4)3 + K2SO4 + MnSO4 + H2O
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Câu 23:
Cân bằng các phương trình bằng phương pháp oxi hóa khử:
Mg + H2SO4 → MgSO4 + SO2 + H2O
 Xem đáp án
Xem đáp án
a) Mg + H2SO4 → MgSO4 + SO2 + H2O
Mg + 2H2SO4 → MgSO4 + SO2 + 2H2O
Câu 24:
Cân bằng các phương trình bằng phương pháp oxi hóa khử:
Mg + H2SO4 → MgSO4 + S + H2O
 Xem đáp án
Xem đáp án
b) Mg + H2SO4 → MgSO4 + S + H2O
3Mg + 4H2SO4 → 3MgSO4 + S + 4H2O
Câu 25:
Cân bằng các phương trình bằng phương pháp oxi hóa khử:
Zn + H2SO4 → ZnSO4 + H2S + H2O
 Xem đáp án
Xem đáp án
c) Zn + H2SO4 → ZnSO4 + H2S + H2O
4Zn + 5H2SO4 → 4ZnSO4 + H2S + 4H2O
Câu 26:
Cân bằng các phương trình bằng phương pháp oxi hóa khử:
M + HNO3 → M(NO3)2 + NO2 + H2O
 Xem đáp án
Xem đáp án
d) M + HNO3 → M(NO3)2 + NO2 + H2O
M + 4HNO3 → M(NO3)2 + 2NO2 + 2H2O
Câu 27:
Cân bằng các phương trình bằng phương pháp oxi hóa khử:
M + HNO3 → M(NO3)2 + NO + H2O
 Xem đáp án
Xem đáp án
e) M + HNO3 → M(NO3)2 + NO + H2O
3M + 8HNO3 → 3M(NO3)2 + 2NO + 4H2O
Câu 28:
Cân bằng các phương trình bằng phương pháp oxi hóa khử:
M + HNO3 → M(NO3)2 + N2O + H2O
 Xem đáp án
Xem đáp án
g) M + HNO3 → M(NO3)2 + N2O + H2O
4M + 10HNO3 → 4M(NO3)2 + N2O + 5H2O
Câu 29:
Cân bằng phương trình oxi hoá – khử:
I2 + Na2S2O3 → Na2S4O6 + NaI
 Xem đáp án
Xem đáp án
I2 + 2Na2S2O3 → Na2S4O6 + 2NaI
Câu 30:
Cân bằng phương trình phản ứng bằng phương pháp thăng bằng electron:
Cl2 + Ca(OH)2 → Ca(OCl)2 + CaCl2 + H2O
 Xem đáp án
Xem đáp án
2Cl2 + 2Ca(OH)2 → Ca(OCl)2 + CaCl2 + 2H2O
Câu 31:
Cân bằng các phản ứng oxi hoá – khử dưới đây theo phương pháp thăng bằng electron, xác định vai trò các chất tham gia và các quá trình oxi hoá, quá trình khử:
a) Cl2 + KOHnóng → KCl + KClO3 + H2O
 Xem đáp án
Xem đáp án
a)
Cl2 vừa là chất khử, vừa chất oxi hoá
: quá trình oxi hoá
: quá trình khử
3Cl2 + 6KOHnóng → 5KCl + KClO3 + 3H2O
Câu 32:
Cân bằng các phản ứng oxi hoá – khử dưới đây theo phương pháp thăng bằng electron, xác định vai trò các chất tham gia và các quá trình oxi hoá, quá trình khử:
b) FeS2 + H2SO4 đặc nóng → Fe2(SO4)3 + SO2 + H2O
 Xem đáp án
Xem đáp án
b)
FeS2 là chất khử, H2SO4 là chất oxi hoá
: quá trình oxi hoá
: quá trình khử
2FeS2 + 14H2SO4 đặc nóng → Fe2(SO4)3 + 15SO2 + 14H2O
Câu 33:
Cân bằng các phản ứng oxi hoá – khử dưới đây theo phương pháp thăng bằng electron, xác định vai trò các chất tham gia và các quá trình oxi hoá, quá trình khử:
b) FeS2 + H2SO4 đặc nóng → Fe2(SO4)3 + SO2 + H2O
 Xem đáp án
Xem đáp án
b)
FeS2 là chất khử, H2SO4 là chất oxi hoá
: quá trình oxi hoá
: quá trình khử
2FeS2 + 14H2SO4 đặc nóng → Fe2(SO4)3 + 15SO2 + 14H2O
Câu 34:
Cân bằng phản ứng hóa học sau bằng phương pháp thăng bằng electron (xác định chất khử, oxi hóa, quá trình oxi hóa, quá trình khử)
1. KClO3 → KCl + O2
 Xem đáp án
Xem đáp án
1.
KClO3 vừa là chất oxi hoá, vừa là chất khử
: quá trình khử
: quá trình oxi hoá
2KClO3 2KCl + 3O2
Câu 35:
Cân bằng phản ứng hóa học sau bằng phương pháp thăng bằng electron (xác định chất khử, oxi hóa, quá trình oxi hóa, quá trình khử)
2. Cl2 + NaOH → NaCl + NaClO + H2O
 Xem đáp án
Xem đáp án
2.
Cl2 vừa là chất oxi hoá, vừa là chất khử
: quá trình oxi hoá
: quá trình khử
Cl2 + 2NaOH → NaCl + NaClO + H2O
Câu 36:
Cân bằng phản ứng oxi hoá khử bằng phương pháp thăng bằng electron:
1) NO2 + NaOH → NaNO2 + NaNO3 + H2O
 Xem đáp án
Xem đáp án
1)
2NO2 + 2NaOH → NaNO2 + NaNO3 + H2O
Câu 37:
Cân bằng phản ứng oxi hoá khử bằng phương pháp thăng bằng electron:
2) Cl2 + NaOH → NaCl + NaClO3 + H2O
 Xem đáp án
Xem đáp án
2)
3Cl2 + 6NaOH → 5NaCl + NaClO3 + 3H2O
Câu 38:
a. Fe + HNO3 → Fe(NO3)3 + N2 + H2O
b. Mg + HNO3 → Mg(NO3)2 + NO + H2O
 Xem đáp án
Xem đáp án
b. 3Mg + 8HNO3 → 3Mg(NO3)2 + 2NO + 4H2O
Câu 39:
Cân bằng các PTHH sau:
c. FexOy + H2 → FeO + H2O
d. CxHy + O2 → CO2 + H2O
e. KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O
 Xem đáp án
Xem đáp án
c. FexOy + (y – x)H2 xFeO + (y – x)H2O
d. CxHy +( ) O2 xCO2 + H2O
e. 2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
Câu 40:
Cân bằng PTHH hợp chất hữu cơ tổng quát:
1) CnH2n + O2 → CO2 + H2O
2) CnH2n+2 + O2 → CO2 + H2O
3) CnH2n-2 + O2 → CO2 + H2O
 Xem đáp án
Xem đáp án
1) CnH2n + O2 nCO2 + nH2O
2) CnH2n+2 + O2 nCO2 + (n+1)H2O
3) CnH2n-2 + O2 nCO2 + (n – 1)H2O
Câu 41:
Cân bằng PTHH hợp chất hữu cơ tổng quát:
4) CnH2n-6 + O2 → CO2 + H2O
5) CnH2n+2O + O2 → CO2 + H2O
 Xem đáp án
Xem đáp án
4) CnH2n-6 + O2 nCO2 + (n – 3)H2O
5) CnH2n+2O + O2 nCO2 + (n +1)H2O
Câu 42:
Biết 1 mol nguyên tử sắt có khối lượng bằng 56g, một nguyên tử sắt có 26 electron. Số hạt electron có trong 5,6g sắt là:
 Xem đáp án
Xem đáp án
0,1 mol sắt → 0,1. 6,022.1023 = 6,022.1022 nguyên tử sắt
Số electron = 6,022.1022. 26 = 15,6572.1023 electron.
Câu 43:
Cho dung dịch NH4NO3 tác dụng với dung dịch bazơ của kim loại thu được 4,48 lít khí (đktc) và 26,1 gam muối. Kim loại đó là
 Xem đáp án
Xem đáp án
nNH4NO3 + M(OH)n → M(NO3)n + nNH3 +nH2O
0,2/n 0,2
→ Mmuối = MM + 62n =
→ MM = 68,5n
→ n = 2 và M là bari (Ba).
Câu 44:
Cho một luồng khí CO đi qua 29 gam một oxit sắt. Sau khi phản ứng xảy ra hoàn toàn người ta thu được một chất rắn có khối lượng 21 gam. Xác định công thức oxit sắt.
 Xem đáp án
Xem đáp án
Gọi công thức của oxit là FexOy
Phản ứng xảy ra:
Ta có:
Vậy oxit là Fe3O4.
Câu 45:
Trong tự nhiên brom có 2 đồng vị là 79Br và 81Br có nguyên tử khối trung bình là 79,92. Thành phần phần trăm về khối lượng của 81Br trong NaBr là bao nhiêu? Có MNa =23 (g/mol).
 Xem đáp án
Xem đáp án
Gọi phần trăm của đồng vị 79Br là x %;
phần trăm của đồng vị 81Br là (100−x)%
Nguyên tử khối trung bình:
→ x = 54
Phần trăm của đồng vị 81Br là 46%.
Xét 1 mol NaBr có:
1 mol Br → 0,46 mol 81Br
Câu 46:
Trung hòa 100 ml dung dịch etyl amin cần 60 ml dung dịch HCl 0,1M. Nồng độ mol/l của dung dịch etyl amin là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Phương trình: HCl + CH3NH2 → CH3NH3Cl
nHCl = 0,1. 0,06 = 0,006 (mol)
Câu 47:
Cho 4,8 g một kim loại R hoá trị II tác dụng hết với dung dịch HNO3 loãng, thu được 1,12 lít khí NO duy nhất (đktc). Kim loại R là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
nNO = 1,12 : 22,4 = 0,05 mol
3R + 8HNO3 → 3R(NO3)2 + 2NO + 4H2O
Theo phương trình ta có:
⇒ R = 4,8 : 0,075 = 64 ⇒ Cu
Câu 48:
Cấu hình electron bền vững, bão hoà, bán bão hoà là gì?
 Xem đáp án
Xem đáp án
Cấu hình bền vững là cấu hình của khí hiếm. Khi mà số electron lớp vỏ bằng 8 (ngoại trừ He).
Ví dụ: Ar có cấu hình là 1s2 2s22p6 3s23p6
Ion Na+ có cấu hình là 1s2 2s22p6
Cấu hình bão hoà là khi phân lớp đạt số electron tối đa. Ví dụ phân lớp s điền đủ 2 e, p điền đủ 6 e, d điền đủ 10 e.
Ví dụ: Mg có cấu hình 1s2 2s22p6 3s2
Cấu hình bán bão hoà là khi phân lớp đạt một nửa số electron tối đa.
Ví dụ: P có cấu hình là 1s2 2s22p6 3s23p3
Câu 49:
Viết cấu hình electron của nguyên tử của nguyên tố Ni và các ion Ni2+, Ni3+. Xác định vị trí (ô, chu kỳ, phân nhóm) của Ni trong bảng tuần hoàn. Cho? biết Ni (Z = 28).
 Xem đáp án
Xem đáp án
Ni thuộc ô 28, nhóm VIIIB
Cấu hình electron: 1s22s22p63s23p63d104s1
Ni2+: 1s22s22p63s23p63d9
Ni3+: 1s22s22p63s23p63d8.
Câu 50:
Cấu hình electron lớp ngoài cùng của nguyên tố nhóm VA là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Cấu hình electron lớp ngoài cùng của nguyên tố nhóm VA là ns2np3.
Câu 51:
Câu nào sau đây đúng?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Trong phản ứng hoá học liên kết giữa các nguyên tử bị phá vỡ, các nguyên tử được bảo toàn.
Câu 52:
Có cách nào để phân biệt khi nào sắt hoá trị II, III?
 Xem đáp án
Xem đáp án
+ Khi Fe tác dụng với các chất có tính oxi hóa mạnh như: F2, Cl2, H2SO4 đặc, nóng, HNO3 … thì sản phẩm của Fe sẽ có hóa trị (III).
+ Khi tác dụng với các chất không có tính oxi hóa hoặc tính oxi hóa yếu như S, HCl, H2SO4 loãng thì sản phẩm của Fe sẽ có hóa trị (II).
Câu 53:
Cho 6,2 gam một amin no, đơn chức, mạch hở X phản ứng hết với dung dịch HCl (vừa đủ), thu được dung dịch chứa 13,5 gam muối. Công thức của X là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Áp dụng định luật bảo toàn khối lượng, ta có:
mamin + mHCl = mmuối
→ mHCl = mmuối – mamin = 13,5 – 6,2 = 7,3 (gam)
Amin no, đơn chức, mạch hở nên có công thức là CnH2n+1NH2.
Phương trình: CnH2n+1NH2 + HCl → CnH2n+2Cl
namin = nHCl = 0,2 (mol)
Vậy amin cần tìm là CH3NH2.
Câu 54:
Cân bằng phản ứng hoá học:
CH3CH2OH + KMnO4 + H2SO4 → CH3COOH + MnSO4 + H2O + K2SO4
 Xem đáp án
Xem đáp án
Chất khử: CH3CH2OH; chất oxi hoá: KMnO4.
Ta có các quá trình:
Phương trình hoá học:
5CH3CH2OH + 4KMnO4 + 6H2SO4 → 5CH3COOH + 4MnSO4 +11H2O + 2K2SO4
Câu 55:
CH3COOK là chất điện li mạnh hay yếu?
 Xem đáp án
Xem đáp án
CH3COOK là chất điện li mạnh.
Phương trình điện li: CH3COOK → CH3COO- + H+
Câu 56:
 Xem đáp án
Xem đáp án
Có 2 yếu tố quyết định nên khả năng điện li của CH3COOH và CH3COONa
1. Độ âm điện.
Độ âm điện của H: 2,2
Độ âm điện của Na: 0,93
⇒ Xét 1 cách tương đói, liên kết giữa O và Na trong phân tử CH3COONa phân cực hơn so với liên kết cộng hóa trị giữa O và H trong CH3COOH nên khả năng phân li tốt hơn.
2. Liên kết hidro
Trong phân tử CH3COOH tồn tại liên kết hidro giữa các phân tử axit ⇒ làm cho phân tử bền, khó phân li.
Giữa các phân tử CH3COONa không có liên kết hidro.
Câu 57:
Đốt cháy hoàn toàn 1,395 gam hợp chất hữu cơ A thu được 3,96 gam CO2; 0,945 gam H2O và 168 ml N2 (đktc). Tỉ khối hơi của A so với không khí bằng 3,21. Công thức phân tử của A là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
MA = 3,21. 29 = 93 (g/mol)
Bảo toàn nguyên tố C:
Bảo toàn nguyên tố H:
Bảo toàn nguyên tố N:
Đặt CTPT của A là CxHyNz
CTPT của A là: (C6H7N)n
→ (6. 12 + 7 + 14). n = 93
→ n = 1
Vậy CTPT của A là C6H7N.
Câu 58:
Trong thực tế người ta thực hiện phản ứng tráng gương đối với chất nào sau đây để tráng ruột bình thuỷ tinh?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Trong thực tế người ta thực hiện phản ứng tráng gương đối với glucozơ để tráng ruột bình thuỷ tinh vì giá thành thấp, dễ tìm, dễ bảo quản, dễ điều chế, không độc.
Câu 59:
 Xem đáp án
Xem đáp án
Các oxit CaO, BaO, P2O5 có thể làm chất hút ẩm (chất làm khô) trong phòng thí nghiệm.
Vì các oxit này dễ dàng tác dụng được với nước (hơi nước).
Các phương trình hóa học :
CaO + H2O → Ca(OH)2
BaO + H2O → Ba(OH)2
P2O5 + 3H2O → 2H3PO4
Câu 61:
Chất khí A có công thức hoá học của A là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Vậy công thức hoá học của A là N2.
Câu 62:
Chỉ dùng 1 thuốc thử duy nhất hãy nhận biết các dung dịch sau: (NH4)2SO4, NaCl, Na2SO4, NH4NO3.
 Xem đáp án
Xem đáp án
- Trích mỗi chất ra 1 ít để làm mẫu thử
- Cho dung dịch Ba(OH)2 vào từng mẫu thử trên, nhận:
+ (NH4)2SO4 vừa có kết tủa trắng tạo thành và có khí mùi khai thoát ra
Ba(OH)2 + (NH4)2SO4 → BaSO4↓ + 2NH3↑ + 2H2O
+ Na2SO4 có kết tủa trắng tạo thành
Ba(OH)2 + Na2SO4 → BaSO4↓ + 2NaOH
+ NH4NO3 có khí mùi khai thoát ra
Ba(OH)2 + 2NH4NO3 → Ba(NO3)2 + 2NH3↑ + 2H2O
+ Còn lại là NaCl không phản ứng.
Câu 63:
Chỉ dùng các kim loại hãy nhận biết các dung dịch sau: NaNO3, HCl, NaOH, HNO3, CuSO4.
 Xem đáp án
Xem đáp án
Cho Fe vào các chất.
- NaNO3, NaOH không hiện tượng.
- HCl hoà tan Fe tạo khí không màu.
Fe + 2HCl → FeCl2 + H2
- HNO3 có khí không màu, hoá nâu trong không khí.
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
- CuSO4 có chất rắn màu đỏ.
2Al + 3CuSO4 → Al2(SO4)3 + 3Cu
Nhỏ CuSO4 vào 2 dung dịch còn lại.
- NaOH có kết tủa xanh.
CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4
- Còn lại NaNO3.
Câu 64:
Chỉ được dùng một kim loại, hãy trình bày cách phân biệt các dung dịch muối sau đây: NH4NO3, (NH4)2SO4, K2SO4. Viết phương trình hoá học của các phản ứng xảy ra.
 Xem đáp án
Xem đáp án
Dùng kim loại bari để phân biệt các dung dịch muối: NH4NO3, (NH4)2SO4, K2SO4.
Lấy mỗi dung dịch một ít (khoảng 2-3 ml) vào từng ống nghiệm riêng. Thêm vào mỗi ống một mẩu nhỏ kim loại bari. Đầu tiên kim loại bari phản ứng với nước tạo thành Ba(OH)2, rồi Ba(OH)2 phản ứng với dung dịch muối.
- Ở ống nghiệm nào có khí mùi khai (NH3) thoát ra, ống nghiệm đó đựng dung dịch NH4NO3:
2NH4NO3 + Ba(OH)2 → Ba(NO3)2 + 2NH3↑ + 2H2O
- Ở ống nghiệm nào có kết tủa trắng (BaSO4) xuất hiện, ống nghiệm đó đựng dung dịch K2SO4:
K2SO4 + Ba(OH)2 → BaSO4↓ + 2KOH
- Ở ống nghiệm nào vừa có khí mùi khai (NH3) thoát ra, vừa có kết tủa trắng (BaSO4) xuất hiện, ống nghiệm đó đựng dung dịch (NH4)2SO4:
(NH4)2SO4 + Ba(OH)2 → BaSO4↓ + 2NH3↑ + 2H2O.