(2023) Đề thi thử Hóa học Cụm trường TP Nam Định, Nam Định có đáp án
(2023) Đề thi thử Hóa học Cụm trường TP Nam Định, Nam Định có đáp án
-
203 lượt thi
-
40 câu hỏi
-
60 phút
Danh sách câu hỏi
Câu 4:
Xăng sinh học E5 là loại xăng có chứa 5% (về thể tích) là etanol, còn lại là xăng khoáng. Công thức phân tử của etanol là
 Xem đáp án
Xem đáp án
Chọn B
Câu 9:
Dung dịch (nồng độ 0,1M) của hợp chất nào sau đây không làm đổi màu quỳ tím?
 Xem đáp án
Xem đáp án
Anilin có tính bazơ rất yếu nên không làm đổi màu quỳ tím, còn lại axit glutamic làm quỳ tím hóa đỏ và lysin, metylamin làm quỳ tím hóa xanh.
Chọn C
Câu 10:
Dung dịch nào sau đây có thể làm mềm nước cứng toàn phần?
 Xem đáp án
Xem đáp án
Dung dịch Na2CO3 có thể làm mềm nước cứng toàn phần:
Mg2+ + CO32- → MgCO3
Ca2+ + CO32- → CaCO3
Chọn D
Câu 11:
Cho phản ứng: Fe(OH)2 + H2SO4 (đặc, nóng, dư) → X + SO2 + H2O. Hợp chất X là
 Xem đáp án
Xem đáp án
Hợp chất X là Fe2(SO4)3:
2Fe(OH)2 + 4H2SO4 → Fe2(SO4)3 + SO2 + 6H2O
Chọn A
Câu 12:
Polietilen dùng để sản xuất ống nhựa, mút cứng, túi nhựa,… Polietilen được tổng hợp bằng cách trùng hợp monome X. Monome X có công thức phân tử là
 Xem đáp án
Xem đáp án
Chọn B
Câu 13:
Đun nóng este X với dung dịch NaOH, thu được hỗn hợp sản phẩm gồm CH3COONa và CH3OH. Este X có công thức cấu tạo là
 Xem đáp án
Xem đáp án
Este X có công thức cấu tạo là CH3COOCH3:
CH3COOCH3 + NaOH → CH3COONa + CH3OH
Chọn C
Câu 14:
Trong phân tử glucozơ (dạng mạch hở) có
 Xem đáp án
Xem đáp án
Trong phân tử glucozơ (dạng mạch hở) có một liên kết π ở C=O.
Chọn C
Câu 15:
Để chuyển hóa thành tristearin, có thể cho triolein phản ứng với
 Xem đáp án
Xem đáp án
Để chuyển hóa thành tristearin, có thể cho triolein phản ứng với H2 dư, xúc tác Ni, đun nóng:
(C17H33COO)3C3H5 + 3H2 → (C17H35COO)3C3H5
Chọn A
Câu 16:
Trong phản ứng của kim loại K với khí Cl2, một nguyên tử K nhường bao nhiêu electron?
 Xem đáp án
Xem đáp án
Trong phản ứng của kim loại K với khí Cl2, một nguyên tử K nhường 1 electron:
K → K+ + 1e
Chọn C
Câu 17:
Khí X có màu nâu đỏ, có mặt trong khí thải của các động cơ đốt trong. Khí X phát thải ra không khí là một trong những nguyên nhân chính gây ra hiện tượng mưa axit. Khí X là
 Xem đáp án
Xem đáp án
Chọn A
Câu 20:
Kim loại sắt phản ứng với chất nào sau đây tạo thành hợp chất sắt (II)?
 Xem đáp án
Xem đáp án
A. Fe + Cl2 → FeCl3
B. Fe + S → FeS
C. Fe + HNO3 → Fe(NO3)3 + NO + H2O
D. Fe + H2SO4 → Fe2(SO4)3 + SO2 + H2O
Chọn B
Câu 21:
Nhận xét nào sau đây không đúng?
 Xem đáp án
Xem đáp án
A. Sai, tơ olon không có nhóm amit nên không thuộc loại poliamit.
B. Đúng
C. Đúng, do các polime không có phân tử khối xác định nên nóng chảy ở một khoảng nhiệt độ khá rộng.
D. Đúng
Chọn A
Câu 22:
Sobitol được sử dụng làm thuốc nhuận tràng, điều trị chứng táo bón. Sobitol có thể được tổng hợp bằng phản ứng hiđro hóa glucozơ (cho phản ứng với H2, xúc tác Ni, đun nóng). Để tổng hợp 118,3 gam sobitol bằng phản ứng trên (sử dụng H2 dư) cần m gam glucozơ. Phản ứng xảy ra hoàn toàn. Giá trị của m là
 Xem đáp án
Xem đáp án
CH2OH-(CHOH)4-CHO + H2 → CH2OH-(CHOH)4-CH2OH
→ mC6H12O6 = 180.118,3/182 = 117 gam
Chọn D
Câu 23:
Thí nghiệm tạo thành sản phẩm có chất kết tủa là
 Xem đáp án
Xem đáp án
A. NaOH + H2SO4 → Na2SO4 + H2O
B, D. Không phản ứng
C. Na2CO3 + CaCl2 → CaCO3↓ + NaCl
Chọn C
Câu 24:
Phèn chua thường được sử dụng để làm trong nước sinh hoạt (như nước giếng,…). Khi cho phèn chua vào nước thấy xuất hiện kết tủa keo trắng sẽ kéo các chất lơ lửng trong nước lắng xuống. Kết tủa keo trắng đó là
 Xem đáp án
Xem đáp án
Kết tủa keo trắng đó là Al(OH)3 được tạo ra từ sự thủy phân Al3+:
Al3+ + H2O ⇌ Al(OH)3 + H+
Chọn D
Câu 25:
Hòa tan hoàn toàn m gam Cu vào dung dịch HNO3 đặc, nóng, dư, thu được 0,224 lít khí NO2. Giá trị của m là
 Xem đáp án
Xem đáp án
Bảo toàn electron: 2nCu = nNO2 = 0,01
→ nCu = 0,005 → mCu = 0,32 gam
Chọn D
Câu 26:
Nhận xét nào sau đây không đúng?
 Xem đáp án
Xem đáp án
C sai, mỡ động vật có thành phần chính là chất béo no. Dầu thực vật có thành phần chính là chất béo không no.
Chọn C
Câu 27:
Nhận xét nào sau đây đúng?
 Xem đáp án
Xem đáp án
A. Sai, phân tử amilopectin có cấu trúc mạch phân nhánh.
B. Đúng
C. Sai, dung dịch saccarozơ có thể hòa tan được Cu(OH)2 tạo thành dung dịch màu xanh lam.
D. Sai, phân tử xenlulozơ được tạo thành từ các đơn vị β-glucozơ.
Chọn B
Câu 28:
Thủy phân hoàn toàn 4,80 gam HCOOCH3 bằng 100 ml dung dịch NaOH 1M (dư). Cô cạn dung dịch sau phản ứng thu được m gam chất rắn gồm HCOONa và NaOH dư. Giá trị của m là
 Xem đáp án
Xem đáp án
HCOOCH3 + NaOH → HCOONa + CH3OH
nHCOOCH3 = 0,08; nNaOH = 0,1 → Chất rắn gồm HCOONa (0,08) và NaOH dư (0,02)
→ m rắn = 6,24 gam
Chọn D
Câu 29:
Cho 0,78 gam bột Zn vào dung dịch CuSO4 dư. Sau khi phản ứng xảy ra hoàn toàn thu được m gam Cu. Giá trị của m là
 Xem đáp án
Xem đáp án
Zn + CuSO4 → ZnSO4 + Cu
nCu = nZn = 0,012 → mCu = 0,768 gam
Chọn D
Câu 30:
Cho 1,78 gam alanin vào 100 ml dung dịch HCl 0,3M thu được dung dịch X. Sau khi phản ứng xảy ra hoàn toàn, làm bay hơi nước và HCl dư của dung dịch X, thu được m gam chất rắn. Giá trị của m là
 Xem đáp án
Xem đáp án
H2NCH(CH3)COOH + HCl → ClH3NCH(CH3)COOH
nAlaHCl = nAla = 0,02 → mAlaHCl = 2,51 gam
Chọn C
Câu 31:
Cho sơ đồ các phản ứng sau:
(1) X + 10X1 (t°) → 2X2↑ + 4Na2SO4 + 2X3 + 30H2O
(2) X3 + CO2 + 2H2O → X4 + X5↓
(3) 2X5 (t°) → Al2O3 + 3H2O
(4) X4 + X1 → X6 + H2O
Các chất X1, X3 và X6 thỏa mãn sơ đồ trên lần lượt là
 Xem đáp án
Xem đáp án
H2NCH(CH3)COOH + HCl → ClH3NCH(CH3)COOH
nAlaHCl = nAla = 0,02 → mAlaHCl = 2,51 gam
Chọn A
Câu 32:
Một loại bình gas 25 kg có khối lượng vỏ là 13 kg, khối lượng khí trong bình là 12 kg. Trong bình (tính theo khối lượng) có chứa 1,7% là etan, 96,8% là propan, còn lại là butan. Biết rằng khi đốt cháy hoàn toàn 1 mol một số ankan bằng oxi dư sẽ tỏa ra nhiệt lượng như sau:
|
Chất |
Etan |
Propan |
Butan |
|
Nhiệt lượng (kJ) |
1560 |
2219 |
2877 |
Một gia đình sử dụng loại bình gas trên để đun nấu. Trung bình mỗi ngày gia đình đó cần tiêu thụ lượng nhiệt cho đun nấu là 12000 kJ. Hãy cho biết sau khoảng bao nhiêu ngày thì gia đình đó sử dụng hết bình gas trên?
 Xem đáp án
Xem đáp án
nC2H6 = 12000.1,7%/30 = 6,8 mol
nC3H8 = 12000.96,8%/44 = 264 mol
nC4H10 = 12000.1,5%/58 = 3,1 mol
Số ngày sử dụng = (6,8.1560 + 264.2219 + 3,1.2877)/12000 ≈ 50 ngày
Chọn B
Câu 33:
Hòa tan 21,76 gam hỗn hợp X gồm Cu và Fe3O4 vào 105,84 gam dung dịch HNO3 50%, thu được dung dịch Y và khí Z (gồm NO và NO2). Cho 500 ml dung dịch chứa hỗn hợp NaOH 0,8M và KOH 1M vào lượng dung dịch Y ở trên. Sau khi kết thúc phản ứng thu được chất rắn T và dung dịch Q. Nung nóng toàn bộ T trong điều kiện có mặt oxi thu được 23,2 gam chất rắn N (gồm CuO và Fe2O3). Cô cạn dung dịch Q để làm bay hơi nước thu được 78,2 gam chất rắn M khan. Các phản ứng xảy ra hoàn toàn. Giá trị nồng độ phần trăm của muối Fe(NO3)3 trong dung dịch Y gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
nNaOH = 0,4; nKOH = 0,5
Nếu kiềm đã phản ứng hết thì Q chứa NaNO3 (0,4) và KNO3 (0,5) → m rắn = 84,5 > 78,2 → Q còn OH- dư
Q chứa Na+ (0,4), K+ (0,5), NO3- (u) và OH- dư (v)
Bảo toàn điện tích: 0,4 + 0,5 = u + v
m rắn = 0,4.23 + 0,5.39 + 62u + 17v = 78,2
→ u = 0,76 và v = 0,14
X gồm Cu (a) và Fe3O4 (b) → mX = 64a + 232b = 21,76
mN = 80a + 160.1,5b = 23,2
→ a = 0,05; b = 0,08
nHNO3 ban đầu = 105,84.50%/63 = 0,84
Dễ thấy nNO3- (Y) = 0,76 < 2a + 3.3b nên Y chứa Cu2+ (0,05), Fe2+ (x) và Fe3+ (y)
Bảo toàn Fe → x + y = 3b
Bảo toàn điện tích cho Y: 0,05.2 + 2x + 3y = 0,76
→ x = 0,06; y = 0,18
Z gồm NO (c) và NO2 (d), bảo toàn N → nZ = c + d = 0,84 – 0,76
nH+ = 0,84 = 4c + 2d + 2.4b
(1)(2) → c = 0,02; d = 0,06
→ mddY = mX + mddHNO3 – mZ = 124,24
C%Fe(NO3)3 = 242y/124,24 = 35,06%
Chọn C
Câu 34:
Hỗn hợp T gồm 2 triglixerit X1 và X2. Thủy phân hoàn toàn m gam hỗn hợp T bằng dung dịch NaOH dư, đun nóng, thu được hỗn hợp sản phẩm trong đó có chứa 43,14 gam muối. Mặt khác, khi đốt cháy hoàn toàn m gam hỗn hợp T bằng oxi dư thu được 2,67 mol CO2 và 2,45 mol nước. Giá trị của m là
 Xem đáp án
Xem đáp án
nT = x, bảo toàn khối lượng:
(2,67.12 + 2,45.2 + 16.6x) + 40.3x = 43,14 + 92x
→ x = 0,05
→ mX = 2,67.12 + 2,45.2 + 16.6x = 41,74 gam
Chọn A
Câu 35:
Cho các thí nghiệm sau:
(a) Cho dung dịch nước vôi trong vào dung dịch Ba(HCO3)2.
(b) Cho dung dịch NaOH dư vào dung dịch chứa hỗn hợp CrCl3.
(c) Cho dung dịch KHSO4 vào dung dịch BaCl2.
(d) Cho bột Cu vào dung dịch Fe2(SO4)3 dư.
(đ) Cho dung dịch H3PO4 vào dung dịch AgNO3.
Số thí nghiệm thu được sản phẩm có chất kết tủa là
 Xem đáp án
Xem đáp án
(a) Ca((OH)2 + Ba(HCO3)2 → CaCO3 + BaCO3 + H2O
(b) NaOH dư + CrCl3 → NaCrO2 + NaCl + H2O
(c) KHSO4 + BaCl2 → BaSO4 + HCl + KCl
(d) Cu + Fe2(SO4)3 dư → CuSO4 + FeSO4
(đ) Không phản ứng.
Chọn D
Câu 36:
Cho các phát biểu sau:
(a) Peptit Gly-Ala-Val có đơn vị aminoaxit đầu N là Val.
(b) Hợp chất X có công thức phân tử C4H10O2 không thể là este.
(c) Dung dịch anilin phản ứng với dung dịch nước Br2 tạo thành kết tủa trắng.
(d) Thủy phân saccarozơ trong dung dịch kiềm, đun nóng sẽ thu được hai loại monosaccarit.
(đ) Thành phần nguyên tố của tơ visco không chứa nitơ.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
(a) Sai, peptit Gly-Ala-Val có đơn vị aminoaxit đầu N là Gly.
(b) Đúng, C4H10O2 có k = 0, trong khi este có k ≥ 1
(c) Đúng
(d) Sai, saccarozơ không bị thủy phân trong dung dịch kiềm.
(đ) Đúng
Chọn D
Câu 37:
Cho X (C4H4O4) là hợp chất hữu cơ tạp chức, mạch hở. X chứa các nhóm chức trong số các nhóm chức sau: -OH (ancol); -CHO (anđehit); -COOH (axit cacboxylic); -COO- (este). Cho các chuyển hóa sau:
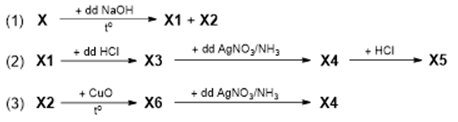
Biết X1, X2, X3, X4, X5 và X6 đều là các hợp chất hữu cơ, có cấu tạo mạch hở. Hợp chất X4 có công thức phân tử C2H8O4N2. Cho các nhận xét sau đây:
(a) X có thể phản ứng với H2 (xúc tác Ni, đun nóng).
(b) X1 có phân tử khối là 74.
(c) X2 có thể tham gia phản ứng tráng bạc.
(d) Phân tử X3 có hai nguyên tử hiđro.
(đ) Phân tử X4 không chứa liên kết π.
(e) X5, X6 là hợp chất đa chức.
Số nhận xét đúng là
 Xem đáp án
Xem đáp án
X4 là C2H8O4N2 hay (COONH4)2; X5 là (COOH)2
→ X3 là OHC-COOH → X1 là OHC-COONa
X6 là (CHO)2 → X2 là OHC-CH2OH
X là OHC-COO-CH2-CHO
(a) Đúng:
OHC-COO-CH2-CHO + 2H2 → HOCH2-COO-CH2-CH2OH
(b) Sai, MX1 = 96
(c) Đúng, X2 chứa -CHO nên có tráng bạc.
(d) Đúng, X3 là C2H2O3
(đ) Đúng, X5 là axit 2 chức, X6 là anđehit 2 chức.
Chọn B
Câu 38:
Este X1 mạch hở được tạo thành từ axit đơn chức Y1 và ancol no, ba chức Z1. Este X2 mạch hở, được tạo thành từ hai axit no, đơn chức Y2, Y3 và ancol no, hai chức Z2. Ancol Z1 và Z2 có cùng số nguyên tử cacbon. Đốt cháy m gam este X1 cần vừa đủ 2,8 lít khí O2, thu được 0,19 mol hỗn hợp CO2 và nước. Đốt cháy 9,17 gam hỗn hợp E gồm X1, X2 bằng oxi dư thu được 0,435 mol CO2. Mặt khác, đun nóng 0,08 mol hỗn hợp E cần vừa đủ 100 ml dung dịch NaOH 2,1M thu được dung dịch F. Cô cạn dung dịch F thu được hỗn hợp ancol H (gồm Z1 và Z2) và m gam hỗn hợp chất rắn G gồm ba muối. Các phản ứng xảy ra hoàn toàn. Giá trị của m là
 Xem đáp án
Xem đáp án
X1 dạng CxHyO6:
CxHyO6 + (x + 0,25y – 3)O2 → xCO2 + 0,5yH2O
nO2 = 0,125; nCO2 + nH2O = 0,19
→ 0,125(x + 0,5y) = 0,19(x + 0,25y – 3)
→ 0,065x – 0,015y = 0,57
→ 13x – 3y = 114
Với y chẵn và y ≤ 2x + 2 – 6 → Chọn x = 12; y = 14
X1 là C12H14O6 hay (C2H3COO)3C3H5
Y1 là C2H3COOH; Z1 là C3H5(OH)3 → Z2 là C3H6(OH)2
Trong phản ứng với NaOH:
nE = nX1 + nX2 = 0,08 và nNaOH = 3nX1 + 2nX2 = 0,21
→ nX1 = 0,05; nX2 = 0,03
9,17 gam hỗn hợp E gồm (C2H3COO)3C3H5 (5e) và (CnH2n+1COO)2C3H6 (3e)
mE = 254.5e + 3e(28n + 132) = 9,17
nCO2 = 12.5e + 3e(2n + 5) = 0,435
→ e = 0,005; en = 0,01 → n = 2
0,08 mol E + NaOH tạo muối gồm C2H3COONa (0,15) và C2H5COONa (0,06)
→ m muối = 19,86 gam
(Chú ý: C2H5COONa là mối trung bình tạo ra từ X2)
Chọn C
Câu 39:
Dung dịch X có hòa tan CuSO4 x mol và KCl y mol. Tiến hành điện phân dung dịch X (với điện cực trơ, màng ngăn xốp) bằng dòng điện một chiều có cường độ không đổi. Hiệu suất của các quá trình điện phân là 100%. Kết quả thí nghiệm thu được tương ứng với thời gian điện phân như sau:
|
Thời gian điện phân |
Kết quả |
|
t giây |
Bắt đầu có khí thoát ra ở catot |
|
2t giây |
Khối lượng dung dịch thu được giảm đi so với ban đầu 2,08 gam |
|
3,5t giây |
Thể tích khí thu được anot gấp 1,2 lần thể tích khí thu được ở catot |
Tổng giá trị (x + y) là
 Xem đáp án
Xem đáp án
Chọn A
t giây bắt đầu có khí thoát ra ở catot → ne trong t giây = 2x
Lúc 3,5t giây có ne = 7x, tại catot: nCu = x → nH2 = 2,5x
n khí anot = 1,2.2,5x = 3x < ne/2 nên đã có O2
nCl2 = 0,5y và nO2 = z → 0,5y + z = 3x
ne = 2.0,5y + 4z = 7x
→ y = 5x; z = 0,5x
Lúc 2t giây có ne = 4x < y nên Cl- chưa hết.
Catot: nCu = x → nH2 = x
Anot: nCl2 = 2x
m giảm = 64x + 2x + 71.2x = 2,08 → x = 0,01
→ y = 0,05
→ x + y = 0,06
Câu 40:
Theo khuyến cáo, mỗi hecta (1 hecta = 10.000 m²) đất trồng lúa, người nông dân cần cung cấp 70 kg N; 35,5 kg P2O5 và 30 kg K2O. Thực hiện đúng theo khuyến cáo trên, người nông dân sử dụng loại phân NPK 20-20-15 trộn với phân kali (độ dinh dưỡng 60%) và phân ure (độ dinh dưỡng 46%). Tổng khối lượng phân bón đã sử dụng cho một hecta đất trên gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
Khối lượng phân mỗi loại NPK (x kg), phân kali (y kg) và phân ure (z kg)
mN = 20%x + 46%z = 70
mP2O5 = 20%x = 35,5
mK2O = 15%x + 60%y = 30
→ x = 177,5; y = 5,625; z = 75
→ x + y + z = 256,125
Chọn B
