(2023) Đề thi thử Hóa THPT Hàn Thuyên, Bắc Ninh (Lần 3) có đáp án
(2023) Đề thi thử Hóa THPT Hàn Thuyên, Bắc Ninh (Lần 3) có đáp án
-
1176 lượt thi
-
40 câu hỏi
-
60 phút
Danh sách câu hỏi
Câu 1:
Phát biểu nào sau đây sai?
 Xem đáp án
Xem đáp án
A. Đúng, C, O hóa trị chẵn nên các hợp chất chứa C, H, O thì số H luôn chẵn.
B. Sai. Sản phẩm của phản ứng xà phòng hoá chất béo là muối của axit béo và glyxerol.
C. Đúng, do ancol có liên kết H liên phân tử, este không có liên kết này.
D. Đúng, bằng cách hiđro hóa, có thể chuyển hoá chất béo lỏng thành chất béo rắn.
Chọn B
Câu 3:
Axit benzoic được sử dụng như một chất bảo quản thực phẩm (kí hiệu là E-210) cho xúc xích, nước sốt cà chua, mù tạt, bơ thực vật…. Nó ức chế sự phát triển của nấm mốc, nấm men và một số vi khuẩn. Công thức của Axit benzoic là:
 Xem đáp án
Xem đáp án
Chọn A
Câu 5:
Hỗn hợp X gồm metan, propen, và isopren. Đốt cháy hoàn toàn 15,0 gam X cần vừa đủ 36,96 lít O2 (đktc). Mặt khác, a mol X phản ứng tối đa với 0,1 mol brom. Giá trị của a là:
 Xem đáp án
Xem đáp án
X gồm CH4, C3H6, C5H8 có dạng chung CxHx+3
nCxHx+3 = 15/(13x + 3)
—> nO2 = (1,25x + 0,75).15/(13x + 3) = 1,65
—> x = 7/3
k = (2x + 2 – x – 3)/2 = 2/3
—> nBr2 = ka = 0,1 —> a = 0,15
Chọn D
Câu 6:
Chất khí nào sau đây không cháy trong oxi?
 Xem đáp án
Xem đáp án
A. C2H2 + O2 —> CO2 + H2O
B. CH4 + O2 —> CO2 + H2O
C. CO2 không cháy do C đã có số oxi hóa tối đa.
D. NH3 + O2 —> N2 + H2O
Chọn C
Câu 7:
Dung dịch NaOH phản ứng được với dung dịch của chất nào sau đây?
 Xem đáp án
Xem đáp án
NaOH + NaHCO3 —> Na2CO3 + H2O
Chọn A
Câu 9:
Trùng hợp 8,96 lít etilen (đktc), nếu hiệu suất phản ứng là 75% thì khối lượng polime thu được là
 Xem đáp án
Xem đáp án
Bảo toàn khối lượng:
mPE = mC2H4 phản ứng = 28.75%.0,4 = 8,4 gam
Chọn C
Câu 10:
Cho 30,45 gam tripeptit mạch hở Gly−Ala−Gly vào dung dịch NaOH dư sau phản ứng hoàn toàn thấy có m gam NaOH phản ứng. Giá trị của m là
 Xem đáp án
Xem đáp án
Gly−Ala−Gly + 3NaOH —> 2GlyNa + AlaNa + H2O
nGly−Ala−Gly = 0,15 —> nNaOH phản ứng = 0,45
—> mNaOH phản ứng = 18 gam
Chọn B
Câu 11:
Hòa tan hết m gam hỗn hợp X gồm Na2O, K, K2O, Ba, BaO (trong đó oxi chiếm 8% khối lượng hỗn hợp) vào lượng nước dư thu được dung dịch Y và 1,792 lít H2 (đktc). Dung dịch Y hòa tan tối đa 8,64 gam nhôm. Giá trị của m là
 Xem đáp án
Xem đáp án
nOH-(Y) = nAl = 0,32
Bảo toàn electron: 0,32 = 2nH2 + 2nO
—> nO = 0,08
—> mX = 0,08.16/8% = 16 gam
Chọn B
Câu 13:
Có mấy hợp chất có công thức phân tử C3H9O2N có chung tính chất vừa tác dụng với HCl và vừa tác dụng với NaOH?
 Xem đáp án
Xem đáp án
Các cấu tạo thỏa mãn:
CH3CH2COONH4
CH3COONH3CH3
HCOONH3CH2CH3
HCOONH2(CH3)2
Chọn C
Câu 14:
Hòa tan hoàn toàn 3,2 gam một oxit kim loại cần vừa đủ 40 ml dung dịch HCl 2M. Công thức oxit đó là:
 Xem đáp án
Xem đáp án
nHCl = 0,08 —> nO = nH2O = 0,04
Oxit dạng RxOy (0,04/y mol)
—> M = Rx + 16y = 3,2y/0,04
—> R = 64y/x
—> x = y = 1 và R = 64: R là Cu
Chọn B
Câu 15:
Tiến hành thí nghiệm theo các bước sau:
Bước 1: Cho 1 ml dung dịch AgNO3 1% vào ống nghiệm sạch.
Bước 2: Thêm từ từ từng giọt dung dịch NH3, lắc đều cho đến khi kết tủa tan hết.
Bước 3: Thêm tiếp khoảng 1 ml dung dịch glucozơ 1% vào ống nghiệm; đun nóng nhẹ.
Phát biểu nào sau đây sai?
 Xem đáp án
Xem đáp án
A. Đúng
B. Sai, thí nghiệm trên chứng minh glucozơ có tính chất của anđehit
C. Đúng
D. Đúng, glucozơ khử Ag+ thành Ag.
Chọn B
Câu 16:
Khẳng định nào sau đây là không đúng
 Xem đáp án
Xem đáp án
B sai, Al không điều chế được bằng phương pháp nhiệt luyện. Điều chế Al bằng cách điện phân Al2O3 nóng chảy.
Chọn B
Câu 19:
Cho m gam hỗn hợp K và Ba tan hết trong nước thu được dung dịch X và 0,1 mol H2. Để trung hòa hết dung dịch X cần V ml dung dịch HCl 1M. Giá trị của V là
 Xem đáp án
Xem đáp án
2H2O + 2e —> 2OH- + H2
H+ + OH- —> H2O
nH+ = nOH- = 2nH2 = 0,2 —> nHCl = 0,2
—> VddHCl = 200 ml
Chọn B
Câu 20:
Etyl axetat không tác dụng với?
 Xem đáp án
Xem đáp án
A. CH3COOC2H5 + O2 —> CO2 + H2O
B. CH3COOC2H5 + Ba(OH)2 —> (CH3COO)2Ba + C2H5OH
C. Không phản ứng
D. CH3COOC2H5 + H2O ⇔ CH3COOH + C2H5OH
Chọn C
Câu 21:
Hỗn hợp X gồm vinyl axetat, metyl axetat, etyl fomat. Đốt cháy 3,08 gam X thu được 2,16 gam H2O. Thành phần % về khối lượng vinyl axetat trong X là?
 Xem đáp án
Xem đáp án
Vinyl axetat C4H6O2 (a mol)
Metyl axetat và etyl fomat có cùng công thức C3H6O2 (b mol)
mX = 86a + 74b = 3,08
nH2O = 3a + 3b = 0,12
—> a = 0,01 và b = 0,03
—> %mC4H6O2 = 27,92%
Chọn A
Câu 22:
Cho dung dịch chứa a mol Ca(HCO3)2 tác dụng với dung dịch chứa a mol chất tan X. Để thu được lượng kết tủa lớn nhất thì X là
 Xem đáp án
Xem đáp án
Để thu được lượng kết tủa lớn nhất thì X là Ba(OH)2:
Ca(HCO3)2 + Ba(OH)2 —> CaCO3 + BaCO3 + 2H2O
Chọn D
Câu 25:
Hỗn hợp X gồm glyxin, alanin và axit glutamic. Trong X, nguyên tố oxi chiếm 40% về khối lượng. Cho m gam X tác dụng hoàn toàn với lượng vừa đủ dung dịch gồm NaOH 2,0% và KOH 2,8%, thu được 8,8 gam muối. Giá trị của m là
 Xem đáp án
Xem đáp án
nNaOH : nKOH = 2/40 : 2,8/56 = 1 : 1
nKOH = nNaOH = x —> nH2O = 2x
—> nO(X) = 4x —> mX = 16.4x/40% = 160x
Bảo toàn khối lượng:
160x + 56x + 40x = 8,8 + 18.2x —> x = 0,04
—> mX = 160x = 6,4 gam
Chọn B
Câu 27:
Đun nóng 0,2 mol este đơn chức X với 135 ml dung dịch NaOH 2M. Sau phản ứng xảy ra hoàn toàn, cô cạn dung dịch thu được ancol etylic và 19,2 gam chất rắn khan. Công thức cấu tạo của X là?
 Xem đáp án
Xem đáp án
Chất rắn khan gồm RCOONa (0,2 mol) và NaOH dư (0,07 mol)
m rắn = 0,2(R + 67) + 0,07.40 = 19,2
—> R = 15: -CH3
X là CH3COOC2H5
Chọn D
Câu 28:
Hợp chất thơm X có công thức phân tử C7H8O phản ứng với Na tạo H2, nhưng không phản ứng với NaOH. Tên gọi của X là
 Xem đáp án
Xem đáp án
X + Na tạo H2 nên X có -OH.
X không phản ứng với NaOH —> X không có -OH phenol.
—> X là C6H5CH2OH (Ancol benzylic)
Chọn B
Câu 30:
Cho hình vẽ mô tả thí nghiệm điều chế HNO3 trong phòng thí nghiệm như sau
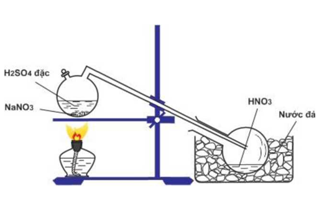
Phát biểu không đúng về quá trình điều chế là
 Xem đáp án
Xem đáp án
A. Sai, HCl đặc cũng là axit mạnh, dễ bay hơi giống HNO3 nên không đẩy HNO3 ra khỏi muối được. Phải dùng axit mạnh, không bay hơi là H2SO4.
B. Đúng, HNO3 thoát ra dạng hơi nên cần làm lạnh để nó ngưng tụ lại.
C. Đúng, đun nóng làm hơi HNO3 thoát ra nhanh.
D. Đúng
Chọn A
Câu 31:
Tiến hành các thí nghiệm sau:
(1) Cho lá sắt vào dụng dịch HCl có thêm vài giọt CuSO4
(2) Cho lá sắt vào dụng dịch FeCl3
(3) Cho lá thép vào dụng dịch ZnSO4
(4) Cho lá sắt vào dụng dịch CuSO4
(5) Cho lá kẽm vào dụng dịch HCl
Số trường hợp xảy ra sự ăn mòn điện hóa là
 Xem đáp án
Xem đáp án
(1) Có ăn mòn điện hóa, do có đủ 2 điện cực (Fe-Cu, trong đó Cu tạo ra do Fe khử Cu2+) và môi trường điện li.
(2) Không ăn mòn điện hóa do không có đủ 2 điện cực.
(3) Có ăn mòn điện hóa, do có đủ 2 điện cực (Fe-C) và môi trường điện li.
(4) Có ăn mòn điện hóa, giống (1).
(5) Không ăn mòn điện hóa do không có đủ 2 điện cực.
Chọn D
Câu 32:
Cho các phát biểu sau :
(1) Ở người, nồng độ glucozơ trong máu duy trì ổn định ở mức 0,1%.
(2) Oxi hóa hoàn toàn glucozơ bằng hiđro (xúc tác Ni, t°) thu được sorbitol.
(3) Tơ xenlulozơ axetat thuộc loại tơ hóa học.
(4) Thủy phân este đơn chức trong môi trường bazơ luôn cho sản phẩm là muối và ancol.
(5) Số nguyên tử N có trong phân tử đipeptit Glu-Lys là 2.
(6) Xenlulozơ trinitrat là nguyên liệu để sản xuất tơ nhân tạo và chế tạo thuốc súng không khói.
Số phát biểu đúng là :
 Xem đáp án
Xem đáp án
(1) Đúng, khi khỏe mạnh nồng độ glucozơ trong máu duy trì ổn định ở mức 0,1%.
(2) Sai, khử glucozơ bằng hiđro (xúc tác Ni, t°) thu được sorbitol.
(3) Đúng
(4) Sai, có thể cho 2 muối (ví dụ CH3COOC6H5) hoặc muối và anđehit (ví dụ CH3COOCH=CH2)…
(5) Sai, Glu có 1N, Lys có 2N nên Glu-Lys có 3N.
(6) Sai, xenlulozơ trinitrat là nguyên liệu để sản xuất thuốc súng không khói.
Chọn A
Câu 33:
Hỗn hợp E gồm este đơn chức X và este hai chức Y (X, Y đều no, mạch hở). Xà phòng hóa hoàn toàn 20,24 gam E cần vừa đủ 140 ml dung dịch NaOH 2M, thu được hai muối có tổng khối lượng a gam và hỗn hợp T gồm hai ancol có cùng số nguyên tử cacbon. Đốt cháy toàn bộ T, thu được 8,064 lít khí CO2 (đktc) và 9,72 gam H2O. Giá trị của a gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
nNaOH = 0,28
Đốt T —> nCO2 = 0,36 và nH2O = 0,54
—> nT = nH2O – nCO2 = 0,18
—> Số C = nCO2/nT = 2
—> T gồm C2H5OH (0,08) và C2H4(OH)2 (0,1)
Bảo toàn khối lượng:
mE + mNaOH = m muối + mT
—> m muối = 21,56
Chọn C
Câu 34:
Nung m gam hỗn hợp gồm Mg và Cu(NO3)2 trong điều kiện không có không khí, sau một thời gian thu được chất rắn X và 10,08 lít (đktc) hỗn hợp khí gồm NO2 và O2. Hòa tan hoàn toàn X bằng 650 ml dung dịch HCl 2M, thu được dung dịch Y chỉ chứa 71,87 gam muối clorua và 0,05 mol hỗn hợp khí Z gồm N2 và H2. Tỉ khối của Z so với He bằng 5,7. Giá trị của m gần giá trị nào nhất sau đây?
 Xem đáp án
Xem đáp án
Đặt nMg = a và nCu(NO3)2 = b
nNO2 + nO2 = 0,45
Bảo toàn O —> nO trong X = 6b – 0,45.2 = 6b – 0,9
—> nH2O = 6b – 0,9
Trong Z tính được nN2 = 0,04 và nH2 = 0,01
Bảo toàn H:
nHCl = 4nNH4Cl + 2nH2 + 2nH2O
—> nNH4Cl = (3,08 – 12b)/4
Bảo toàn Cl:
nHCl = 2a + 2b + (3,08 – 12b)/4 = 1,3
m muối = 95a + 135b + 53,5(3,08 – 12b)/4 = 71,87
—> a = 0,39 và b = 0,25
—> m = 56,36 gam
Chọn B
Câu 35:
Cho các phát biểu sau:
(a) Kim loại đồng tan trong dung dịch FeCl2 dư.
(b) Hỗn hợp gồm Cu và Fe3O4 có số mol bằng nhau tan hết trong dung dịch HCl dư.
(c) Dung dịch AgNO3 không tác dụng với dung dịch Fe(NO3)2.
(d) Ion Ag+ có tính oxi hóa mạnh hơn ion Fe2+.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
(a) Sai, Cu không phản ứng với FeCl2.
(b) Đúng: Cu + Fe3O4 + 8HCl —> CuCl2 + 3FeCl2 + 4H2O
(c) Sai: AgNO3 + Fe(NO3)2 —> Ag + Fe(NO3)3
(d) Đúng
Chọn D
Câu 36:
Cho các phát biểu sau:
(a) Điện phân dung dịch NaCl (điện cực trơ), thu được khí H2 ở catot.
(b) Cho CO dư qua hỗn hợp Al2O3 và CuO đun nóng đến phản ứng hoàn toàn, thu được Al và Cu.
(c) Nhúng thanh Zn vào dung dịch chứa CuSO4 và H2SO4, có xuất hiện ăn mòn điện hóa.
(d) Kim loại có nhiệt độ nóng chảy thấp nhất là Hg, kim loại dẫn điện tốt nhất là Ag.
(e) Cho dung dịch AgNO3 dư vào dung dịch FeCl2, thu được chất rắn gồm Ag và AgCl.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
(a) Đúng: NaCl + H2O —> H2 (catot) + Cl2 (anot) + NaOH
Nếu không có màng ngăn: Cl2 + NaOH —> NaCl + NaClO + H2O
(b) Sai, CO khử được oxit kim loại sau Al nên thu được Al2O3 và Cu
(c) Đúng, do có đủ điều kiện: điện cực Zn-Cu (Cu vừa tạo ra do Zn khử Cu2+) và môi trường điện li.
(d) Đúng
(e) Đúng: FeCl2 + AgNO3 dư —> Fe(NO3)3 + AgCl + Ag
Chọn A
Câu 37:
Điện phân dung dịch X chứa hỗn hợp gồm CuSO4 và NaCl (có tỉ lệ mol tương ứng là 1 : 3) với điện cực trơ, màng ngăn xốp, cường độ dòng điện không đổi 2A. Sau thời gian điện phân t (giờ), thu được dung dịch Y (chứa hai chất tan) có khối lượng giảm 12,45 gam so với dung dịch X. Dung dịch Y phản ứng vừa hết với 3,06 gam Al2O3. Bỏ qua sự hoàn tan của khí trong nước và sự bay hơi của hơi nước, hiệu suất điện phân 100%. Giá trị của t gần nhất với giá trị nào sau đây?.
 Xem đáp án
Xem đáp án
Dung dịch Y chứa hai chất tan gồm Na2SO4 và NaOH
nAl2O3 = 0,03 —> nNaOH = 0,06
Đặt nCuSO4 = a —> nNa2SO4 = a
Bảo toàn Na —> nNaCl = 2a + 0,06
Theo đề —> 2a + 0,06 = 3a —> a = 0,06
Catot: nCu = 0,06 và nH2 = u
Anot: nCl2 = 0,09 và nO2 = v
Bảo toàn electron:
2u + 0,06.2 = 4v + 0,09.2
m giảm = 0,06.64 + 2u + 0,09.71 + 32v = 12,45
—> u = 0,15 và v = 0,06
—> ne = 2u + 0,06.2 = 0,42
ne = It/F —> t = 20265s = 5,63h
Chọn D
Câu 38:
Dung dịch A chứa a mol Ba(OH)2. Cho m gam NaOH vào A sau đó sục CO2 (dư) vào ta thấy lượng kết tủa biến đổi theo đồ thị
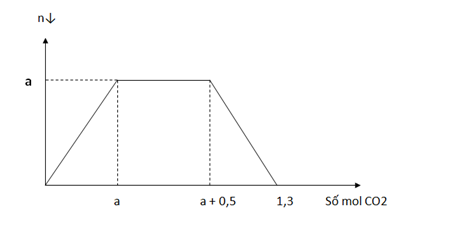
Giá trị của a và m là
 Xem đáp án
Xem đáp án
Đoạn đồ thị nằm ngang ứng với sự tạo thành NaHCO3
—> nNaHCO3 = nCO2 = a + 0,5 – a = 0,5
—> nNaOH = 0,5
—> m = 20 gam
Khi nCO2 = 1,3 thì tạo 2 muối axit NaHCO3 và Ba(HCO3)2.
Bảo toàn C —> nBa(HCO3)2 = 0,4
—> nBa(OH)2 = 0,4
Chọn C
Câu 39:
Cho các phát biểu sau:
(1) Chất béo là trieste của glixerol với axit béo.
(2) Chất béo nhẹ hơn nước và không tan trong nước.
(3) Glucozơ thuộc loại monosaccarit.
(4) Anilin là một bazơ, dung dịch của nó làm giấy quỳ tím chuyển màu xanh.
(5) Tất cả các peptit đều có phản ứng với Cu(OH)2 tạo thành hợp chất màu tím.
(6) Dung dịch saccarozơ không tham gia phản ứng tráng bạc.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
(1)(2)(3) Đúng
(4) Sai, anilin có tính bazơ rất yếu nên dung dịch của nó không làm giấy quỳ tím chuyển màu.
(5) Sai, dipeptit không có phản ứng màu biure này.
(6) Đúng
Chọn D
Câu 40:
Cho các sơ đồ phản ứng sau:
C8H14O4 + 2NaOH → X1 + X2 + H2O
X1 + H2SO4 → X3 + Na2SO4
X3 + X4 → Nilon-6,6 + H2O
Phát biểu nào sau đây đúng?
 Xem đáp án
Xem đáp án
(2) —> X1 là muối, X3 là axit
(3) —> X3 là HOOC-(CH2)4-COOH và X4 là NH2-(CH2)6-NH2
—> X1 là NaOOC-(CH2)4-COONa
Phản ứng 1 có H2O nên chất tham gia còn 1 nhóm COOH.
C8H14O4 là HOOC-(CH2)4-COO-C2H5; X2 là C2H5OH
A. Đúng
B. Sai, C2H5OH có phân tử khối nhỏ hơn và liên kết H kém bền hơn CH3COOH nên C2H5OH) có nhiệt độ sôi thấp hơn CH3COOH
C. Sai, X4 làm quỳ tím chuyển sang màu xanh.
D. Sai, dạng axit luôn có nhiệt độ nóng chảy thấp hơn dạng muối.
Chọn A
