(2023) Đề thi thử Hóa học Sở giáo dục và đào tạo Bắc Giang (Lần 2) có đáp án
(2023) Đề thi thử Hóa học Sở giáo dục và đào tạo Bắc Giang (Lần 2) có đáp án
-
929 lượt thi
-
40 câu hỏi
-
60 phút
Danh sách câu hỏi
Câu 2:
Có thể dùng lượng vừa đủ chất nào sau đây để làm mềm nước cứng tạm thời?
 Xem đáp án
Xem đáp án
Có thể dùng lượng vừa đủ NaOH để làm mềm nước cứng tạm thời:
M(HCO3)2 + NaOH → MCO3 + NaHCO3 + H2O
Chọn A
Câu 3:
Để bảo vệ vỏ tàu biển làm bằng thép, người ta thường gắn lên vỏ tàu biển (phía ngoài, tiếp xúc với nước biển) các tấm kim loại nào sau đây?
 Xem đáp án
Xem đáp án
Câu 21:
Cho 4 dung dịch riêng biệt: BaCl2, NaOH, KHSO4 và AgNO3. Số dung dịch có khả năng phản ứng với FeSO4 là
 Xem đáp án
Xem đáp án
Có 3 dung dịch có khả năng phản ứng với FeSO4 là:
BaCl2 + FeSO4 → FeCl2 + BaSO4
NaOH + FeSO4 → Fe(OH)2 + Na2SO4
AgNO3 + FeSO4 → Ag2SO4 + Ag + Fe(NO3)3
Chọn A
Câu 22:
Glucozơ lên men thành ancol etylic theo phản ứng sau: C6H12O6 (enzim) → 2C2H5OH + 2CO2. Để thu được 46 gam C2H5OH cần dùng m gam glucozơ. Biết hiệu suất của quá trình lên men là 60%. Giá trị của m là
 Xem đáp án
Xem đáp án
C6H12O6 (enzim) → 2C2H5OH + 2CO2
mC6H12O6 = 46.180/(46.2.60%) = 150 gam
Chọn A
Câu 23:
Cho khí H2 (dư) qua ống đựng 10 gam hỗn hợp X gồm Fe2O3 và Al2O3 nung nóng. Sau khi các phản ứng xảy ra hoàn toàn, thu được 7,6 gam chất rắn. Khối lượng của Al2O3 trong 10 gam X là ?
 Xem đáp án
Xem đáp án
Al2O3 không bị H2 khử nên:
nO(Fe2O3) = (10 – 7,6)/16 = 0,15
→ nFe2O3 = 0,05 → mAl2O3 = 10 – 0,05.160 = 2 gam
Chọn C
Câu 24:
Thí nghiệm nào sau đây không xảy ra phản ứng?
 Xem đáp án
Xem đáp án
A. Na + H2O → NaOH + H2
B. Không phản ứng
C. Al + NaHSO4 → Na2SO4 + Al2(SO4)3 + H2
D. Cu + AgNO3 → Cu(NO3)2 + Ag
Chọn B
Câu 25:
Để hòa tan hoàn toàn 10 gam oxit của kim loại R cần vừa đủ 500 ml dung dịch HCl 1M. Kim loại R là
 Xem đáp án
Xem đáp án
nHCl = 0,5 → nO = nH2O = 0,25
→ nRxOy = 0,25/y
→ Rx + 16y = 10y/0,25
→ R = 24y/x
Chọn x = y = 1 và R = 24 → R là Mg
Chọn A
Câu 26:
Khi đốt cháy hoàn toàn một amin đơn chức X, thu được 8,4 lít khí CO2, 1,4 lít khí N2 (các thể tích khí đo ở đktc) và 10,125 gam H2O. Công thức phân tử của X là
 Xem đáp án
Xem đáp án
nN2 = 0,0625 → nX = nN = 2nN2 = 0,125
nCO2 = 0,375 → Số C = nCO2/nX = 3
nH2O = 0,5625 → Số H = 2nH2O/nX = 9
→ X là C3H9N
Chọn B
Câu 27:
Este X mạch hở, có tỉ khối so với H2 bằng 44. Thủy phân hoàn toàn 22 gam X bằng dung dịch NaOH (dư), thu được 20,5 gam muối. Công thức cấu tạo thu gọn của X là
 Xem đáp án
Xem đáp án
MX = 88 → X là C4H8O2
n muối = nX = 0,25 → M muối = 82: CH3COONa
Công thức cấu tạo thu gọn của X là CH3COOC2H5
Chọn C
Câu 28:
Cacbohiđrat X là chất rắn, không màu, vị ngọt, dễ tan trong nước; X có nhiều trong quả nho chín nên được gọi là đường nho. Cho X phản ứng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3 (đun nóng), thu được sản phẩm hữu cơ Y. Tên gọi của X, Y lần lượt là
 Xem đáp án
Xem đáp án
X có nhiều trong quả nho chín nên được gọi là đường nho → X là glucozơ
X + AgNO3 trong NH3 (đun nóng), thu được sản phẩm hữu cơ Y → Y là amoni gluconat.
CH2OH-(CHOH)4-CHO + AgNO3 + NH3 + H2O → CH2OH-(CHOH)4-COONH4 + Ag + NH4NO3
Chọn D
Câu 29:
Phát biểu nào sau đây là đúng?
 Xem đáp án
Xem đáp án
A. Sai, trùng hợp stiren thu được polistiren.
B. Sai, trùng hợp buta-1,3-đien với acrilonitrin có xúc tác Na được cao su buna-N.
C. Đúng, poli (etylen terephtalat) được điều chế bằng phản ứng trùng ngưng các monome C2H4(OH)2 và p-C6H4(COOH)2 tương ứng.
D. Sai, tơ visco là tơ bán tổng hợp.
Chọn C
Câu 30:
Este X mạch hở, có công thức phân tử C4H6O2. Thủy phân X trong môi trường axit, thu được chất hữu cơ Y và ancol metylic. Phát biểu nào sau đây không đúng?
 Xem đáp án
Xem đáp án
Cấu tạo của X là CH2=CH-COOCH3 (metyl acrylat)
Y là CH2=CH-COOH
A. Đúng
B. Đúng, Y có hai liên kết pi (π), gồm 1C=C và 1C=O.
C. Đúng
D. Sai: CH2=CH-COOH + Br2 → CH2Br-CHBr-COOH
Chọn D
Câu 31:
Một loại xăng E là hỗn hợp gồm isooctan (2,2,4-trimetylpentan) và heptan có tỉ khối hơi so với He bằng 28,22. Khi sử dụng cho một số động cơ, cần trộn hơi xăng E với không khí (chứa 21% O2 theo thể tích) theo tỉ lệ thể tích tương ứng 1 : V để đốt cháy vừa đủ và hoàn toàn xăng. Giá trị của V gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
1 lít xăng E chứa C8H18 (a) và C7H16 (b)
→ a + b = 1 và 114a + 100b = 28,22.4.1
→ a = 0,92; b = 0,08
VO2 = 12,5a + 11b = 12,38 lít
→ V không khí = 12,38/21% = 58,95
Chọn A
Câu 32:
Cho các phát biểu sau:
(a) Este benzyl axetat có mùi thơm của hoa nhài.
(b) Triolein, tripanmitin đều có khả năng làm mất màu dung dịch brom.
(c) Mạch của xenlulozơ có dạng sợi, không xoắn, không nhánh.
(d) Muối mononatri glutamat được sử dụng làm bột ngọt (mì chính).
(e) Polietilen là chất dẻo mềm, được dùng làm màng mỏng, vật liệu cách điện, bình chứa.
Số phát biểu đúng là :
 Xem đáp án
Xem đáp án
(a) Đúng
(b) Sai, triolein (C17H33COO)3C3H5 có khả năng làm mất màu dung dịch brom do có 3C=C; tripanmitin (C15H31COO)3C3H5 là chất béo no nên không làm mất màu dung dịch brom.
(c)(d)(e) Đúng
Chọn B
Câu 33:
Trong bình kín không có không khí chứa 18,4 gam hỗn hợp rắn A gồm FeCO3, Fe(NO3)2, FeS và Fe, trong đó oxi chiếm 15,65% về khối lượng. Nung bình ở nhiệt độ cao đến phản ứng hoàn toàn thu được hỗn hợp rắn B và 0,08 mol hỗn hợp khí X gồm 3 khí có tỉ khối hơi so với He là a. Hòa tan hết chất rắn B trong 91 gam dung dịch H2SO4 84%. Kết thúc phản ứng thu được dung dịch Y và 0,4 mol khí SO2. Cho 740ml dung dịch NaOH 1M vào dung dịch Y thu được 23,54 gam kết tủa duy nhất. Giá trị của a là
 Xem đáp án
Xem đáp án
Trong A có nO = 0,18 mol
Khí X (0,08 mol) gồm CO2, NO2, SO2
→ Trong B chứa O (0,18 – 0,08.2 = 0,02 mol), Fe (x mol) và S (y mol)
nNaOH = 0,74
nFe(OH)3 = 0,22 → nNaOH đã trung hòa axit dư = 0,74 – 0,22.3 = 0,08 → nH2SO4 = 0,04
nH2SO4 bđ = 0,78 → nH2SO4 pư = 0,74
Bảo toàn S: y + 0,74 = 3x/2 + 0,4
Bảo toàn electron: 3x + 6y = 0,02.2 + 0,4.2
→ x = 0,24 và y = 0,02
Bảo toàn khối lượng: mX = mA – mB = 4
→ MX = 4/0,08 = 50
→ dX/He = 12,5
Chọn C
Câu 34:
Một loại quặng photphorit có chứa 73% Ca3(PO4)2, 26% CaCO3 và 1% SiO2 (phần trăm theo khối lượng). Để sản xuất supephotphat đơn từ 1 tấn quặng photphorit ở trên cần dùng vừa đủ m tấn dung dịch H2SO4 65%. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
Lấy 310 gam quặng
→ nCa3(PO4)2 = 310.73%/310 = 0,73
và nCaCO3 = 310.26%/100 = 0,806
Ca3(PO4)2 + 2H2SO4 → Ca(H2PO4)2 + 2CaSO4
CaCO3 + H2SO4 → CaSO4 + CO2 + H2O
→ nH2SO4 = 0,73.2 + 0,806 = 2,266
→ mddH2SO4 = 2,266.98/65% = 341,64
Tỉ lệ: 310 gam quặng cần 341,64 gam dung dịch H2SO4 65%.
→ 1 tấn quặng cần 1,1 tấn dung dịch H2SO4 65%.
Chọn B
Câu 35:
Tiến hành các thí nghiệm sau:
(a) Sục từ từ khí CO2 đến dư vào dung dịch Ca(OH)2.
(b) Sục từ từ khí CO2 đến dư vào dung dịch NaAlO2.
(c) Cho từ từ dung dịch NaOH đến dư vào dung dịch AlCl3.
(d) Cho từ từ dung dịch Ba(OH)2 đến dư vào dung dịch Al2(SO4)3.
(e) Cho từ từ dung dịch HCl đến dư vào dung dịch Ba(AlO2)2.
Sau khi các phản ứng xảy ra hoàn toàn, số thí nghiệm có sự tạo thành kết tủa sau đó kết tủa tan hết là :
 Xem đáp án
Xem đáp án
(a) CO2 + Ca(OH)2 → CaCO3 + H2O
CO2 + H2O + CaCO3 → Ca(HCO3)2
(b) CO2 + H2O + NaAlO2 → Al(OH)3 + NaHCO3
(c) NaOH + AlCl3 → Al(OH)3 + NaCl
Al(OH)3 + NaOH → NaAlO2 + H2O
(d) Ba(OH)2 + Al2(SO4)3 → BaSO4 + Al(OH)3
Ba(OH)2 + Al(OH)3 → Ba(AlO2)2 + H2O
(e) Ba(AlO2)2 + HCl + H2O → BaCl2 + Al(OH)3
Al(OH)3 + HCl → AlCl3 + H2O
Chọn A
Câu 36:
Hỗn hợp X gồm triglixerit Y và axit béo Z. Cho m gam X phản ứng hoàn toàn với dung dịch NaOH (dư), thu được sản phẩm hữu cơ gồm hai muối có cùng số nguyên tử cacbon và 2,76 gam glixerol. Nếu đốt cháy hết m gam X thì cần vừa đủ 3,445 mol O2, thu được 2,43 mol CO2 và 2,29 mol H2O. Khối lượng của Y trong m gam X là
 Xem đáp án
Xem đáp án
nY = nC3H5(OH)3 = 0,03
nO = 6nY + 2nZ = 2nCO2 + nH2O – 2nO2
→ nZ = 0,04
Y và Z có độ không no tương ứng là k và g
→ nCO2 – nH2O = 0,14 = 0,03(k – 1) + 0,04(g – 1)
→ 3k + 4g = 21
Với k ≥ 3 và g ≥ 1 → k = g = 3 là nghiệm duy nhất.
nC = 0,03(3CZ + 3) + 0,04CZ = 2,43 → CZ = 18
→ Y là (C17H35COO)3C3H5 (0,03 mol)
→ mY = 26,70 gam
Chọn C
Câu 37:
Hỗn hợp E gồm ba este no, mạch hở X (đơn chức), Y (hai chức), Z (ba chức) đều được tạo thành từ axit cacboxylic và ancol. Đốt cháy hoàn toàn m gam E, thu được số mol CO2 lớn hơn số mol H2O là 0,425 mol. Mặt khác, m gam E phản ứng vừa đủ với dung dịch NaOH, thu được hỗn hợp T gồm hai muối và 28,6 gam hỗn hợp Q gồm một ancol đơn chức và một ancol hai chức. Đốt cháy hoàn toàn T cần vừa đủ 0,25 mol O2, thu được CO2, 0,35 mol Na2CO3 và 0,15 mol H2O. Phần trăm khối lượng của X trong m gam E gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
nNaOH = 2nNa2CO3 = 0,7 → nO(T) = 1,4
Bảo toàn O → nCO2 = 0,35
→ nC(T) = nNa2CO3 + nCO2 = 0,7
→ T có nC = nNa → T gồm HCOONa (0,3) và (COONa)2 (0,2)
(Bảo toàn H tính nHCOONa rồi bảo toàn Na tính n(COONa)2)
Bảo toàn khối lượng → mE = 47,8
Đốt E tạo nCO2 = u và nH2O = v → u – v = 0,425
mE = 12u + 2v + 1,4.16 = 47,8
→ u = 1,875; v = 1,45
Bảo toàn C → nC(Ancol) = 1,175
Bảo toàn H → nH(Ancol) = 3,3
→ nAncol = nH/2 – nC = 0,475
Ancol gồm AOH (0,25) và B(OH)2 (0,225) (Bấm hệ nAncol và nO để tính số mol)
nC(Ancol) = 0,25CA + 0,225CB = 1,175
→ 10CA + 9CB = 47 → CA = 2 và CB = 3 là nghiệm duy nhất.
Ancol gồm C2H5OH (0,25) và C3H6(OH)2 (0,225).
X là HCOOC2H5: 0,05 mol
Z là HCOO-C3H6-OOC-COO-C2H5: 0,2 mol
Vì nC3H6(OH)2 > n(COONa)2 nên Y là (HCOO)2C3H6: 0,025 mol
→ mX = 3,7 gam
(Lưu ý: Tính trước nY = nC3H6(OH)2 – n(COONa)2, từ đó tính nX và nZ)
Chọn B
Câu 38:
Cho các phản ứng sau (các chất phản ứng theo đúng tỉ lệ mol):
(a) X + 2NaOH → X1 + X2 + X3;
(b) X1 + HCl → X4 + NaCl;
(c) X2 + HCl → X5 + NaCl;
(d) X3 + CuO (t°) → X6 + Cu + H2O.
Biết X có công thức phân tử C6H10O4 và chứa hai chức este; X1, X2 đều có hai nguyên tử cacbon trong phân tử và khối lượng mol của X1 nhỏ hơn khối lượng mol của X2. Cho các phát biểu sau:
(a) Phân tử khối của X5 là 76.
(b) X4 là hợp chất hữu cơ đa chức.
(c) X6 là anđehit axetic.
(d) Đốt cháy hoàn toàn X2 thu được số mol CO2 lớn hơn số mol H2O.
(e) Từ X3 có thể điều chế trực tiếp X4 bằng một phản ứng hóa học.
Số phát biểu không đúng là :
 Xem đáp án
Xem đáp án
(b)(c) → X1. X2 đều là các muối natri.
X1, X2 cùng C nên mỗi chất 2C → X là:
CH3COO-CH2-COO-C2H5
X1 là CH3COONa
X2 là HO-CH2-COONa
X3 là C2H5OH
X4 là CH3COOH
X5 là HO-CH2-COOH
X6 là CH3CHO
(a) Đúng, MX5 = 76
(b) Sai, X4 là hợp chất hữu cơ đơn chức.
(c) Đúng
(d) Sai, đốt X2 có nCO2 = nH2O:
2C2H3O3Na + 3O2 → Na2CO3 + 3CO2 + 3H2O
(e) Đúng: C2H5OH + O2 → CH3COOH + H2O (lên men giấm)
Chọn B
Câu 39:
Cho sơ đồ chuyển hóa:
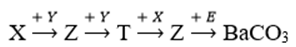
Biết chất X còn có tên gọi khác là xút ăn da; Y, Z, T là các hợp chất khác nhau; mỗi mũi tên ứng với một phản ứng. Các chất T và E thỏa mãn sơ đồ trên là
 Xem đáp án
Xem đáp án
X còn được gọi là xút ăn da → X là NaOH
→ Y là CO2, Z là Na2CO3, T là NaHCO3, E là Ba(OH)2.
(Loại E là Ba3(PO4)2 vì muối này không tan, không phản ứng với Na2CO3).
NaOH + CO2 → Na2CO3 + H2O
CO2 + H2O + Na2CO3 → NaHCO3
NaHCO3 + NaOH → Na2CO3 + H2O
Na2CO3 + Ba(OH)2 → BaCO3 + NaOH
Chọn B
Câu 40:
Hòa tan 14,35 gam muối MSO4.nH2O vào 300 ml dung dịch NaCl 0,6M, thu được dung dịch X. Tiến hành điện phân X với điện cực trơ, màng ngăn xốp, cường độ dòng điện không đổi, hiệu suất điện phân bằng 100%. Sau t giây, thấy khối lượng catot tăng m gam đồng thời ở anot thu được 2,24 lít khí (đktc). Sau 2t giây, tổng thể tích khí thoát ra từ hai điện cực là 7,28 lít (đktc). Giá trị của m là ?
 Xem đáp án
Xem đáp án
nNaCl = 0,18
Trong t giây: Anot thu được 0,1 mol khí gồm nCl2 = 0,09 → nO2 = 0,01
→ ne trong t giây = 2nCl2 + 4nO2 = 0,22
Trong t giây tiếp theo anot thu thêm được nO2 = ne/4 = 0,055
→ nH2 = n khí tổng – nCl2 – nO2 tổng = 0,17
Bảo toàn electron cho catot trong 2t giây:
2nM + 2nH2 = 0,22.2
→ nM = 0,05
→ M + 96 + 18n = 287
→ n = 7 và M = 65 là nghiệm phù hợp.
Dễ thấy ne < 2nH2 nên trong t giây đầu tiên đã có H2 bên catot
→ m tăng = mZn = 0,05.65 = 3,25
Chọn D
