(2023) Đề thi thử Hóa THPT theo đề minh họa của Bộ Giáo dục có đáp án (Đề 23)
(2023) Đề thi thử Hóa THPT theo đề minh họa của Bộ Giáo dục có đáp án (Đề 23)
-
1070 lượt thi
-
40 câu hỏi
-
60 phút
Danh sách câu hỏi
Câu 4:
Do sự thiếu hiểu biết, vào mùa đông, một số gia đình sử dụng bếp than đặt trong phòng kín để sưởi ấm, dẫn đến hiện tượng các thành viên trong gia đình bị ngộ độc khí X, có thể dẫn tới tử vong. Khí X là
 Xem đáp án
Xem đáp án
Chọn C
Câu 6:
Kim loại Ba tác dụng với H2O trong dung dịch tạo ra H2 và chất nào sau đây?
 Xem đáp án
Xem đáp án
Chọn B
Câu 11:
X là kim loại dẫn điện tốt, được dùng làm dây dẫn điện trong hệ thống điện cao thế. X là
 Xem đáp án
Xem đáp án
Chọn B
Câu 13:
Ở điều kiện thích hợp, kim loại nào sau đây bị S oxi hóa lên mức oxi hóa +3?
 Xem đáp án
Xem đáp án
Chọn B
Câu 15:
Epibatidine, một loại dầu không màu được phân lập từ da của loài ếch mũi tên độc Equadorian Epipedobates ba màu. Đây là hợp chất có tác dụng giảm đau gấp vài lần morphine, nhưng lại không gây nghiện. Cấu trúc hóa học của epibatidine mô tả như hình dưới:
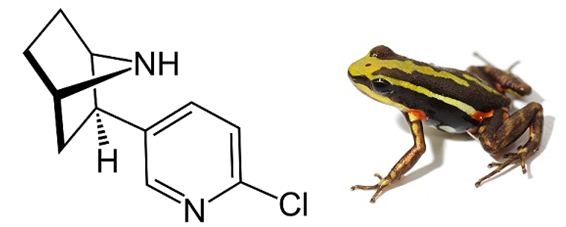
Công thức phân tử của Epibatadine là
 Xem đáp án
Xem đáp án
Chọn D
Câu 18:
Cho cốc nước cứng A, đung sôi A, để nguội, cho tiếp dung dịch Na2CO3 đến dư không thu được kết tủa. Nước cứng trong A là loại nước gì?
 Xem đáp án
Xem đáp án
Chọn C
Câu 21:
Este X có công thức phân tử C4H8O2. Thủy phân X trong dung dịch NaOH dư, thu được sản phẩm gồm natri fomat và ancol Y. Công thức của Y là
 Xem đáp án
Xem đáp án
Chọn C
Câu 22:
Cây xanh là nguồn sống quý giá của con người, là lá phổi xanh duy trì sự sống của trái đất. Chúng ta không thể tồn tại mà không có cây xanh và bảo vệ nó là trách nhiệm của tất cả chúng ta. Thống kê cho thấy, trung bình mỗi người hít thở 16 lần mỗi phút, mỗi lần hấp thụ khoảng 0,5 lít không khí. Và để bảo đảm sự sống cho 7,5 tỷ người đang sinh sống trên hành tinh này, chúng ta cần 562 tỷ cây xanh. Trung bình mỗi người mỗi năm hấp thụ tối thiểu khoảng bao nhiêu mét khối không khí? Biết 1 năm có 365 ngày.
 Xem đáp án
Xem đáp án
Chọn D
Câu 23:
Nhiệt phân hoàn toàn m gam Ca(HCO3)2, thu được CaCO3, H2O và 2,24 lít CO2 (ở đktc). Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn A
Câu 24:
Thủy phân 68,4 gam saccarozơ trong môi trường axit với hiệu suất 92%, sau phản ứng thu được hỗn hợp X. Cho toàn bộ X tác dụng với lượng dư dung dịch AgNO3 trong NH3, đun nóng, phản ứng hoàn toàn thu được m gam Ag. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn A
Câu 26:
 Xem đáp án
Xem đáp án
Đáp án D
Gồm có: poli(butađien-stien), polibutađien, poliisopren, poli(butađien-acrilonitrin)
Câu 27:
Để khử hoàn toàn m gam Fe2O3 thành kim loại Fe ở nhiệt độ cao (không có oxi) cần tối thiểu 5,4 gam kim loại Al. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn A
Câu 28:
Đốt cháy hoàn toàn 0,15 mol một amin X no, đơn chức mạch hở bằng khí oxi vừa đủ, thu được 1,2 mol hỗn hợp gồm CO2, H2O và N2. Số đồng phân bậc 1 của X là
 Xem đáp án
Xem đáp án
Chọn A
Câu 29:
Đốt cháy hoàn toàn hỗn hợp T gồm este hai chức, mạch hở X và este đơn chức Y thu được 6,54 mol CO2 và 3,6 mol H2O. Mặt khác, thủy phân hoàn toàn T cần dụng 141.285 gam dung dịch NaOH 50,96%, cô cạn dung dịch sau phản ứng thu được rắn Q gồm 3 muối (đều có phân tử khối lớn > 90 đvC). Ngưng tụ phần hơi thu được 117, 875 ml ancol etylic 40o. Biết khối lượng riêng của ancol etylic nguyên chất bằng 0,8 g/ml và của nước bằng 1 g/ml. Phần trăm khối lượng của muối có phân tử khối nhỏ nhất trong Q là
 Xem đáp án
Xem đáp án
Chọn B
Câu 30:
Đốt hỗn hợp X gồm Fe và Cu trong O2, thu được 31,2 gam hỗn hợp Y gồm Fe, Cu, Fe3O4 và CuO. Cho Y vào dung dịch chứa 0,4 mol HCl, thu được dung dịch Z chỉ chứa muối, V lít H2 và 18,4 gam chất rắn T. Cho T tác dụng với dung dịch HCl có khí thoát ra. Biết các phản ứng xảy ra hoàn toàn. Giá trị của V là
 Xem đáp án
Xem đáp án
Đáp án B
Quy hỗn hợp Y về (Fe, O, Cu) tác dụng với HCl, chất rắn T gồm Cu, Fe dư.
Gọi số mol Fe, O phản ứng là x,y mol, số mol H2 là z mol.
Câu 31:
Cho hai chất hữu cơ mạch hở E, G có cùng công thức đơn giản nhất là CH2O. Các chất E, G, X tham gia phản ứng theo đúng tỉ lệ mol như sơ đồ dưới đây:
Biết: X, Y, Z, T là các chất hữu cơ và ME < MG < 100. Cho các phát biểu sau:
(a) Đốt cháy a mol Z cần 3 mol O2 (hiệu suất phản ứng là 100%).
(b) Y được điều chế trực tiếp từ C2H4.
(c) G là hợp chất đa chức.
(d) T hòa tan được Cu(OH)2.
(e) Y có nhiệt độ sôi cao hơn E.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án D
Câu 32:
Hỗn hợp X gồm triglixerit Y và axit béo Z. Cho m gam X phản ứng hoàn toàn với dung dịch NaOH dư, thu được sản phẩm hữu cơ gồm hai muối có cùng số nguyên từ cacbon và 2,3 gam glixerol. Nếu đốt cháy hết m gam X thì cần vừa đủ 3,17 mol O2, thu được 2,235 mol CO2 và 2,11 mol H2O. Khối lượng của Y trong m gam X là
 Xem đáp án
Xem đáp án
Đáp án C
Câu 33:
Nung m gam hỗn hợp X gồm Fe, Fe(NO3)2, Fe(NO3)3 và FeCO3 trong bình kín (không có không khí). Sau khi các phản ứng xảy ra hoàn toàn, thu được chất rắn Y và khí Z có tỉ khối so với H2 là 22,5 (giả sử khí NO2 sinh ra không tham gia phản ứng nào khác). Cho Y tan hoàn toàn trong dung dịch gồm 0,01 mol KNO3 và 0,15 mol H2SO4 (loãng), thu được dung dịch chỉ chứa 21,23 gam muối trung hòa của kim loại và hỗn hợp hai khí T có tỉ khối so với H2 là 8 (trong đó có một khí hóa nâu trong không khí). Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án B
Câu 34:
Thực hiện các thí nghiệm sau:
(a) Cho dung dịch (NH4)2SO4 vào dung dịch Ba(OH)2 đun nóng.
(b) Điện phân nóng chảy Al2O3.
(c) Cho dung dịch NaHCO3 vào dung dịch CaCl2 đun nóng.
(d) Cho từ từ dung dịch hỗn hợp chứa 0,5x mol HCl, 0,25x mol H2SO4 và dung dịch chứa 1,1x mol Na2CO3.
(e) Hòa tan Fe3O4 trong dung dịch HNO3 loãng.
Sau khi phản ứng kết thúc, số thí nghiệm tạo thành chất khí là
 Xem đáp án
Xem đáp án
Đáp án A
a. Khí NH3
b. O2
c. CO2
d. H+ hết ko có khí thoát ra
e. NO
Câu 35:
Hòa tan hoàn toàn hai chất rắn X, Y (có số mol bằng nhau) vào nước thu được dung dịch Z. Tiến hành các thí nghiệm sau:
- Thí nghiệm 1: Cho dung dịch NaOH dư vào V lít Z, đun nóng thu được n1 mol khí.
- Thí nghiệm 2: Cho dung dịch H2SO4 dư vào V lít Z, thu được n2 mol khí không màu, hóa nâu ngoài không khí, là sản phẩm khử duy nhất.
- Thí nghiệm 3: Cho dung dịch Ba(OH)2 dư vào V lít Z, thu được n1 mol kết tủa.
Biết các phản ứng xảy ra hoàn toàn và n1 = 6n2. Hai chất X, Y lần lượt là
 Xem đáp án
Xem đáp án
Đáp án A
Thí nghiệm 1 và 2 thu được cùng 1 số mol nên loại D.
Thí nghiệm 2 có sinh ra khí NO nên loại B.
Vì n1 = 6n2 ⟶ Chọn A.
Câu 36:
Nung nóng hỗn hợp X gồm propen, axetilen và hiđro với xúc tác Ni trong bình kín (chỉ xảy ra phản ứng cộng H2), sau một thời gian thu được hỗn hợp khí Y có tỉ khối so với X là 1,25. Đốt cháy hết Y, thu được 0,435 mol CO2 và 0,525 mol H2O. Mặt khác, Y phản ứng tối đa với 0,21 mol brom trong dung dịch. Phần trăm khối lượng của propen trong X là
 Xem đáp án
Xem đáp án
Đáp án B
Câu 37:
Khí hỗn hợp X gồm Fe3O4, Fe2O3, CuO (trong đó nguyên tố oxi chiếm 27,03% theo khối lượng) bằng CO ở nhiệt độ cao, sau một thời gian thu được chất rắn Y và khí Z. Hoà tan Y trong dung dịch HNO3 dư thu được dung dịch T và khí NO (sản phẩm khử duy nhất). Cho thanh nhôm có khối lượng m gam vào dung dịch T thấy thoát ra 2,24 lít khí NO (chất khí duy nhất ở đktc) và khối lượng thanh nhôm thay đổi theo thời gian được biểu diễn bằng đồ thị dưới đây
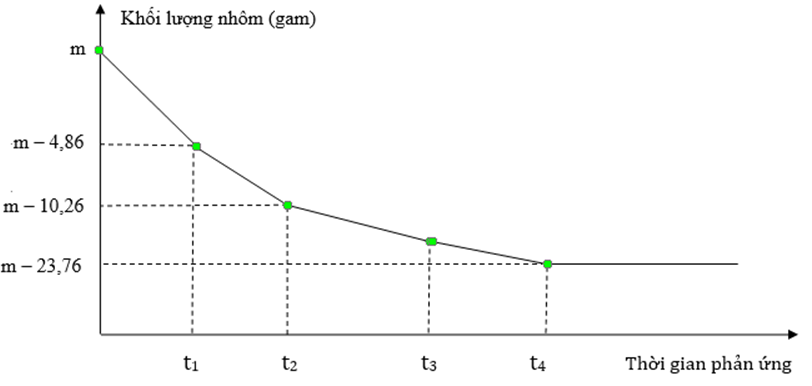
Biết các phản ứng xảy ra hoàn toàn và giả sử kim loại sinh ra không bám vào thanh nhôm. Số mol của Fe2O3 là
 Xem đáp án
Xem đáp án
Đáp án A
Đoạn 1: Al với HNO3 dư (tạo NO, NH4+)
Đoạn 2: Al với Fe3+
nAl đoạn 2 = (10,26 – 4,86)/27 = 0,2 —> nFe3+ = 0,6
Đoạn 3 và 4: Al với Cu2+ và Fe2+ (0,6 mol)
nAl hai đoạn này = (23,76 – 10,26)/27 = 0,5
Bảo toàn electron: 0,5.3 = 2nCu2+ + 2nFe2+ ⟶ nCu2+ = 0,15
X gồm Fe3O4 (u), Fe2O3 (v) và CuO (0,15)
mO = 16(4u + 3v + 0,15) = 27,03%(232u + 160v + 0,15.80)
Bảo toàn Fe ⟶ 3u + 2v = 0,6 ⟶ u = 0,1; v = 0,15
Câu 38:
Điện phân dung dịch chứa Cu(NO3)2, CuSO4 và NaCl với điện cực trơ, cường độ dòng điện không đổi 2A, hiệu suất 100%. Kết quả thí nghiệm được ghi trong bảng sau:
|
Thời gian điện phân (giây) |
t |
t + 2895 |
2t |
|
Tổng số mol khí ở 2 điện cực |
a |
a + 0,03 |
2,125a |
|
Số mol Cu ở catot |
b |
b + 0,02 |
b + 0,02 |
Giá trị của t là
 Xem đáp án
Xem đáp án
Đáp án B
Câu 39:
Cho sơ đồ phản ứng:
X (C5H8O2) + NaOH → X1 (muối) + X2
Y (C5H8O2) + NaOH → Y1 (muối) + Y2
Biết X1 và Y1 có cùng số nguyên tử cacbon; X1 có phản ứng với nước brom, còn Y1 thì không. Cho các phát biểu sau:
(a) Đốt cháy a mol X1 cần dùng 3a mol O2 ( hiệu suất phản ứng là 100%).
(b) Thực hiện phản ứng lên men giấm X2, thu được axit axetic.
(c) Y2 tác dụng với dung dịch AgNO3 trong NH3 đun nóng, thu được kết tủa trắng bạc.
(d) Cho C2H2 tác dụng với nước (có xúc tác), thu được X2.
(e) Y1 tác dụng với axit HCl, thu được axit axetic.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án B
a. X1: CH2=CH-COONa (2C3H3O2Na + 6O2 ⟶ 5CO2 + 3H2O + Na2CO3) ⟶ĐÚNG
b. X2: C2H5OH. (C2H5OH + O2 ⟶ CH3COOH + H2O) ⟶ ĐÚNG
c. Y2: CH3CHO ( có tráng bạc) ⟶ ĐÚNG
d. C2H2 + H2O à CH3CHO ⟶ SAI
E. Y1: C2H5COONa + HCl ⟶ C2H5COOH + NaCl ⟶ SAI
Câu 40:
Tiến hành các thí nghiệm sau:
- Bước 1: Cho vào ống nghiệm 2 – 3 ml dung dịch lòng trắng trứng 10%.
- Bước 2: Đun nóng ống nghiệm trên ngọn lửa đèn cồn cho đến sôi trong khoảng 1 phút.
Cho các nhận định sau:
(a) Ở bước 2 xảy ra hiện tượng đông tụ lòng trắng trứng, phần đông tụ có màu trắng.
(b) Ở bước 2, thay vì đun nóng, ta nhỏ vài giọt dung dịch HNO3 đậm đặc vào ống nghiệm thì lòng trắng trứng không bị đông tụ.
(c) Hiện tượng đông tụ cũng xảy ra khi thay dung dịch lòng trắng trứng bằng dung dịch thịt cua (giã cua sau khi đã bỏ mai, cho nước vừa đủ, vắt lấy nước lọc).
(d) Sau khi ăn hải sản không nên ăn liền trái cây như hồng, nho, lựu,. Trong các trái cây này thường có chứa nhiều axit tannic, khi gặp protein trong hải sản sẽ tạo nên hiện tượng đông đặc và sinh ra những chất khó tiêu hóa.
(e) Hải sản có vỏ không nên dùng chung với những trái cây chứa nhiều vitamin C. Bởi các loại hải sản này rất giàu asen, khi gặp vitamin C trong trái cây asen lập tức biến đổi và gây ra độc tố.
Số nhận định đúng là
 Xem đáp án
Xem đáp án
Đáp án A
a. Đúng
b. Lòng trắng trứng bị đông tụ bới HNO3 ⟶ Sai
c. Đúng
d. Đúng
e. Đúng