Ôn thi Tốt nghiệp THPT môn Hóa học (Đề 11)
-
189 lượt thi
-
40 câu hỏi
-
60 phút
Danh sách câu hỏi
Câu 1:
Hỗn hợp 0,78 mol Mg và x mol Zn vào dung dịch chứa 1,2 mol Cu2+ và 1,2 mol Ag+. Sau phản ứng hoàn toàn, lọc bỏ phần dung dịch thu được chất rắn gồm 2 kim loại. Giá trị của x có thể là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Câu 2:
Phát biểu nào sau đây đúng?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
A. Sai: CH3COOCH=CH2 + NaOH → CH3COONa + CH3CHO
Chỉ sản phẩm CH3CHO có tráng bạc và tạo ra 2Ag.
B. Sai: C5H10O2 có 4 đồng phân este có khả năng tham gia phản ứng tráng bạc.
HCOO−CH2−CH2−CH2−CH3.
HCOO−CH(CH3)−CH2−CH3.
HCOO−CH2−CH(CH3)2.
HCOO-C(CH3)3
C. Đúng:
CH3COOC6H4OH + 3KOH → CH3COOK + C6H4(OK)2 + 2H2O
D. Sai: HCOOCH3, CH3COOH, HOCH2CHO, có 2 trong 3 đồng phân này tráng gương.
Câu 3:
Hợp chất nào sau đây có khối lượng mol phân tử là số lẻ?
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Anilin có số N lẻ nên phân tử khối lẻ.
Câu 4:
Kali tác dụng với dung dịch chất nào sau đây không tạo thành kết tủa?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Kali tác dụng với dung dịch Ba(NO3)2 không tạo thành kết tủa:
2K + 2H2O → 2KOH + H2.
Các dung dịch còn lại đều tạo kết tủa, tương ứng là Mg(OH)2, Fe(OH)2 và Cu(OH)2.
Câu 5:
Quá trình nào sau đây không có sự trao đổi electron?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Quá trình dùng giấm ăn để khử mùi tanh của nhớt cá không có sự trao đổi electron, ở đây xảy ra phản ứng axit−bazơ giữa CH3COOH và một số amin gây ra mùi tanh của cá.
Câu 6:
Vật liệu polime nào sau đây trong thành phần không chứa nguyên tố nitơ?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Tơ lapsan được tổng hợp từ axit terephtalic và etylen glicol nên thành phần không có chứa nitơ.
Câu 7:
Cho các cặp oxi hóa – khử được sắp xếp theo chiều tăng dần tính oxi hóa ion kim loại như sau: Mg2+/Mg; Al3+/Al; Zn2+/Zn; Cu2+/Cu. Kim loại có tính khử mạnh nhất là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Kim loại có tính khử mạnh nhất trong dãy là Mg.
Câu 8:
Phát biểu nào sau đây không đúng?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Crom là kim loại cứng nhất, ứng dụng chủ yếu để làm thép và mạ vào một số đồ vật trong đời sống.
Câu 9:
Phát biểu nào sau đây không đúng?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Ở điều kiện thường glucozơ ở trạng thái rắn, dạng mạch vòng. Trong dung dịch hai dạng vòng chiếm chủ yếu và chuyển đổi qua lại thông qua dạng mạch hở.
Câu 10:
Este nào sau đây khi thủy phân trong môi trường kiềm không thu được muối và ancol?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Câu 11:
Phát biểu nào sau đây không đúng?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Kim loại Cs được dùng làm tế bào quang điện.
Câu 12:
Chất béo nào sau đây là chất lỏng ở điều kiện thường và có 98 nguyên tử hiđro trong phân tử?
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Chất béo thể lỏng ở điều kiện thường (không no) và có 98 nguyên tử hiđro trong phân tử là trilinolein (C17H31COO)3C3H5.
Câu 13:
Trường hợp nào sau đây có xảy ra quá trình ăn mòn điện hóa (kim loại sử dụng trong các thí nghiệm được coi là tinh khiết)?
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Để đoạn dây thép trong không khí ẩm có ăn mòn điện hóa do có cặp điện cực Fe−C tiếp xúc trực tiếp với nhau và môi trường điện li (không khí ẩm).
Câu 14:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Trong tự nhiên, canxi sunfat tồn tại dưới dạng ngậm nước (CaSO4.2H2O) được gọi là thạch cao sống.
Câu 15:
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Trộn bột kim loại nhôm với bột sắt oxit thu được hỗn hợp tecmit dùng để hàn đường ray tàu hoả.
Câu 16:
Để sơ cứu cho người bị bỏng phenol (C6H5OH) người ta có thể sử dụng dung dịch loãng nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Có thể sử dụng dung dịch loãng của nước vôi trong để rửa:
2C6H5OH + Ca(OH)2 → (C6H5O)2Ca + 2H2O.
Câu 17:
Thủy phân 10,36 gam etyl fomat trong dung dịch chứa 6,4 gam NaOH đun nóng. Sau khi phản ứng xảy ra hoàn toàn, cô cạn dung dịch thì thu được m gam chất rắn. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Câu 19:
Kim loại nào sau đây có thể tác dụng với nước ở điều kiện thường?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Kim loại Ba tác dụng với nước ở điều kiện thường:
Ba + 2H2O → Ba(OH)2 + H2.
Câu 20:
Amin nào sau đây không ở thể khí ở điều kiện thường?
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Isopropyl amin không ở thể khí ở điều kiện thường.
Câu 22:
Thành phần phần trăm về khối lượng của nguyên tố kim loại M trong hỗn hợp X gồm MCl2 và MSO4 là 21,10%. Thành phần phần trăm về khối lượng của nguyên tố lưu huỳnh trong X là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Câu 23:
Tiến hành thí nghiệm như hình vẽ:
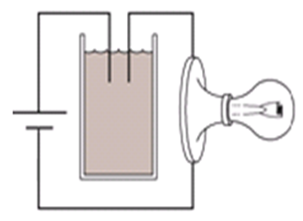
Ban đầu trong cốc chứa dung dịch Ca(OH)2. Sục rất từ từ CO2 vào cốc cho tới dư. Hỏi độ sáng của bóng đèn thay đổi như thế nào?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Câu 24:
Hoà tan hoàn toàn một lượng hỗn hợp gồm Al, MgCO3, Fe3O4 vào dung dịch H2SO4 loãng, thu được dung dịch X. Cho dung dịch Ba(OH)2 tới dư vào dung dịch X, sau khi các phản ứng xảy ra hoàn toàn thu được kết tủa Y. Nung Y trong không khí đến khối lượng không đổi, thu được hỗn hợp chất rắn Z gồm
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
X chứa MgSO4, Al2(SO4)3, FeSO4, Fe2(SO4)4, có thể có H2SO4 dư.
Y gồm Fe(OH)2, Fe(OH)3, Mg(OH)2, BaSO4
Nung Y trong không khí đến khối lượng không đổi, thu được hỗn hợp chất rắn Z gồm BaSO4, MgO, Fe2O3.
Câu 25:
Hợp chất hữu cơ X thủy phân trong cả môi trường axit và môi trường bazơ. X không thể là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Tinh bột thuỷ phân trong môi trường axit.
Câu 26:
Kim loại nào sau đây có nhiệt độ nóng chảy thấp nhất?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Hg có nhiệt độ nóng chảy thấp nhất.
Câu 27:
Cho 10,22 gam aminoaxit X có trong tự nhiên phản ứng vừa đủ với V mL dung dịch HCl 1,0M thì thu được 15,33 gam muối. Giá trị của V và amino axit X tương ứng là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Câu 28:
Thực hiện các thí nghiệm sau:
(1) Sục khí CO2 vào dung dịch Ca(OH)2 dư.
(2) Sục khí NH3 dư vào dung dịch AlCl3.
(3) Sục khí CO2 dư vào dung dịch NaAlO2.
(4) Cho dung dịch AgNO3 vào dung dịch FeCl3.
(5) Cho dung dịch HCl vào dung dịch K2CO3.
(6) Cho ure vào dung dịch Ca(OH)2.
Sau khi kết thúc thí nghiệm, số trường hợp thu được kết tủa là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
(1) CO2 + Ca(OH)2 → CaCO3↓ + H2O.
(2) 3NH3 + 3H2O + AlCl3 → Al(OH)3↓ + 3NH4Cl
(3) CO2 + 2H2O + NaAlO2 → Al(OH)3↓ + NaHCO3
(4) 3AgNO3 + FeCl3 → 3AgCl↓ + Fe(NO3)3
(5) 2HCl + K2CO3 → 2KCl + CO2 + H2O
(6) (NH2)2CO + Ca(OH)2 → CaCO3↓ + 2NH3
Vậy có 5 trường hợp thu được kết tủa sau phản ứng.
Câu 29:
Thực hiện các thí nghiệm sau:
(a) Điện phân MgCl2 nóng chảy.
(b) Cho dung dịch Fe(NO3)2 vào dung dịch AgNO3 dư.
(c) Nhiệt phân hoàn toàn CaCO3.
(d) Cho kim loại Na vào dung dịch CuSO4 dư.
(e) Dẫn khí H2 dư đi qua bột CuO nung nóng.
Sau khi các phản ứng kết thúc, số thí nghiệm thu được kim loại là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Câu 30:
Một mẫu cồn X (thành phần chính là C2H5OH) có lẫn metanol (CH3OH). Đốt cháy 15 gam cồn X tỏa ra nhiệt lượng 437,85 kJ. Biết khi đốt cháy 1 mol metanol tỏa ra nhiệt lượng là 716 kJ, đốt cháy 1 mol etanol tỏa ra nhiệt lượng là 1370 kJ. Phần trăm tạp chất metanol trong X là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Câu 31:
Hợp chất hữu cơ X có công thức phân tử C7H16O6N2. Từ X thực hiện các chuyển hóa sau (theo đúng tỉ lệ mol)
(1) X + 3NaOH → 2Y + Z + T. (2) Y + 2HCl → M + NaCl.
(3) Z + HCl → Q + NaCl. (4) Q + T ⇋ CH3COOCH3 + H2O.
Phát biểu nào sau đây không đúng?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
(3)(4) Þ Q là CH3COOH, Z là CH3COONa, T là CH3OH.
(1) Þ Y chứa 2C và 2Na.
(2) Þ Y chứa 1N (amin).
Vậy Y là H2N-CH2-COONa; M là ClH3N-CH2-COOH.
X là CH3COONH3-CH2-COO-NH3-CH2-COO-CH3.
A. Đúng, M, T, Q đều có H linh động nên phản ứng được với Na giải phóng khí H2.
B. Sai, Y chỉ có tính bazơ, M chỉ có tính axit.
C. Đúng.
D. Đúng, P là CH4.
Câu 32:
Cho m gam hỗn hợp X gồm ZnO, CuO, ZnS và Cu2S (oxi chiếm 20% khối lượng) tan vừa đủ trong dung dịch H2SO4 và NaNO3, thu được dung dịch Y chứa 4m gam muối trung hòa và 0,840 lít (ở đktc) hỗn hợp khí gồm NO2, SO2 (không còn sản phẩm khử nào khác). Cho Y tác dụng vừa đủ với dung dịch Ba(NO3)2 được dung dịch Z và 11,65 gam kết tủa. Cô cạn Z được chất rắn T, nung T đến khối lượng không đổi thu được 3,36 lít (ở đktc) hỗn hợp khí có tỉ khối so với H2 bằng 19,5. Giá trị gần nhất của m là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Câu 33:
Cho 31,64 gam hỗn hợp X gồm Mg, Fe, Fe3O4, Fe(NO3)2 vào dung dịch chứa KNO3 (27,27 gam) và H2SO4 (86,24 gam). Sau khi phản ứng xảy ra hoàn toàn, thu được dung dịch Y chỉ chứa 121,83 gam các muối sunfat trung hòa và 5,152 lít hỗn hợp khí Z (ở đktc) gồm NO, N2O và H2 (tỉ lệ mol tương ứng 12 : 10 : 1). Cho dung dịch Y phản ứng vừa đủ với dung dịch NaOH thì thu được kết tủa Q. Nung Q trong không khí đến khối lượng không đổi thu được 39,2 gam chất rắn. Phần trăm khối lượng của Mg trong X gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Câu 34:
Cho 6,4 gam hỗn hợp X gồm hai hợp chất hữu cơ mạch hở có công thức phân tử C5H14O4N2 và C9H24O8N4 phản ứng vừa đủ với 160 mL dung dịch NaOH 0,5M. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch Y và 0,896 lít hỗn hợp khí Z (ở đktc) gồm hai amin đồng đẳng kế tiếp có tỉ khối hơi so với hiđro là 18,125. Cô cạn dung dịch Y thu được chất rắn G chỉ chứa 3 muối hữu cơ có cùng số nguyên tử cacbon. Phần trăm khối lượng của muối có khối lượng mol lớn nhất trong G là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Z gồm CH3NH2 (0,025 mol) và C2H5NH2 (0,015 mol)
Đặt a, b là số mol C5H14O4N2 và C9H24O8N4
Þ mX = 166a + 316b = 6,4.
nNaOH = 2a + 4b = 0,08
Þ a = 0,01; b = 0,015.
Sản phẩm tạo 3 muối cùng C nên X gồm:
TH1:
C2H5NH3-OOC-COO-NH3CH3: 0,01 mol
CH3COO-NH3-CH2-COO-NH3-CH2-COO-NH3-CH2-COO-NH3-CH3: 0,015 mol
Không thỏa mãn số mol các amin, loại.
TH2:
CH3COONH3-CH2-COONH3CH3: 0,01 mol
CH3NH3-OOC-COO-NH3-CH2-COO-NH3-CH2-COO-NH3-C2H5: 0,015 mol
Các muối gồm (COONa)2 (0,015 mol), CH3COONa (0,01 mol) và GlyNa (0,04 mol).
Þ %(COONa)2 = 29,96%.
Câu 35:
Đốt cháy hoàn toàn 4,96 gam photpho trong khí O2 dư, toàn bộ sản phẩm sinh ra cho vào 400 ml dung dịch hỗn hợp NaOH 0,4M và KOH 0,6M, kết thúc phản ứng thu được dung dịch X. Biết các phản ứng xảy ra hoàn toàn. Tổng khối lượng muối có trong dung dịch X là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Câu 36:
Hỗn hợp X gồm các hiđrocacbon có công thức dạng C5Hy và H2. Đun nóng 0,5875 mol X với Ni, sau một thời gian phản ứng thu được hỗn hợp M chỉ chứa các hiđrocacbon. Đốt cháy hoàn toàn M thu được 23,175 gam H2O. Biết tỉ khối của M so với hiđro bằng 35,15. Mặt khác, 14,06 gam X tác dụng tối đa với m gam brom. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Câu 37:
Để tráng 50 chiếc gương soi có diện tích bề mặt 0,4 m² với độ dày 0,1 μm người ta cho m gam glucozơ thực hiện phản ứng với lượng dư dung dịch bạc nitrat trong amoniac. Biết khối lượng riêng của bạc là 10,49 g/cm³ và hiệu suất của quá trình là 65%. Giá trị gần nhất của m là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Câu 38:
Cho các phát biểu sau:
(1) Anilin và phenol đều ít tan trong nước, dung dịch của chúng đều không làm đổi màu quì tím.
(2) Khi tách hiđro các ankan (trừ metan) sẽ thu được anken có mạch cacbon tương ứng.
(3) Tripeptit Gly-Ala-Glu phản ứng hoàn toàn với NaOH theo tỉ lệ mol 1 : 3.
(4) Sản phẩm trùng hợp metyl metacrylat được dùng để làm thủy tinh hữu cơ.
(5) Chiếu sáng hỗn hợp neopentan (2,2-đimetylpropan) và clo sẽ thu được tối đa 4 dẫn xuất monoclo.
(6) Đề hiđrat hóa ancol secbutylic (butan−2−ol) sẽ thu được 2 anken đồng phân cấu tạo của nhau.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Các phát biểu (1), (2), (4), (6) đúng.
(3) Sai: Gly-Ala-Glu + 4NaOH → GlyNa + AlaNa + GluNa2 + 2H2O.
(5) Sai, chỉ thu được 1 dẫn xuất monoclo là (CH3)3C-CH2Cl.
(6) Đúng, thu được CH2=CH-CH2-CH3 và CH3-CH=CH-CH3.
Câu 39:
Tiến hành thí nghiệm sau:
Bước 1: Rót vào 2 ống nghiệm 1, 2 mỗi ống khoảng 3 mL dung dịch H2SO4 loãng rồi cho vào mỗi ống một mẩu kim loại kẽm nguyên chất.
Bước 2: Nhỏ thêm 2 - 3 giọt dung dịch CuSO4 vào ống 2.
Quan sát hiện tượng và so sánh lượng bọt khí thoát ra ở 2 ống nghiệm. Cho các phát biểu sau:
(1) Tốc độ khí thoát ra ở ống nghiệm 2 nhanh hơn so với ống nghiệm 1.
(2) Ở ống nghiệm 1 chỉ xảy ra ăn mòn hoá học còn ở ống nghiệm 2 chỉ xảy ra ăn mòn điện hoá.
(3) Lượng bọt khí thoát ra ở hai ống trong cùng một thời điểm là như nhau.
(4) Ở cả hai ống nghiệm, kim loại Zn đều bị ăn mòn, bị oxi hóa thành ion Zn2+.
(5) Ở ống nghiệm 2, hiện tượng không thay đổi khi thay dung dịch CuSO4 bằng dung dịch MgSO4.
(6) Nếu ở bước 2 thay dung dịch CuSO4 bằng dung dịch ZnSO4 khí thoát ra sẽ nhanh hơn.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
(1) Đúng, ống 2 có ăn mòn điện hóa nên xảy ra nhanh hơn ống 1 chỉ có ăn mòn hóa học.
(2) Sai, ống 1 chỉ có ăn mòn hóa học, ống 2 có cả ăn mòn hóa học và ăn mòn điện hóa.
(3) Sai, ống 2 thoát khí nhanh hơn nên trong cùng thời điểm ống 2 thoát khí nhiều hơn.
(4) Đúng, ở cả hai ống nghiệm, kim loại Zn đều bị ăn mòn, bị oxi hóa thành ion Zn2+.
(5) Sai, thay CuSO4 bằng MgSO4 thì không có ăn mòn điện hóa (do Zn không khử được Mg2+ nên không có đủ 2 điện cực).
(6) Sai (như trên).
Câu 40:
Hỗn hợp A gồm ancol đơn chức X, axit 2 chức mạch hở Y và Z là sản phẩm este hóa của X và Y. Cho 0,45 mol A (trong đó số mol của X lớn hơn số mol Y) phản ứng với dung dịch NaHCO3 dư thì thu được 8,96 lít khí CO2 (ở đktc). Mặt khác, cũng 0,45 mol A phản ứng vừa đủ với 250 mL dung dịch NaOH 2,0M, cô cạn dung dịch sau phản ứng thu được 37,0 gam muối. Đốt cháy hoàn toàn 0,45 mol A thì thu được 36,96 lít khí CO2 (ở đktc) và 23,4 gam nước. Phần trăm khối lượng của Y trong A là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
