(2023) Đề thi thử Hóa Học THPT soạn theo ma trận đề minh họa BGD ( Đề 5) có đáp án
(2023) Đề thi thử Hóa Học THPT soạn theo ma trận đề minh họa BGD ( Đề 5) có đáp án
-
1053 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 7:
Kim loại được dùng làm chất trao đổi nhiệt trong lò phản ứng hạt nhân là
 Xem đáp án
Xem đáp án
Chọn đáp án A
Câu 8:
Khi đun nóng axit axetic với ancol etylic có mặt H2SO4 đặc, thu được este có công thức là
 Xem đáp án
Xem đáp án
Chọn đáp án B
Câu 9:
Trong các chất: NaOH, Mg(OH)2, Ba(OH)2, KOH, chất có tính bazơ yếu nhất là
 Xem đáp án
Xem đáp án
Chọn đáp án C
Câu 13:
X là ancol đầu tiên trong dãy đồng đẳng ancol no, đơn chức, có khả năng thẩm thấu nhanh qua đường tiêu hóa. Nếu uống rượu có lẫn X sẽ dẫn tới hiện tượng thở nhanh, rối loạn thị giác (có thể gây mù lòa), co giật, có thể dẫn đến tử vong. Tên gọi của X là
 Xem đáp án
Xem đáp án
Chọn đáp án D
Câu 16:
Cho các phương pháp sau:
(a) Gắn kim loại kẽm vào kim loại sắt. (b) Gắn kim loại đồng vào kim loại sắt.
(c) Phủ một lớp sơn lên bề mặt sắt. (d) Tráng thiếc lên bề mặt sắt.
Số phương pháp điện hóa được sử dụng để bảo vệ kim loại sắt không bị ăn mòn là
 Xem đáp án
Xem đáp án
Chọn đáp án C
Câu 17:
Cho amin X đơn chức tác dụng với dung dịch HCl tạo thành muối có dạng RNH3Cl. X là amin bậc mấy?
 Xem đáp án
Xem đáp án
Chọn đáp án A
Câu 19:
Cho một mẩu nhỏ kim loại X vào cốc thủy tinh chứa dung dịch CuSO4, quan sát thấy có hiện tượng sủi bọt khí không màu và xuất hiện kết tủa màu xanh. X là
 Xem đáp án
Xem đáp án
Chọn đáp án C
Câu 21:
Hòa tan hoàn toàn m gam bột Al trong dung dịch KOH loãng, dư thu được 2,688 lít khí H2 (đktc). Giá trị của m là
Tính chất nào sau đây không đúng với crom?
 Xem đáp án
Xem đáp án
Chọn đáp án B
Câu 24:
Khối lượng phân tử trung bình của xenlulozơ trong sợi bông là 4860000 đvC. Số gốc glucozơ có trong xenlulozơ nêu trên là
 Xem đáp án
Xem đáp án
Chọn đáp án B
Câu 25:
Đốt cháy hoàn toàn m hỗn hợp X gồm 2 amino axit no X (trong phân tử có một nhóm NH2 và một nhóm COOH), thu được N2, 3,08 gam CO2 và 1,53 gam H2O. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn đáp án C
Câu 26:
X là chất rắn, dạng sợi, màu trắng, chiếm 98% thành phần bông nõn. Đun nóng X trong dung dịch H2SO4 70% đến phản ứng hoàn toàn, thu được chất Y. Phát biểu nào sau đây đúng?
 Xem đáp án
Xem đáp án
Chọn đáp án B
Câu 27:
Thổi luồng khí CO đến dư qua ống sứ chứa 10,88 gam hỗn hợp gồm Fe3O4 và MgO nung nóng, đến khi các phản ứng xảy ra hoàn toàn thu được 8,32 gam hỗn hợp rắn X. Cho toàn bộ X vào dung dịch HCl loãng, dư thu được dung dịch chứa m gam muối. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn A.
Chỉ có Fe3O4 bị CO khử nên: nO bị lấy đi = (10,88 – 8,32)/16 = 0,16 mol
Þ = 0,04 mol Þ nFe = 0,12 mol
mhỗn hợp = 10,88g Þ nMgO = 0,04 mol
Muối gồm FeCl2 (0,12) và MgCl2 (0,04) Þ mmuối = 19,04 gam
Câu 28:
Tiến hành thí nghiệm theo các bước sau:
Bước 1: Nhỏ vài giọt dung dịch iot vào ống nghiệm chứa 2 ml dung dịch hồ tinh bột.
Bước 2: Đun nóng ống nghiệm trên ngọn lửa đèn cồn (không để sôi) khoảng 1-2 phút.
Bước 3: Ngâm ống nghiệm trong cốc nước nguội khoảng 5-6 phút.
Phát biểu nào sau đây đúng?
 Xem đáp án
Xem đáp án
Chọn đáp án B
Câu 29:
Cho sơ đồ phản ứng: X ® Fe ® Y ® Fe(OH)3 ® X (mỗi mũi tên là một phản ứng). Biết X, Y là các hợp chất khác nhau của sắt. Các chất X, Y lần lượt là
 Xem đáp án
Xem đáp án
Chọn đáp án C
Câu 30:
X là este đơn chức, chứa vòng benzen. Đốt cháy hoàn toàn 18,0 gam X, thu được 47,52 gam CO2 và 10,8 gam H2O. Nếu đun nóng X với dung dịch NaOH dư, thu được chất hữu cơ Y thuộc dãy đồng đẳng của metanol. Số đồng phân cấu tạo của X là
 Xem đáp án
Xem đáp án
Chọn D.
Đốt hỗn hợp X ta được: nO (trongX) = 0,24 mol
Ta có: C : H : O = : nO = 9 : 10 : 2
Vậy CTPT của X là C9H10O2
Cho X với dung dịch NaOH dư, thu được chất hữu cơ Y thuộc dãy đồng đẳng của ancol metylic
X là và C6H5CH2COOCH3 ,CH3C6H4COOCH3 (o,m, p) C6H5COOC2H5.
Câu 31:
Cho các phát biểu sau:
(a) Trùng hợp vinyl xianua thu được tơ nitron.
(b) Cho xenlulozơ vào ống nghiệm chứa nước Svayde, khuấy đều thấy xenlulozơ tan ra.
(c) Khi nấu canh cua, hiện tượng riêu cua nổi lên là do sự đông đặc protein.
(d) Khả năng phản ứng thế hiđro trong vòng benzen của anilin cao hơn benzen.
(e) Các polime bán tổng hợp đều có nguồn gốc từ các polime thiên nhiên.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Chọn B.
(c) Sai, Khi nấu canh cua, hiện tượng riêu cua nổi lên là do sự đông tụ protein.
Câu 32:
Cho các phát biểu sau:
(a) Nhôm và sắt đều bị thụ động hóa khi tiếp xúc với HNO3 đặc, nguội.
(b) Sử dụng nước cứng gây tiêu tốn nhiên liệu và có thể tắc đường ống dẫn nước nóng.
(c) Thép cacbon để trong không khí ẩm có thể xảy ra ăn mòn điện hóa.
(d) Hỗn hợp Cu và Fe3O4 (tỉ lệ mol 1 : 1) tan hết trong dung dịch HCl dư.
(e) Kim loại Mg, Al, K, Fe chỉ được điều chế bằng phương pháp điện phân nóng chảy.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Chọn C.
(e) Sai, Kim loại Fe điều chế chủ yếu bằng phương pháp nhiệt luyện.
Câu 33:
Cho 87,8 gam một triglixerit X tác dụng với dung dịch NaOH vừa đủ, thu được glixerol và hỗn hợp muối Y. Cho Y tác dụng với a mol H2 (Ni, t°), thu được 91,0 gam hỗn hợp muối Z. Đốt cháy hoàn toàn Z cần vừa đủ 7,6 mol O2, thu được 5,25 mol CO2. Giá trị của a là
 Xem đáp án
Xem đáp án
Chọn C.
Quy đổi Z thành HCOONa (x mol), CH2 (y mol) và H2 (z mol)
mZ = 68x + 14y + 2z = 91
= 0,5x + 1,5y + 0,5z = 7,6
= x + y – 0,5x = 5,25
Þ x = 0,3; y = 5,1; z = -0,4
Ta có: = x/3 = 0,1 mol và nNaOH = 0,3 mol
Bảo toàn khối lượng Þ mY = 90,6g Þ = (mZ – mY)/2 = 0,2 mol
Câu 34:
Tinh thể CuSO4.5H2O thường dùng làm chất diệt nấm, sát khuẩn… Khi nung nóng khối lượng CuSO4.5H2O giảm dần. Đồ thị sau đây biểu diễn độ giảm khối lượng của CuSO4.5H2O khi tăng dần nhiệt độ:
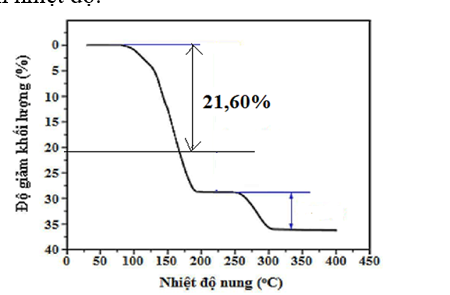
Thành phần chất rắn sau khi nhiệt độ đạt đến 200°C là
 Xem đáp án
Xem đáp án
Chọn B.
Khi nung tới 200°C: CuSO4.5H2O ® CuSO4.(5-x)H2O + xH2O
m giảm = 18x = 21,6%.250 Þ x = 3
Chất rắn là CuSO4.2H2O
Câu 35:
Một chiếc xuồng máy dùng động cơ đốt trong sử dụng xăng, trung bình một giờ hoạt động thì động cơ cần một nhiệt lượng là 9000 kJ. Giả thiết xăng chỉ gồm heptan và octan có tỉ lệ mol tương ứng là 1 : 9, khi được đốt cháy hoàn toàn 1 mol heptan tỏa ra lượng nhiệt là 3744,4 kJ và 1 mol octan tỏa ra lượng nhiệt là 5928,7 kJ. Nếu chiếc xuồng đó đã sử dụng hết 5 lít xăng ở trên thì thời gian xuồng hoạt động được là t giờ, biết hiệu suất sử dụng nhiên liệu của động cơ là 30%, khối lượng riêng của xăng là 0,72 g/ml. Giá trị của t gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
Chọn A.
Gọi C7H16 (x mol) và C8H18 (9x mol)
Ta có: m = 100x + 114.94x = 5000.0,72 Þ x = 3,197 mol
Nhiệt lượng tạo công cơ học: (3,197.3744,4 + 3,197.9.5928,7).0,3 = 54770 kJ
Số giờ hoạt động là: 54770/9000 = 6,08h
Câu 36:
Hòa tan hoàn toàn m gam hỗn hợp X gồm MgCO3, Fe2O3, FeS và FeS2 trong dung dịch H2SO4 (đặc, nóng, dư) thu được khí SO2 và dung dịch Y chứa (m + 33) gam muối. Mặt khác, hòa tan hoàn toàn m gam X trên vào dung dịch HNO3 (đặc, nóng, dư) thu được 17,92 lít (đktc) hỗn hợp khí Z (gồm NO2 và CO2) có tổng khối lượng là 36,7 gam và dung dịch T. Cô cạn dung dịch T thu được 70,22 gam hỗn hợp muối khan. Phần trăm khối lượng của Fe2O3 trong X có giá trị gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
Chọn A.
Z gồm NO2 (0,75 mol) và CO2 (0,05 mol)
X gồm MgCO3 (0,05 mol), Fe2O3 (a mol), FeS (b mol) và FeS2 (c mol)
m = 0,05.84 + 160a + 88b + 120c (1)
Bảo toàn e: 9b + 15c = 0,75 (2)
mmuối sunfat = 0,05.120 + 400(2a + b + c)/2 = m + 33 (3)
T chứa Mg2+ (0,05), Fe3+ (2a + b + c), SO42- (b + 2c) và NO3-: 0,1 + 6a + 3b + 3c – 2b – 4c (BTĐT)
0,05.24 + 56(2a + b + c) + 96(b + 2c) + 62(0,1 + 6a + 3b + 3c – 2b – 4c) = 70,22 (4)
Từ (1), (2), (3), (4) Þ a = 0,1; b = 0,05; c = 0,02; m = 27
Vậy = 59,26%.
Câu 37:
Cho hỗn hợp bột gồm BaO, NaHCO3 và X (tỉ lệ mol tương ứng 2 : 1 : 1) vào nước dư, khuấy đều, đun nhẹ để đuổi hết các khí. Dung dịch sau phản ứng chỉ chứa một chất tan duy nhất có số mol bằng số mol chất X ban đầu. Trong các chất sau: NH4HCO3, Na2SO4, (NH4)2SO4, (NH4)2CO3 có mấy chất thỏa mãn vai trò của X?
 Xem đáp án
Xem đáp án
Chọn D.
BaO + H2O ® Ba(OH)2
Ba(OH)2 + NaHCO3 ® BaCO3 + NaOH + H2O
Sau 2 phản ứng trên dung dịch còn lại Ba(OH)2 (1), NaOH (1) và X (1)
Dung dịch sau các phản ứng gọi là Y.
• Nếu X là NH4HCO3: Ba(OH)2 + NH4HCO3 ® BaCO3 + NH3 + 2H2O
Þ Y chứa NaOH (1): Thỏa mãn
• Nếu X là Na2SO4: Ba(OH)2 + Na2SO4 ® BaSO4 + 2NaOH
Þ Y chứa NaOH (3): Không thỏa mãn
• Nếu X là (NH4)2SO4: Ba(OH)2 + (NH4)2SO4 ® BaSO4 + 2NH3 + 2H2O
Þ Y chứa NaOH (1): Thỏa mãn
• Nếu X là (NH4)2CO3: Ba(OH)2 + (NH4)2CO3 ® BaCO3 + 2NH3 + 2H2O
Þ Y chứa NaOH (1): Thỏa mãn
Vậy có 3 chất X trong dãy thỏa mãn.
Câu 38:
Đốt cháy hoàn toàn 0,2 mol hỗn hợp M gồm ba chất hữu cơ mạch hở X, Y, Z (chỉ chứa nhóm chức este, MX < MY < MZ) cần dùng 28,224 lít O2 (đktc), thu được 58,08 gam CO2 và 14,4 gam H2O. Mặt khác hiđro hóa hoàn toàn 0,2 mol M bằng lượng H2 vừa đủ (xúc tác Ni, t°), thu được hỗn hợp N gồm hai hợp chất hữu cơ. Đun nóng toàn bộ N với dung dịch NaOH vừa đủ, thu được hỗn hợp P gồm 3 muối của 3 axit cacboxylic đơn chức và hỗn hợp Q gồm hai ancol no hơn kém nhau một nguyên tử cacbon. Tỉ khối hơi của Q so với H2 bằng 35,5. Phần trăm khối lượng của Y trong hỗn hợp M là
 Xem đáp án
Xem đáp án
Chọn D.
Bảo toàn khối lượng Þ mM = 32,16g
Bảo toàn O Þ nO(N) = nO(M) = 0,92 mol Þ nNaOH = 0,46 mol
Các muối cacboxylat đơn chức nên nQ = nN = nM = 0,2 mol
Số O trung bình của Q = 0,46/0,2 = 2,3
Q dạng CnH2n+2O2,3 Þ MQ = 14n + 38,8 = 35,5.2 Þ n = 2,3
Q gồm C2H4(OH)2 (0,14) và C3H5(OH)3 (0,06)
N gồm 2 este với số C là x, y tương ứng với 2 ancol kể trên.
nCO2 = 0,14x + 0,06y = 1,32 Þ 7x + 3y = 66
Với x ≥ 4; y ≥ 6 Þ x = 6, y = 8 là nghiệm duy nhất
N gồm C6H10O4 (0,14) và C8H12O6 (0,06) Þ mN = 32,68g
= (mN – mM)/2 = 0,26 mol. Từ N tạo 3 muối nên có 2 trường hợp:
TH1: N gồm:
(CH3COO)2C2H4: 0,14 mol; (HCOO)2(C2H5COO)C3H5: 0,06 mol
M gồm:
X là (CH3COO)2C2H4: 0,14
Z là (HCOO)2(C2H3COO)C3H5: u
Y là (HCOO)2(C2HCOO)C3H5: v
® u + v = 0,06 và = u + 2v = 0,26 (Vô nghiệm)
TH2: N gồm:
(HCOO)(C2H5COO)C2H4: 0,14 mol; (HCOO)(CH3COO)2C3H5: 0,06 mol
M gồm:
Y là (HCOO)(C2H3COO)C2H4: u
X là (HCOO)(C2HCOO)C2H4: v
Z là (HCOO)(CH3COO)2C3H5: 0,06
u + v = 0,14 và = u + 2v = 0,26 Þ u = 0,02; v = 0,12
Þ %Y = 0,02.144/32,16 = 8,96%.
Câu 39:
Trộn 13,05 gam hỗn hợp gồm CuSO4 và NaCl với dung dịch chứa p mol HCl, thu được dung dịch Y. Tiến hành điện phân dung dịch Y với điện cực trơ, màng ngăn xốp, cường độ dòng điện 0,5A, hiệu suất điện phân là 100%. Lượng khí sinh ra từ bình điện phân và lượng kim loại Cu sinh ra ở catot theo thời gian điện phân được cho ở bảng sau:
|
Thời gian điện phân (giây) |
t |
t + 11580 |
3,8t |
|
Lượng khí sinh ra từ bình điện phân (mol) |
a |
a + 0,04 |
5,4a |
|
Lượng kim loại Cu sinh ra ở catot (mol) |
0,025 |
0,045 |
0,045 |
Giá trị của p là
 Xem đáp án
Xem đáp án
Chọn D.
Trong khoảng thời gian 11580s Þ ne = 0,06 mol
Khi đó tại catot có Cu (0,045 – 0,025 = 0,02 mol), H2 (0,01 mol)
còn tại anot có Cl2 (x mol), O2 (y mol) Þ
Þ tại thời điểm t chỉ có Cl2 (a mol) với a = 0,025, ne = 0,05 mol
Tại thời điểm 3,8t: ne = 0,19 mol
Khi đó tại catot có Cu (0,045 mol), H2 (0,05 mol) còn anot Cl2 (u mol), O2 (v mol)
Þ u + v = 5,4.0,025 – 0,05 và 2u + 4v = 0,19 Þ u = 0,075 và v = 0,01
mNaCl = 13,05 – 0,045.160 = 5,85g Þ nNaCl = 0,1 mol
BT Cl: 0,1 + p = 2u = 0,15 Þ p = 0,05 mol
Câu 40:
Hợp chất hữu cơ X (C4H6O4); Y(C8H8O4) đều mạch hở và chỉ chứa một loại nhóm chức. Thực hiện phản ứng hóa học sau:
(1) X + NaOH X1 + X2.
(2) Y + NaOH Y1 + Y2 + Y3.
Biết rằng khi đốt cháy hoàn toàn X1 hoặc Y1 ta chỉ thu được Na2CO3 và CO2; Y2 có phản ứng tráng bạc.
Cho các nhận định sau:
(a) Chất Y3 dùng để pha chế xăng sinh học E5.
(b) Chất X2 dùng để điều chế axit axetic trong công nghiệp.
(c) Chất X2 và Y3 thuộc cùng dãy đồng đẳng.
(d) Các chất Y2, Y3 đều là các hợp chất no, đơn chức, mạch hở.
(e) Chất X2 có nhiệt độ sôi cao hơn so Y2.
Số nhận định đúng là
 Xem đáp án
Xem đáp án
Chọn C.
Các chất X: CH3-OOC-COO-CH3 và Y: C2H5-OOC-CºC-COO-CH=CH2
X1: (COONa)2 ; X2: CH3OH
Y1: C2(COONa)2 ; Y2: CH3CHO ; Y3: C2H5OH
(a) Đúng.
(b) Đúng.
(c) Đúng.
(d) Đúng.
(e) Đúng.
