(2024) Đề minh họa tham khảo BGD môn Hóa có đáp án (Đề 2)
-
108 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 6:
Cho các chất: Al, Fe3O4, CaCO3 và Al(OH)3. Số chất trong dãy tác dụng được với dung dịch HCl là
 Xem đáp án
Xem đáp án
Chọn đáp án B.
Câu 7:
Thủy phân chất béo trong môi trường kiềm thu được muối của axit béo và
 Xem đáp án
Xem đáp án
Chọn đáp án A.
Câu 17:
Nung 21,4 gam Fe(OH)3 ở nhiệt độ cao đến khối lượng không đổi, thu được m gam chất rắn. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn đáp án A.
Câu 18:
Lên men 90 gam glucozơ để điều chế ancol etylic, hiệu suất phản ứng 100%, thu được V lít khí CO2 (đktc). Giá trị của V là
 Xem đáp án
Xem đáp án
Chọn đáp án C.
Câu 19:
Cho amin (hai chức, mạch hở) tác dụng vừa đủ với 400 ml dung dịch HCl 0,1M, sau phản ứng thu được 2,66 gam muối. Công thức của amin là
 Xem đáp án
Xem đáp án
Chọn đáp án C.
Câu 22:
Chất nào sau đây phản ứng với dung dịch NaOH, đun nóng tạo thành HCOONa và C2H5OH?
 Xem đáp án
Xem đáp án
Chọn đáp án C.
Câu 24:
Cho dãy các chất: Gly-Gly, H2NCH2COOH, CH3COOCH3, tinh bột. Số chất tác dụng được với dung dịch NaOH, đun nóng là
 Xem đáp án
Xem đáp án
Chọn đáp án A.
Câu 25:
Hỗn hợp gồm a mol Cu và b mol Fe2O3 tan hết được trong dung dịch HCl. Tỉ lệ (a : b) nào sau đây là không hợp lí?
 Xem đáp án
Xem đáp án
Chọn đáp án C.
Câu 26:
Chất hữu cơ X có công thức C3H9NO2. Cho X phản ứng với dung dịch NaOH đun nóng, thu được muối Y và khí Z làm xanh giấy quỳ tím ẩm. Nung Y với NaOH rắn và CaO, thu được khí metan. Công thức của X là
 Xem đáp án
Xem đáp án
Chọn đáp án A.
Câu 27:
Cho 15,2 gam hỗn hợp bột gồm Mg và Cu có tỉ lệ mol tương ứng là 1 : 2 vào dung dịch chứa 0,2 mol Fe2(SO4)3. Sau khi các phản ứng xảy ra hoàn toàn, thu được m gam kim loại. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn đáp án B.
Câu 28:
Kali đicromat là chất rắn màu da cam, tan tốt trong nước và có tính oxi hóa mạnh. Công thức của kali đicromat là
 Xem đáp án
Xem đáp án
Chọn đáp án C.
Câu 29:
Axit fomic có trong nọc kiến. Khi bị kiến cắn, chọn chất nào sau đây bôi vào vết thương để giảm sưng tấy?
 Xem đáp án
Xem đáp án
Chọn đáp án A.
Câu 30:
Đốt cháy một lượng bột sắt trong khí clo, thu được hỗn hợp chất rắn X. Hòa tan X vào lượng nước dư, sau phản ứng hoàn toàn, thu được dung dịch Y và thấy còn lại một lượng chất rắn không tan. Dung dịch Y chứa chất tan nào sau đây?
 Xem đáp án
Xem đáp án
Chọn đáp án B.
Câu 31:
Cho các sơ đồ phản ứng sau (theo đúng tỉ lệ mol):
(1) X + Y Na2CO3 + H2O.
(2) X + Ba(OH)2 BaCO3 + Y + H2O.
(3) Z + Y NaAlO2 + 2H2O.
Các chất X, Z thỏa mãn sơ đồ trên lần lượt là
 Xem đáp án
Xem đáp án
(1) NaHCO3 + NaOH Na2CO3 + H2O
(2) NaHCO3 + Ba(OH)2 BaCO3 + NaOH + H2O
(3) Al(OH)3 + NaOH NaAlO2 + 2H2O
Câu 32:
Thủy phân hoàn toàn 1 mol chất E có công thức C9H8O4 (có chứa vòng benzen) trong dung dịch NaOH dư, thu được 2 mol chất X, 1 mol chất Y và 1 mol H2O. Chất Y tác dụng với dung dịch HCl loãng thu được chất hữu cơ Z. Cho các nhận định sau:
(a) Chất Z tác dụng với KOH theo tỉ lệ mol 1 : 2.
(b) Chất X có phản ứng tráng bạc.
(c) Phân tử chất Y có 3 nguyên tử oxi.
(d) Chất E tác dụng với NaOH theo tỉ lệ mol 1 : 4.
(e) Chất E có 3 công thức cấu tạo thỏa mãn.
Số nhận định đúng là
 Xem đáp án
Xem đáp án
E: C9H8O4 Số pi + vòng = 6 E có 1 vòng benzen và 2 pi C=C trong 2 gốc -COO-
Thủy phân 1 mol E thu được 1 mol H2O E có dạng este của phenol
E: HCOO-C6H4-CH2-OOOCH
HCOO-C6H4-CH2-OOOCH (E) + 3NaOH 2HCOONa (X) + NaO-C6H4-CH2OH (Y)
NaO-C6H4-CH2OH (Y) + HCl HO-C6H4-CH2OH (Z) + NaCl
(a) Sai, Z tác dụng với KOH theo tỉ lệ mol 1 : 1
(b) Đúng, vì X có dạng HCOOR
(c) Sai, Y có chứa 2 nguyên tử oxi
(d) Sai, E tác dụng với NaOH theo tỉ lệ mol 1 : 3
(e) Đúng, E có 3 vị trí đồng phân o, m, p
Câu 33:
Tiến hành phản ứng nhiệt nhôm hỗn hợp rắn X gồm Al, FeO, Fe2O3 và Fe3O4 (trong điều kiện không có không khí) thu được hỗn hợp rắn Y. Chia hỗn hợp Y thành 2 phần bằng nhau:
- Phần 1 cho vào dung dịch HNO3 (loãng, dư) thấy thoát ra 16,8 gam khí không màu, hóa nâu trong không khí (sản phẩm khử duy nhất của N+5).
- Phần 2 cho vào dung dịch KOH dư thấy thoát ra 8,064 lít khí H2 (đktc) và còn m gam rắn không tan.
Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của m là
 Xem đáp án
Xem đáp án
Phần 1: Y (1)
Phần 2: Y (2)
3y=1,68-0,72 y=0,32 =17,92 gam
Câu 34:
Muối đồng(II) sunfat khi ở dạng khan có màu trắng và khi kết tinh ngậm nước tạo thành dung dịch có màu xanh. Ở điều kiện nhiệt độ 20oC có 2730 gam dung dịch CuSO4 bão hòa. Sau đó, đun nóng dung dịch này lên đến 85oC thì dừng lại. Giả thiết rằng độ tan ở 20oC và 85oC của CuSO4 lần lượt là 36,5 và 87,7. Biết rằng độ tan của một chất ở nhiệt độ xác định là khối lượng chất đó tan trong 100 gam nước để tạo dung dịch bão hòa. Khối lượng CuSO4 cần thêm vào dung dịch để thu được dung dịch bão hòa ở nhiệt độ 85oC?
 Xem đáp án
Xem đáp án
- Ở 20oC, độ tan của CuSO4 là 36,5 36,5 gam CuSO4 hòa tan trong 100 gam nước tạo thành 136,5 gam dung dịch CuSO4
Với 2730 gam dung dịch ,
- Ở 85oC, độ tan của CuSO4 là 87,7 87,7 gam CuSO4 hòa tan trong 100 gam nước tạo thành 187,7 gam dung dịch CuSO4
Với 2000 gam H2O
Khối lượng CuSO4 cần thêm vào = 1754 – 730 = 1024 gam
Câu 35:
Cho các phát biểu sau:
(a) Benzyl axetat có mùi thơm hoa nhài, công thức phân tử của nó là C8H8O2.
(b) Trong cơ thể, chất béo bị oxi hóa chậm thành CO2, H2O và cung cấp năng lượng cho cơ thể.
(c) Khi cho nước cốt chanh vào sữa bò thì sữa bò bị kết tủa.
(d) Trong phòng thí nghiệm, không thể dùng dung dịch HCl để rửa sạch anilin dính trong ống nghiệm.
(e) Phenol không tham gia phản ứng thế.
(f) Trong tinh bột, hàm lượng của amilozơ lớn hơn amilopectin.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
(a) Sai, công thức của benzyl axetat là CH3COOCH2C6H5 (C9H10O2)
(b) Đúng theo ứng dụng của chất béo
(c) Đúng do xảy ra hiện tượng đông tụ protein
(d) Sai, có thể dùng HCl để rửa anilin dính trên ống nghiệm vì phản ứng tạo thành muối C6H5NH3Cl dễ bị rửa trôi
(e) Sai, phenol có phản ứng thế với brom tạo thành kết tủa trắng
(f) Sai, hàm lượng amilopectin lớn hơn amilozơ
Câu 36:
Hỗn hợp E gồm axit béo X và hai triglixerit Y, Z (MY < MZ); trong E tỉ lệ về khối lượng của cacbon và oxi là 167 : 24. Đốt cháy hoàn toàn m gam E cần dùng 4,785 mol O2, thu được 6,59 mol hỗn hợp gồm CO2 và H2O. Nếu đun nóng m gam E với dung dịch NaOH vừa đủ, cô cạn dung dịch sau phản ứng thu được (m + 2,44) gam hỗn hợp T gồm ba muối C15H31COONa, C17H33COONa và C17H35COONa. Thành phần phần trăm về khối lượng của Y trong hỗn hợp E là
 Xem đáp án
Xem đáp án
Xét E:
Xét T:
Câu 37:
Thực hiện thí nghiệm điện phân dung dịch CuSO4 theo hình vẽ dưới đây:
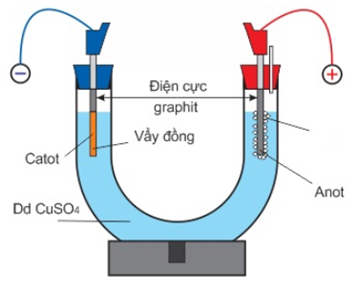
Cho các nhận định sau:
(a) Trong quá trình điện phân, pH của dung dịch sẽ giảm dần.
(b) Sau khi điện phân một thời gian, điện cực anot sẽ bị tan ra.
(c) Dung dịch sau điện phân có thể hòa tan được kẽm (vừa đủ).
(d) Nếu thay dung dịch CuSO4 bằng dung dịch CuCl2 thì bản chất của quá trình điện phân không thay đổi.
(e) Khi dung dịch CuSO4 bị điện phân hết, điện cực anot sẽ có khí không màu nhẹ hơn không khí thoát ra.
Số nhận định sai là
 Xem đáp án
Xem đáp án
(a) Đúng, phương trình điện phân CuSO4 + H2O Cu + O2 + H2SO4. Quá trình điện phân tạo thành H2SO4 nên pH sẽ giảm dần
(b) Sai, điện cực graphit là điện cực trơ nên sẽ không bị tan trong quá trình điện phân. Anot chỉ tan khi được làm từ đồng (hiện tượng dương cực tan)
(c) Đúng, vì dung dịch sau điện phân có chứa H2SO4 nên có thể hòa tan Zn
(d) Sai, bản chất sẽ thay đổi vì SO42- không bị điện phân còn Cl- sẽ bị điện phân thành khí Cl2
(e) Sai, điện cực anot sẽ thoát ra khí O2 (nặng hơn không khí)
Câu 39:
Thực hiện các thí nghiệm sau:
(a) Cho dung dịch chứa a mol KHSO4 vào dung dịch chứa a mol NaHCO3.
(b) Cho 1,6a mol CO2 vào dung dịch chứa a mol Ba(OH)2.
(c) Hòa tan a mol Fe3O4 vào dung dịch chứa 5a mol H2SO4 loãng.
(d) Cho dung dịch chứa a mol Ca(HCO3)2 vào dung dịch chứa a mol NaOH.
(e) Cho 2,5a mol NaOH vào dung dịch chứa a mol H3PO4.
(f) Hòa tan hỗn hợp gồm Cu và Fe3O4 (tỉ lệ mol 1 : 1) vào lượng dư dung dịch HCl loãng.
Sau khi phản ứng xảy ra hoàn toàn, số thí nghiệm thu được dung dịch chứa hai muối có số mol bằng nhau là
 Xem đáp án
Xem đáp án
(a) Đúng, dung dịch thu được chứa 0,5a mol K2SO4 và 0,5a mol Na2SO4
(b) Sai, dung dịch thu được chỉ chứa Ba(HCO3)2
(c) Đúng, dung dịch thu được chứa a mol FeSO4 và a mol Fe2(SO4)3
(d) Sai, dung dịch thu được chỉ chứa NaHCO3
(e) Đúng, dung dịch thu được chứa 0,5a mol Na2HPO4 và 0,5a mol Na3PO4
(f) Sai, dung dịch thu được chứa 1 mol CuCl2 và 3 mol FeCl3
Câu 40:
Đốt cháy hoàn toàn một lượng photpho trong oxi dư, thu được chất rắn X. Trộn lượng chất rắn X trên vào hỗn hợp rắn Y gồm Na, Na2O, K và K2O thu được m gam hỗn hợp Z. Hòa tan m gam Z vào nước dư thu được dung dịch T và 1,344 lít khí H2 (đktc). Cô cạn dung dịch T thu được 24,48 gam rắn. Mặt khác, cho hỗn hợp rắn Y trên tác dụng với lượng vừa đủ dung dịch HCl thu được dung dịch Q chứa 26,6 gam chất tan. Biết rằng tỉ lệ số mol của nguyên tố oxi trong X : số mol của nguyên tố oxi trong hỗn hợp Y là 15 : 7. Giá trị của m là
 Xem đáp án
Xem đáp án
Trường hợp 1:
Điền số điện tích \[ \to \] \[ \to \] Chuyển dịch điện tích
Ta có:
Chuyển dịch điện tích \[ \to \sum\limits_{}^{} {{n^ - }} = 3x - y = 2n_O^{2 - {\rm{ trong Y}}} + 2{n_{{H_2}}} = \frac{{0,5x.5.7}}{{15}} + 2.0,06{\rm{ (2)}}\]
Từ (1), (2) x < 0, y < 0 Loại
Trường hợp 2:
Điền số điện tích \[ \to \] \[ \to \] Chuyển dịch điện tích
Chuyển dịch điện tích \[ \to \sum\limits_{}^{} {{n^ - }} = 3x + y = 2n_O^{2 - {\rm{ trong Y}}} + 2{n_{{H_2}}} = \frac{{0,5x.5.7}}{{15}} + 2.0,06{\rm{ (2)}}\]
Từ (1), (2)

