Đề thi thử THPT môn Hóa năm 2022 có đáp án (Mới nhất) - Đề 4
-
8621 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
Muối ngậm nước CaSO4.2H2O có tên thường gọi là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Thạch cao khan là CaSO4
Thạch cao nung là CaSO4.H2O hoặc CaSO4.0,5H2O
Thạch cao sống là CaSO4.2H2O
Thạch cao khan là CaSO4
Thạch cao nung là CaSO4.H2O hoặc CaSO4.0,5H2O
Thạch cao sống là CaSO4.2H2O
Câu 2:
Chất hữu cơ X có đặc điểm sau: Phân tử có nhiều nhóm -OH, có vị ngọt, hòa tan được Cu(OH)2 ở nhiệt độ thường và tham gia phản ứng tráng gương. X là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
A. Sai vì xenlulozơ không phản ứng với Cu(OH)2
B. Sai vì không có nhóm chức anđehit (-CH=O) nên saccarozơ không có tính khử như glucozơ nên không tham gia phản ứng tráng gương
D. Sai vì tinh bột không phản ứng với Cu(OH)2
A. Sai vì xenlulozơ không phản ứng với Cu(OH)2
B. Sai vì không có nhóm chức anđehit (-CH=O) nên saccarozơ không có tính khử như glucozơ nên không tham gia phản ứng tráng gương
D. Sai vì tinh bột không phản ứng với Cu(OH)2
Câu 3:
Phát biểu nào sau đây là đúng?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
A sai vì đây là phản ứng một chiều.
B sai vì có những este khi thủy phân trong NaOH thu được muối, anđehit, xeton, nước.
HCOOCH = CH2 + NaOH HCOONa + CH3CHO
C đúng. Ví dụ: CH3COOCH3 + H2O CH3COOH + CH3OH
D sai vì este isoamyl axetat có mùi chuối chín.
A sai vì đây là phản ứng một chiều.
B sai vì có những este khi thủy phân trong NaOH thu được muối, anđehit, xeton, nước.
HCOOCH = CH2 + NaOH HCOONa + CH3CHO
C đúng. Ví dụ: CH3COOCH3 + H2O CH3COOH + CH3OH
D sai vì este isoamyl axetat có mùi chuối chín.
Câu 4:
Chất phản ứng được với dung dịch HCl và dung dịch NaOH là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Chất phản ứng được với dung dịch HCl và dung dịch NaOH là NaHCO3:
NaHCO3 + HCl → NaCl + CO2 + H2O
NaHCO3 + NaOH → Na2CO3 + H2O
Còn lại Na2CO3 chỉ phản ứng với HCl, không phản ứng với NaOH. Các chất NaCl, NaNO3 không phản ứng với cả HCl và NaOH
Chất phản ứng được với dung dịch HCl và dung dịch NaOH là NaHCO3:
NaHCO3 + HCl → NaCl + CO2 + H2O
NaHCO3 + NaOH → Na2CO3 + H2O
Còn lại Na2CO3 chỉ phản ứng với HCl, không phản ứng với NaOH. Các chất NaCl, NaNO3 không phản ứng với cả HCl và NaOH
Câu 5:
Sắt tây là sắt được tráng
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
- Sắt tây là sắt được tráng một lớp mỏng kim loại thiếc (Sn) bảo vệ sắt không bị ăn mòn theo phương pháp bảo vệ bề mặt.
- Sắt tráng kẽm được gọi là tôn.
- Sắt tây là sắt được tráng một lớp mỏng kim loại thiếc (Sn) bảo vệ sắt không bị ăn mòn theo phương pháp bảo vệ bề mặt.
- Sắt tráng kẽm được gọi là tôn.
Câu 6:
Điện phân dung dịch gồm NaCl và HCl (điện cực trơ, màng ngăn xốp). Trong quá trình điện phân, so với dung dịch ban đầu, giá trị pH của dung dịch thu được
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Ban đầu dung dịch có pH < 7
2HCl → H2 + Cl2
Khi HCl bị điện phân hết thì pH = 7
2NaCl + 2H2O H2 + Cl2 + 2NaOH
Do tạo NaOH nên pH > 7
→ pH tăng dần.
Ban đầu dung dịch có pH < 7
2HCl → H2 + Cl2
Khi HCl bị điện phân hết thì pH = 7
2NaCl + 2H2O H2 + Cl2 + 2NaOH
Do tạo NaOH nên pH > 7
→ pH tăng dần.
Câu 7:
Nhỏ vài giọt H2SO4 loãng vào dung dịch K2CrO4 thấy dung dịch chuyển sang màu
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Nhỏ vài giọt H2SO4 loãng vào dung dịch K2CrO4 thấy dung dịch chuyển sang màu da cam:
Nhỏ vài giọt H2SO4 loãng vào dung dịch K2CrO4 thấy dung dịch chuyển sang màu da cam:
2K2CrO4 (vàng) + H2SO4 → K2Cr2O7 (da cam) + K2SO4 + H2O
Câu 8:
Độ dinh dưỡng của phân lân được xác định theo phần trăm khối lượng
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Độ dinh dưỡng của phân đạm được đánh giá bằng hàm lượng %N trong phân.
Độ dinh dưỡng của phân lân được đánh giá bằng hàm lượng %P2O5 tương ứng với lượng photpho có trong thành phần của nó.
Độ dinh dưỡng của phân kali được đánh giá bằng hàm lượng %K2O tương ứng với lượng kali có trong thành phần của nó.
Độ dinh dưỡng của phân đạm được đánh giá bằng hàm lượng %N trong phân.
Độ dinh dưỡng của phân lân được đánh giá bằng hàm lượng %P2O5 tương ứng với lượng photpho có trong thành phần của nó.
Độ dinh dưỡng của phân kali được đánh giá bằng hàm lượng %K2O tương ứng với lượng kali có trong thành phần của nó.
Câu 9:
Kim loại có khối lượng riêng lớn nhất là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Kim loại có khối lượng riêng lớn nhất là Os
Kim loại có khối lượng riêng lớn nhất là Os
Câu 10:
Bằng phương pháp điện phân dung dịch có thể điều chế được kim loại
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Phương pháp điện phân dung dịch để điều chế các kim loại trung bình, yếu.(Sau Al)
Phương pháp điện phân dung dịch để điều chế các kim loại trung bình, yếu.(Sau Al)
Câu 11:
Trong phòng thí nghiệm, kim loại Na được bảo quản bằng cách ngâm trong
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Kim loại Na là một kim loại có tính khử mạnh, có khả năng phản ứng được với nhiều chất ngay ở nhiệt độ thường. Do đó trong phòng thí nghiệm Na thường được ngâm trong dầu hỏa để tránh tiếp xúc với môi trường không khí.
Kim loại Na là một kim loại có tính khử mạnh, có khả năng phản ứng được với nhiều chất ngay ở nhiệt độ thường. Do đó trong phòng thí nghiệm Na thường được ngâm trong dầu hỏa để tránh tiếp xúc với môi trường không khí.
Câu 12:
Ở nhiệt độ thường, dung dịch HNO3 đặc có thể chứa trong bình bằng kim loại
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Ở nhiệt độ thường, dung dịch HNO3 đặc có thể chứa trong bình bằng kim loại nhôm vì nhôm thụ động trong HNO3 đặc nguội.
Ở nhiệt độ thường, dung dịch HNO3 đặc có thể chứa trong bình bằng kim loại nhôm vì nhôm thụ động trong HNO3 đặc nguội.
Câu 13:
Số đồng phân este có công thức C4H8O2 là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Các đồng phân Este:
HCOO-CH2-CH2-CH3
HCOO-CH(CH3)2
CH3-COO-CH2-CH3
CH3-CH2-COO-CH3
Các đồng phân Este:
HCOO-CH2-CH2-CH3
HCOO-CH(CH3)2
CH3-COO-CH2-CH3
CH3-CH2-COO-CH3
Câu 14:
Trong số các ion sau, ion kim loại có tính oxi hóa mạnh nhất là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
K+ Na+ Mg2+ Al3+ Zn2+ Fe2+ Ni2+ Sn2+ Pb2+ H+ Cu2+ Fe3+ Ag+ Hg2+ Pt2+ Au3+
Tính oxi hóa tăng dần
Câu 15:
Khi đốt cháy este X thu được số mol CO2 lớn hơn số mol H2O. X có thể là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Khi đốt cháy este X thu được số mol CO2 lớn hơn số mol H2O → X có thể là metyl acrylat (CH2=CH- COOCH3)
Khi đốt cháy este X thu được số mol CO2 lớn hơn số mol H2O → X có thể là metyl acrylat (CH2=CH- COOCH3)
Câu 16:
Teflon là tên của một polime được dùng làm
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Teflon (-CF2-CF2-)n là tên của một polime được dùng làm chất dẻo.
Teflon (-CF2-CF2-)n là tên của một polime được dùng làm chất dẻo.
Câu 17:
Nhận định nào sau đây không đúng?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Sai, chúng đều có công thức phân tử dạng (C6H10O5)n nhưng giá trị n của xenlulozơ lớn hơn rất nhiều so với tinh bột nên chúng không phải là đồng phân của nhau.
Sai, chúng đều có công thức phân tử dạng (C6H10O5)n nhưng giá trị n của xenlulozơ lớn hơn rất nhiều so với tinh bột nên chúng không phải là đồng phân của nhau.
Câu 18:
Có thể điều chế Fe bằng cách dùng CO để khử
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Có thể điều chế Fe bằng cách dùng CO để khử Fe2O3 ở nhiệt độ cao:
Fe2O3 + 3CO 2Fe + 3CO2
Có thể điều chế Fe bằng cách dùng CO để khử Fe2O3 ở nhiệt độ cao:
Fe2O3 + 3CO 2Fe + 3CO2
Câu 19:
Muối mono natri của amino axit nào sau đây được dùng làm bột ngọt (mì chính)?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Axit glutamic: HOOC−CH2−CH2−CH(NH2) −COOH
Axit glutamic: HOOC−CH2−CH2−CH(NH2) −COOH
Câu 20:
Glucozơ và fructozơ đều
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
- Glucozơ và fructozơ đều không tham gia phản ứng thủy phân.
- Chỉ có glucozơ có nhóm chức −CHO.
- Glucozơ và fructozơ đều thuộc monosaccarit.
- Glucozơ và fructozơ đều không tham gia phản ứng thủy phân.
- Chỉ có glucozơ có nhóm chức −CHO.
- Glucozơ và fructozơ đều thuộc monosaccarit.
Câu 21:
Tiến hành thí nghiệm với các chất X, Y, Z, T. Kết quả được ghi ở bảng sau
|
Mẫu thử |
Thuốc thử |
Hiện tượng |
|
X, Z |
Quỳ tím |
Chuyển màu hồng |
|
Y |
Dung dịch AgNO3/NH3 |
Tạo kết tủa |
|
Z, Y |
Dung dịch Br2 |
Nhạt màu nâu đỏ |
|
T |
Cu(OH)2 |
Dung dịch màu tím |
X, Y, Z, T lần lượt là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Y, Z làm nhạt màu Br2 nên loại A (sai ở axit glutamic), loại C (sai ở axit benzoic), loại D (sai ở axit oxalic) → Chọn B.
3C4H4 + 6AgNO3 + 8NH3 → 3C4H4Ag2 + 6NH4NO3
C4H4 + 3Br2 → C4H4Br6
CH2=CH-COOH + Br2 → CH2(Br)-CH(Br)-COOH
Y, Z làm nhạt màu Br2 nên loại A (sai ở axit glutamic), loại C (sai ở axit benzoic), loại D (sai ở axit oxalic) → Chọn B.
3C4H4 + 6AgNO3 + 8NH3 → 3C4H4Ag2 + 6NH4NO3
C4H4 + 3Br2 → C4H4Br6
CH2=CH-COOH + Br2 → CH2(Br)-CH(Br)-COOH
Câu 22:
Phát biểu nào sau đây sai
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
A. Đúng, cặp điện cực Fe-C trong môi trường điện li là không khí ẩm
B. Sai. Nước cứng tạm thời chứa Ca(HCO3)2, Mg(HCO3)2
C. Đúng:
HCl + H2O + NaAlO2 → NaCl + Al(OH)3
Al(OH)3 + 3HCl → AlCl3 + 3H2O
A. Đúng, cặp điện cực Fe-C trong môi trường điện li là không khí ẩm
B. Sai. Nước cứng tạm thời chứa Ca(HCO3)2, Mg(HCO3)2
C. Đúng:
HCl + H2O + NaAlO2 → NaCl + Al(OH)3
Al(OH)3 + 3HCl → AlCl3 + 3H2O
Câu 23:
Cho 9,97 gam hỗn hợp X gồm lysin và alanin tác dụng vừa đủ với dung dịch NaOH thu được 11,73 gam muối. Mặt khác 9,97 gam hỗn hợp X trên tác dụng với dung dịch HCl dư thu được dung dịch Y. Cô cạn dung dịch Y được m gam muối khan. Giá trị của m là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Đặt a, b là số mol Ala, Lys
mX = 89a + 146b = 9,97
nX = a + b =
→ a = 0,03; b = 0,05
nHCl = nN = a + 2b = 0,13
→ m muối = mX + mHCl = 14,715 gam
Đặt a, b là số mol Ala, Lys
mX = 89a + 146b = 9,97
nX = a + b =
→ a = 0,03; b = 0,05
nHCl = nN = a + 2b = 0,13
→ m muối = mX + mHCl = 14,715 gam
Câu 24:
Hòa tan hết 3,24 gam kim loại X trong 100 ml dung dịch NaOH 1,5M thu được 4,032 lít H2 (đktc) và dung dịch Y. Kim loại X là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
nH2 = 0,18
Kim loại X hóa trị n, bảo toàn electron: 3,24 = 0,18.2 → X = 9n
→ n = 3, X = 27: X là Al
nH2 = 0,18
Kim loại X hóa trị n, bảo toàn electron: 3,24 = 0,18.2 → X = 9n
→ n = 3, X = 27: X là Al
Câu 25:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
(C17H33COO)3C3H5 + 3H2 → (C17H35COO)3C3H5
(C17H33COO)3C3H5 + 3NaOH → 3C17H35COONa + C3H5(OH)3
C17H35COONa + HCl → C17H35COOH + NaCl
→ Z là axit stearic.
(C17H33COO)3C3H5 + 3H2 → (C17H35COO)3C3H5
(C17H33COO)3C3H5 + 3NaOH → 3C17H35COONa + C3H5(OH)3
C17H35COONa + HCl → C17H35COOH + NaCl
→ Z là axit stearic.
Câu 26:
Đốt cháy hoàn toàn 3,1 gam photpho trong khí oxi dư. Sau đó cho toàn bộ sản phẩm vào 9,6 gam NaOH, thu được dung dịch X. Khối lượng từng chất tan trong dung dịch X là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
nP = 0,1 mol; nNaOH = 0,24 mol
→ = 2,4 → Tạo Na3PO4 (a) và Na2HPO4 (b)
nP = a + b = 0,1
nNaOH = 3a + 2b = 0,24
→ a = 0,04; b = 0,06
→ nNa3PO4 = 6,56; mNa2HPO4 = 8,52
nP = 0,1 mol; nNaOH = 0,24 mol
→ = 2,4 → Tạo Na3PO4 (a) và Na2HPO4 (b)
nP = a + b = 0,1
nNaOH = 3a + 2b = 0,24
→ a = 0,04; b = 0,06
→ nNa3PO4 = 6,56; mNa2HPO4 = 8,52
Câu 27:
Cho hỗn hợp Cu và Fe3O4 vào dung dịch H2SO4 loãng dư. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch X và một lượng chất rắn không tan. Muối trong dung dịch X là :
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Fe3O4 + H2SO4 → Fe2(SO4)3 + FeSO4 + H2O
Cu + Fe2(SO4)3 → CuSO4 + FeSO4
Chất rắn không tan là Cu dư → Muối trong dung dịch chỉ có FeSO4 và CuSO4
Fe3O4 + H2SO4 → Fe2(SO4)3 + FeSO4 + H2O
Cu + Fe2(SO4)3 → CuSO4 + FeSO4
Chất rắn không tan là Cu dư → Muối trong dung dịch chỉ có FeSO4 và CuSO4
Câu 28:
Hình vẽ sau đây mô tả thí nghiệm điều chế khí Y từ hỗn hợp rắn gồm CaC2 và Al4C3:
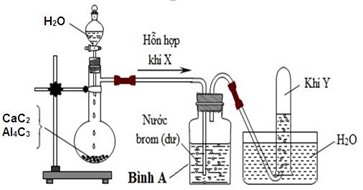
Vậy khí Y là:

Vậy khí Y là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
CaC2 + 2H2O → Ca(OH)2 + C2H2↑
Al4C3 + 12H2O → 4Al(OH)3↓ + 3CH4↑
Hỗn hợp khí X có chứa C2H2 và CH4. Cho hh này qua dung dịch Br2 thì C2H2 bị giữ lại, còn CH4 thoát ra ngoài.
C2H2 + 2Br2 → C2H2Br4
Vì CH4 không tan trong nước bằng cách đẩy nước. ⇒ Khí Y là CH4
CaC2 + 2H2O → Ca(OH)2 + C2H2↑
Al4C3 + 12H2O → 4Al(OH)3↓ + 3CH4↑
Hỗn hợp khí X có chứa C2H2 và CH4. Cho hh này qua dung dịch Br2 thì C2H2 bị giữ lại, còn CH4 thoát ra ngoài.
C2H2 + 2Br2 → C2H2Br4
Vì CH4 không tan trong nước bằng cách đẩy nước. ⇒ Khí Y là CH4
Câu 29:
Cho hợp chất hữu cơ X (C5H8O4) thuần chức, mạch hở. Đun nóng X với dung dịch NaOH chỉ thu được hai chất hữu cơ Y và Z. Hiđro hóa Z thu được ancol T. Biết X tham gia phản ứng tráng bạc. Nhận định nào sau đây không chính xác?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
X tráng bạc nên X chứa gốc HCOO-.
Hiđro hóa Z tạo ancol T nên Z là anđehit hoặc xeton.
→ X là (HCOO)2CH-C2H5 hoặc (HCOO)2C(CH3)2
Y là HCOONa
Z là C2H5-CHO hoặc CH3COCH3
T là C2H5-CH2OH hoặc CH3CHOHCH3
→ Phát biểu D không chính xác.
X tráng bạc nên X chứa gốc HCOO-.
Hiđro hóa Z tạo ancol T nên Z là anđehit hoặc xeton.
→ X là (HCOO)2CH-C2H5 hoặc (HCOO)2C(CH3)2
Y là HCOONa
Z là C2H5-CHO hoặc CH3COCH3
T là C2H5-CH2OH hoặc CH3CHOHCH3
→ Phát biểu D không chính xác.
Câu 30:
Tiến hành các thí nghiệm sau:
(a) Cho Fe3O4 vào lượng dư dung dịch HCl.
(b) Cho Al2O3 vào lượng dư dung dịch NaOH.
(c) Cho Mg vào dung dịch HNO3 loãng, lạnh (phản ứng không thu được chất khí).
(d) Cho Fe vào dung dịch Fe2(SO4)3 dư.
(e) Cho dung dịch chứa a mol KHSO4 vào dung dịch chứa a mol NaHCO3.
(g) Cho dung dịch Fe(NO3)2 vào dung dịch AgNO3 dư.
Sau khi các phản ứng xảy ra hoàn toàn thì số thí nghiệm thu được dung dịch chứa hai muối là
(a) Cho Fe3O4 vào lượng dư dung dịch HCl.
(b) Cho Al2O3 vào lượng dư dung dịch NaOH.
(c) Cho Mg vào dung dịch HNO3 loãng, lạnh (phản ứng không thu được chất khí).
(d) Cho Fe vào dung dịch Fe2(SO4)3 dư.
(e) Cho dung dịch chứa a mol KHSO4 vào dung dịch chứa a mol NaHCO3.
(g) Cho dung dịch Fe(NO3)2 vào dung dịch AgNO3 dư.
Sau khi các phản ứng xảy ra hoàn toàn thì số thí nghiệm thu được dung dịch chứa hai muối là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
(a) Fe3O4 + 8HCl → FeCl2 + 2FeCl3 + 4H2O
(b) Al2O3 + 2NaOH → 2NaAlO2 + H2O
(c) 4Mg + 10HNO3 → 4Mg(NO3)2 + NH4NO3 + 3H2O
(d) Fe + Fe2(SO4)3 dư → 3FeSO4
(e) 2KHSO4 + 2NaHCO3 → K2SO4 + Na2SO4 + CO2 + H2O
(g) Fe(NO3)2 + AgNO3 dư → Fe(NO3)3 + Ag
(a) Fe3O4 + 8HCl → FeCl2 + 2FeCl3 + 4H2O
(b) Al2O3 + 2NaOH → 2NaAlO2 + H2O
(c) 4Mg + 10HNO3 → 4Mg(NO3)2 + NH4NO3 + 3H2O
(d) Fe + Fe2(SO4)3 dư → 3FeSO4
(e) 2KHSO4 + 2NaHCO3 → K2SO4 + Na2SO4 + CO2 + H2O
(g) Fe(NO3)2 + AgNO3 dư → Fe(NO3)3 + Ag
Câu 31:
Cho m gam hỗn hợp gồm Na, Na2O, Ba, BaO (trong đó tỉ lệ khối lượng giữa kim loại và oxi là 10 : 1) tác dụng với một lượng dư H2O, thu được 1,12 lít H2 (đktc) và 300 ml dung dịch X. Cho X tác dụng với 200 ml dung dịch chứa hỗn hợp gồm H2SO4 0,25M và HCl 0,3M, thu được 500 ml dung dịch có pH = 1,7. Giá trị của m gần nhất với
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
nH2SO4 = 0,05; nHCl = 0,06 → nH+ = 0,16
pH = 1,7 → [H+] = 0,02 → nH+ dư = 0,01
→ nOH- = 0,15 = 2nO + 2nH2
→ nO = 0,025
→ m = 11.0,025.16 = 4,4 gam
nH2SO4 = 0,05; nHCl = 0,06 → nH+ = 0,16
pH = 1,7 → [H+] = 0,02 → nH+ dư = 0,01
→ nOH- = 0,15 = 2nO + 2nH2
→ nO = 0,025
→ m = 11.0,025.16 = 4,4 gam
Câu 32:
Cho các phát biểu sau
(a) Không nên dùng dầu, mỡ động thực vật để lâu trong không khí.
(b) Tơ là những vật liệu polime hình sợi dài, mảnh với độ bền nhất định.
(c) Hầu hết các polime là những chất rắn, không bay hơi, có nhiệt độ nóng chảy xác định.
(d) Sự đông tụ và kết tủa protein xảy ra khi đun nóng hoặc cho axit, bazơ hoặc một số muối vào dung dịch protein.
(e) Cao su lưu hóa có tinh đàn hồi, chịu nhiệt, lâu mòn, khó tan trong các dung môi hơn cao su thường. Số phát biểu đúng là
(a) Không nên dùng dầu, mỡ động thực vật để lâu trong không khí.
(b) Tơ là những vật liệu polime hình sợi dài, mảnh với độ bền nhất định.
(c) Hầu hết các polime là những chất rắn, không bay hơi, có nhiệt độ nóng chảy xác định.
(d) Sự đông tụ và kết tủa protein xảy ra khi đun nóng hoặc cho axit, bazơ hoặc một số muối vào dung dịch protein.
(e) Cao su lưu hóa có tinh đàn hồi, chịu nhiệt, lâu mòn, khó tan trong các dung môi hơn cao su thường. Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
(a) Đúng, dầu mỡ để lâu trong không khí sẽ bị oxi hóa tạo ra nhiều chất độc hại.
(c) Sai, polime có nhiệt độ nóng chảy không xác định
(a) Đúng, dầu mỡ để lâu trong không khí sẽ bị oxi hóa tạo ra nhiều chất độc hại.
(c) Sai, polime có nhiệt độ nóng chảy không xác định
Câu 33:
Hỗn hợp X chứa hai amin kế tiếp thuộc dãy đồng đẳng của metyl amin. Hỗn hợp Y chứa glyxin và lysin. Đốt cháy hoàn toàn 0,2 mol hỗn hợp Z (gồm X và Y) cần vừa đủ 1,035 mol O2, thu được 16,38 gam H2O; 18,144 lít (đktc) hỗn hợp CO2 và N2. Phần trăm khối lượng amin có khối lượng phân tử nhỏ hơn trong Z là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Amin = CH3NH2 + ?CH2 (1)
Lys = C2H5NO2 + 4CH2 + NH (2)
Quy đổi Z thành CH3NH2 (a), C2H5NO2 (b), CH2 (c) và NH (d)
nZ = a + b = 0,2
nO2 = 2,25a + 2,25b + 1,5c + 0,25d = 1,035
nH2O = 2,5a + 2,5b + c + 0,5d = 0,91
nCO2 + nN2 = (a + 2b + c) + = 0,81
→ a = 0,1; b = 0,1; c = 0,38; d = 0,06
→ mZ = 16,82
nCH2 (1) = c – nCH2 (2) = 0,14
nCH3CH2 = 0,1 → Số CH2 trung bình = 1,4
→ C2H5NH2 (0,06) và C3H7NH2 (0,04)
→ %C2H5NH2 = 16,05%
Amin = CH3NH2 + ?CH2 (1)
Lys = C2H5NO2 + 4CH2 + NH (2)
Quy đổi Z thành CH3NH2 (a), C2H5NO2 (b), CH2 (c) và NH (d)
nZ = a + b = 0,2
nO2 = 2,25a + 2,25b + 1,5c + 0,25d = 1,035
nH2O = 2,5a + 2,5b + c + 0,5d = 0,91
nCO2 + nN2 = (a + 2b + c) + = 0,81
→ a = 0,1; b = 0,1; c = 0,38; d = 0,06
→ mZ = 16,82
nCH2 (1) = c – nCH2 (2) = 0,14
nCH3CH2 = 0,1 → Số CH2 trung bình = 1,4
→ C2H5NH2 (0,06) và C3H7NH2 (0,04)
→ %C2H5NH2 = 16,05%
Câu 34:
Thực hiện các thí nghiệm sau:
(a) Cho Na dư vào cốc chứa ancol etylic.
(b) Đun nóng tripanmitin với dung dịch NaOH dư.
(c) Cho nhúm bông vào dung dịch H2SO4 đặc, đun nóng.
(d) Cho dung dịch HCl vào dung dịch axit glutamic.
(e) Đun nóng axit amino axetic với ancol metylic có khí HCl làm xúc tác.
(g) Cho dung dịch fructozơ vào dung dịch AgNO3/NH3 đun nóng. Số thí nghiệm xảy ra phản ứng là
(a) Cho Na dư vào cốc chứa ancol etylic.
(b) Đun nóng tripanmitin với dung dịch NaOH dư.
(c) Cho nhúm bông vào dung dịch H2SO4 đặc, đun nóng.
(d) Cho dung dịch HCl vào dung dịch axit glutamic.
(e) Đun nóng axit amino axetic với ancol metylic có khí HCl làm xúc tác.
(g) Cho dung dịch fructozơ vào dung dịch AgNO3/NH3 đun nóng. Số thí nghiệm xảy ra phản ứng là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Tất cả đều phản ứng:
(a) 2Na + 2C2H5OH → 2C2H5ONa + H2
(b) (C15H31COO)3C3H5 + 3NaOH → 3C15H31COONa + C3H5(OH)3
(c) 12n(C6H10O5)n + H2SO4 → 6nCO2 + 12nSO2 + 17nH2O
(d) HCl + NH2-C3H5(COOH)2 → ClH3N-C3H5(COOH)2
(e) NH2-CH2-COOH + CH3OH + HCl → H3NCl-CH2-COOCH3 + H2O
(g) Fructozơ ⇔ Glucozơ → 2Ag
Tất cả đều phản ứng:
(a) 2Na + 2C2H5OH → 2C2H5ONa + H2
(b) (C15H31COO)3C3H5 + 3NaOH → 3C15H31COONa + C3H5(OH)3
(c) 12n(C6H10O5)n + H2SO4 → 6nCO2 + 12nSO2 + 17nH2O
(d) HCl + NH2-C3H5(COOH)2 → ClH3N-C3H5(COOH)2
(e) NH2-CH2-COOH + CH3OH + HCl → H3NCl-CH2-COOCH3 + H2O
(g) Fructozơ ⇔ Glucozơ → 2Ag
Câu 35:
Tiến hành phản ứng nhiệt nhôm hoàn toàn hỗn hợp Al và 8 gam Fe2O3 thu được hỗn hợp rắn X. Cho X tác dụng vừa đủ với V ml dung dịch NaOH 1,5M sinh ra 1,68 lít H2 (ở đktc). Giá trị của V là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Bảo toàn electron: 3nAl = 2nH2 + 6nFe2O3
→ nAl = 0,15
→ nNaOH = nAlO2 = nAl = 0,15 → V = 100 ml
Bảo toàn electron: 3nAl = 2nH2 + 6nFe2O3
→ nAl = 0,15
→ nNaOH = nAlO2 = nAl = 0,15 → V = 100 ml
Câu 36:
Cho 33,4 gam hỗn hợp rắn X gồm Mg, MgO, Fe(NO3)2 và FeCO3 vào dung dịch chứa 1,29 mol HCl và 0,166 HNO3, khuấy đều cho các phản ứng xảy ra hoàn toàn, thu được dung dịch Y chỉ chứa các muối và 0,163 mol hỗn hợp khí Z gồm N2O, N2 và 0,1 mol CO2. Cho dung dịch AgNO3 dư vào dung dịch Y thu được 191,595 gam kết tủa. Nếu tác dụng tối đa với các chất tan có trong dung dịch Y cần dùng dung dịch chứa 1,39 mol KOH. Biết rằng tổng số mol nguyên tử oxi có trong X là 0,68 mol. Số mol của N2 có trong Z là bao nhiêu:
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
nKOH = 3a + 2b + c + 0,06.2 = 1,39 (1)
→ d = 0,1
nFeCO3 = 0,1 → nFe(NO3)2 = a + 0,06 – 0,1 = a – 0,04
Bảo toàn N:
2(a – 0,04) + 0,166 = 2.(0,163 – 0,1) + c + 0,1 (2)
nO = = 0,68 (3)
Giải hệ (1), (2), (3) → a = 0,09; b = 0,48; c = 0,04
Bảo toàn H → nH2O = 0,648
u, v là số mol N2 và N2O → u + v = 0,063
Bảo toàn khối lượng: 28u + 44v = 2,244
→ u = 0,033 và v = 0,03
nKOH = 3a + 2b + c + 0,06.2 = 1,39 (1)
→ d = 0,1
nFeCO3 = 0,1 → nFe(NO3)2 = a + 0,06 – 0,1 = a – 0,04
Bảo toàn N:
2(a – 0,04) + 0,166 = 2.(0,163 – 0,1) + c + 0,1 (2)
nO = = 0,68 (3)
Giải hệ (1), (2), (3) → a = 0,09; b = 0,48; c = 0,04
Bảo toàn H → nH2O = 0,648
u, v là số mol N2 và N2O → u + v = 0,063
Bảo toàn khối lượng: 28u + 44v = 2,244
→ u = 0,033 và v = 0,03
Câu 37:
Đốt cháy hoàn toàn hỗn hợp gồm chất béo X (x mol) và chất béo Y (y mol) (MX > MY) thu được số mol CO2 nhiều hơn số mol nước là 0,15. Mặt khác cùng lượng hỗn hợp trên tác dụng tối đa với 0,07 mol Br2 trong dung dịch. Biết thủy phân hoàn toàn X hoặc Y đều thu được muối của axit oleic và axit stearic. Tỷ lệ x : y có giá trị gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
X và Y đều tạo bởi axit oleic và axit stearic; MX > MY nên: X là (C17H33COO)(C17H35COO)2C3H5 (k = 4)
Y là (C17H33COO)2(C17H35COO)C3H5 (k = 5)
nCO2 – nH2O = 3x + 4y = 0,15
nBr2 = x + 2y = 0,07
→ x = 0,01 và y = 0,03
→ x : y = 1 : 3
X và Y đều tạo bởi axit oleic và axit stearic; MX > MY nên: X là (C17H33COO)(C17H35COO)2C3H5 (k = 4)
Y là (C17H33COO)2(C17H35COO)C3H5 (k = 5)
nCO2 – nH2O = 3x + 4y = 0,15
nBr2 = x + 2y = 0,07
→ x = 0,01 và y = 0,03
→ x : y = 1 : 3
Câu 38:
A là hỗn hợp chứa một axit (X) RCOOH, một ancol hai chức (Y) R’(OH)2 và một este hai chức (Z) (R”COO)2R’ (biết X, Y, Z đều no, mạch hở). Đốt cháy hoàn toàn 0,09 mol A cần 11,088 lít khí O2 (đktc). Sau phản ứng thấy khối lượng của CO2 lớn hơn khối lượng của H2O là 11,10 gam. Mặt khác, 15,03 gam A tác dụng vừa đủ với 0,15 mol KOH. Cô cạn dung dịch sau phản ứng thu được m gam muối khan và một ancol duy nhất là etylenglycol. Giá trị của m gần nhất với:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Quy đổi hỗn hợp A thành:
CnH2nO2: a mol, C2H4(OH)2: b mol
H2O: -c mol
CnH2nO2 + (1,5n – 1)O2 → nCO2 + nH2O
C2H4(OH)2 + 2,5O2 → 2CO2 + 3H2O
nA = a + b – c = 0,09 (1)
nO2 = a(1,5n – 1) + 2,5b = 0,495 (2)
mCO2 – mH2O = 44(na + 2b) – 18(na + 3b – c) = 11,1 (3)
Tỷ lệ:
là cố định, không phụ thuộc lượng A nên:
Giải hệ trên được: a = 0,1; b = 0,07; c = 0,08; na = 0,28
→ n = 2,8
Muối là CnH2n-1O2K (0,15 mol)
→ m muối = 16,38 gam
Quy đổi hỗn hợp A thành:
CnH2nO2: a mol, C2H4(OH)2: b mol
H2O: -c mol
CnH2nO2 + (1,5n – 1)O2 → nCO2 + nH2O
C2H4(OH)2 + 2,5O2 → 2CO2 + 3H2O
nA = a + b – c = 0,09 (1)
nO2 = a(1,5n – 1) + 2,5b = 0,495 (2)
mCO2 – mH2O = 44(na + 2b) – 18(na + 3b – c) = 11,1 (3)
Tỷ lệ:
là cố định, không phụ thuộc lượng A nên:
Giải hệ trên được: a = 0,1; b = 0,07; c = 0,08; na = 0,28
→ n = 2,8
Muối là CnH2n-1O2K (0,15 mol)
→ m muối = 16,38 gam
Câu 39:
Tiến hành thí nghiệm theo các bước sau:
Bước 1: Cho vào ống nghiệm 1-2 ml dung dịch hồ tinh bột. Bước 2: Nhỏ vài giọt dung dịch iot vào ống nghiệm đó.
Bước 3: Đun nóng dung dịch trong ống nghiệm một lát trên ngọn lửa đèn cồn, không để dung dịch sôi. Bước 4: Làm nguội dung dịch trong ống nghiệm vừa đun ở bước 3 bằng cách ngâm ống nghiệm trong cốc thủy tinh chứa nước ở nhiệt độ thường.
Cho các phát biểu sau:
(1) Dung dịch ở bước 1 có khả năng hòa tan Cu(OH)2 tạo dung dịch có màu xanh lam.
(2) Sau bước 2, dung dịch trong ống nghiệm có màu xanh tím.
(3) Ở bước 3, màu xanh tim của dung dịch trong ống nghiệm bị nhạt dần hoặc mất màu.
(4) Sau bước 4, màu xanh tím của dung dịch trong ống nghiệm sẽ biến mất hoàn toàn.
(5) Ở bước 1, nếu thay tinh bột bằng glucozơ thì các hiện tượng thí nghiệm sau bước 2 vẫn xảy ra tương tự.
Số phát biểu đúng là
Bước 1: Cho vào ống nghiệm 1-2 ml dung dịch hồ tinh bột. Bước 2: Nhỏ vài giọt dung dịch iot vào ống nghiệm đó.
Bước 3: Đun nóng dung dịch trong ống nghiệm một lát trên ngọn lửa đèn cồn, không để dung dịch sôi. Bước 4: Làm nguội dung dịch trong ống nghiệm vừa đun ở bước 3 bằng cách ngâm ống nghiệm trong cốc thủy tinh chứa nước ở nhiệt độ thường.
Cho các phát biểu sau:
(1) Dung dịch ở bước 1 có khả năng hòa tan Cu(OH)2 tạo dung dịch có màu xanh lam.
(2) Sau bước 2, dung dịch trong ống nghiệm có màu xanh tím.
(3) Ở bước 3, màu xanh tim của dung dịch trong ống nghiệm bị nhạt dần hoặc mất màu.
(4) Sau bước 4, màu xanh tím của dung dịch trong ống nghiệm sẽ biến mất hoàn toàn.
(5) Ở bước 1, nếu thay tinh bột bằng glucozơ thì các hiện tượng thí nghiệm sau bước 2 vẫn xảy ra tương tự.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
(1) Sai, hồ tinh bột không có tính chất này
(2) Đúng
(3) Đúng
(4) Sai, khi làm lạnh màu xanh tím xuất hiện trở lại
(5) Sai, glucozơ không có phản ứng màu với I2.
(1) Sai, hồ tinh bột không có tính chất này
(2) Đúng
(3) Đúng
(4) Sai, khi làm lạnh màu xanh tím xuất hiện trở lại
(5) Sai, glucozơ không có phản ứng màu với I2.
Câu 40:
X là este no, đơn chức; Y là este đơn chức, không no chứa một liên kết đôi C=C (X, Y đều mạch hở). Đốt cháy hoàn toàn 0,08 mol hỗn hợp E chứa X, Y (số mol X lớn hơn số mol Y) cần dùng 7,28 lít O2 (đktc). Mặt khác đun nóng 0,08 mol E với dung dịch NaOH (lấy dư 20% so với phản ứng), cô cạn dung dịch sau phản ứng thu được m gam rắn khan và hỗn hợp F chứa 2 ancol đồng đẳng kế tiếp. Đun nóng F với CuO thu được hỗn hợp chứa 2 andehit, lấy toàn bộ hỗn hợp 2 andehit này tác dụng với AgNO3/NH3 thu được 28,08 gam Ag. Giá trị m là.
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
nAnđehit = nF = nE = 0,08
nAg = 0,26 > 2nAnđehit → Anđehit gồm HCHO (0,05) và CH3CHO (0,03)
Do nX > nY nên nX = 0,05 và nY = 0,03
→ F gồm CH3OH (0,05) và C2H5OH (0,03)
X = CO2 + ?CH2 + H2
Y = CO2 + ?CH2
Quy đổi E thành CH2 (a), H2 (0,05) và CO2 (0,08)
nO2 = 1,5a + 0,05.0,5 = 0,325 → a = 0,2
→ mE = 6,42
nNaOH phản ứng = 0,08 → nNaOH đã dùng = 0,08 + 0,08.20% = 0,096
Bảo toàn khối lượng:
mE + mNaOH = m rắn + mF
→ m rắn = 7,28g
nAnđehit = nF = nE = 0,08
nAg = 0,26 > 2nAnđehit → Anđehit gồm HCHO (0,05) và CH3CHO (0,03)
Do nX > nY nên nX = 0,05 và nY = 0,03
→ F gồm CH3OH (0,05) và C2H5OH (0,03)
X = CO2 + ?CH2 + H2
Y = CO2 + ?CH2
Quy đổi E thành CH2 (a), H2 (0,05) và CO2 (0,08)
nO2 = 1,5a + 0,05.0,5 = 0,325 → a = 0,2
→ mE = 6,42
nNaOH phản ứng = 0,08 → nNaOH đã dùng = 0,08 + 0,08.20% = 0,096
Bảo toàn khối lượng:
mE + mNaOH = m rắn + mF
→ m rắn = 7,28g
